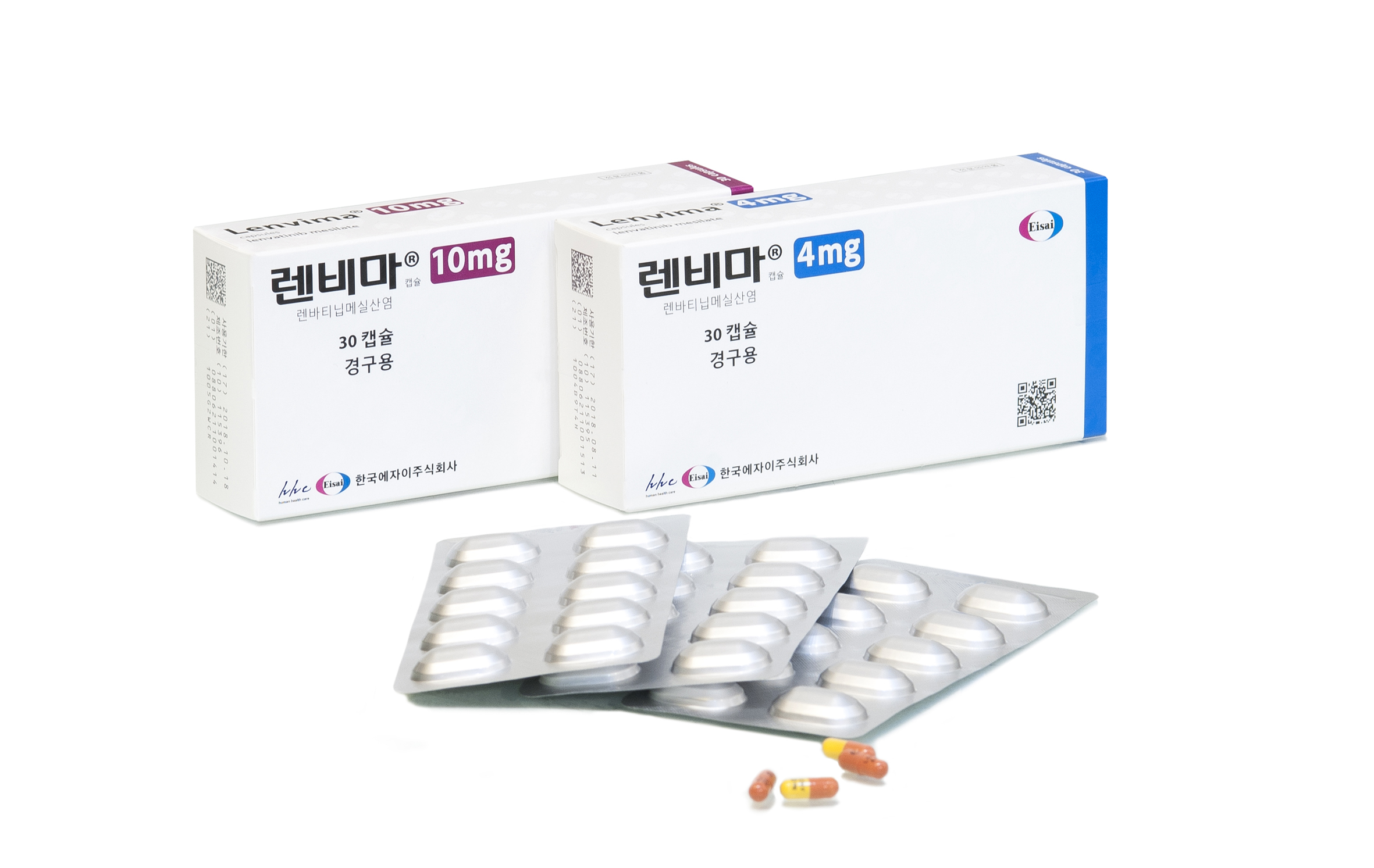
에자이(대표 하루오 나이토)는 절제가 불가능한 간세포암에 대한 1차 치료제로서 비교제품인 소라페닙 대비 자사가 연구개발한 항암제인 렌비마(성분명 렌바티닙메실산염, 이하 '렌바티닙')를 평가하는 3상 임상인 'Study 304'가 1차 유효성 평가변수를 만족시켰다고 발표했다.
Study 304는 간세포암 표준 치료제인 소라페닙 대비 절제가 불가능한 간세포암 환자에 대한 1차 치료제로서 렌바티닙의 효능과 안전성을 평가하는 다기관 무작위 공개형 글로벌 3상 임상이다. 해당 연구에서 954명의 참가자는 1:1 비율로 무작위로 배정되어 기준 체중에 따라 렌바티닙 12mg 또는 8mg을 1일 1회 (478명) 또는 소라페닙 400mg을 1일 2회 (476명) 투여 받았다. 해당 치료는 질병이 진행되거나 수용할 수 없는 독성이 발생할 때까지 지속되었다.
해당 임상은 전체생존(OS)을 1차 유효성 평가변수로 채택하여, 전체생존에 있어 비열등성을 입증하는 것을 목표로 설정하였다. 다른 평가변수에는 무진행 생존 (PFS), 질병진행기간(TTP) 객관적 반응률(ORR)이 있었다.
임상 결과에 따르면 렌바티닙은 소라페닙 대비 OS의 비열등성에 대한 통계적 기준을 만족시켰으며 PFS, TTP 및 ORR에 대해 통계학적으로 유의하고 임상적으로 의미가 있는 개선을 보였다.
렌바티닙 치료군에서 가장 많이 나타난 다섯 가지의 이상반응은 고혈압, 설사, 식욕 감퇴, 체중 감소, 피로감이었으며, 이는 렌바티닙의 기 알려진 부작용 프로파일과 일치한다. 삶의 질, 혈장 약동학 변수, 안전성과 같은 기타 2차 유효성 평가변수에 대한 분석은 현재 진행 중이다.
에자이는 일본, 미국, 유럽 및 중국 등 아시아 시장 허가 신청 관련 규제 당국과 논의를 진행할 예정이며, 오는 학회에서도 관련 내용을 소개할 계획이다.
한편 간암은 암으로 인한 사망 가운데 두 번째로 높은 비율을 차지하며 세계적으로 연간 약 70만명이 사망하는 암으로 대부분 중국과 같은 아시아 국가와 아프리카에서 발생한다. 간세포암은 원발성 간암의 85%~90%를 차지한다. 초기 단계의 간세포암은 수술, 고주파 열치료, 에탄올 주입술, 화학색전술 등 다양한 방법으로 치료가 가능하나 절제가 불가능한 간세포암종의 치료는 제한적이고 예후가 좋지 않아 의학적으로 아직 충족되지 못한 요구가 높다.
| 인기기사 | 더보기 + |
-
1 프로티나, 미국 IDT와 MOU 체결... 차세대 항체 치료제 개발 가속 -
2 '조 단위' R&D 시대 명암… 제약업계, 속도와 실속 사이 답 찾다 -
3 차백신연구소, 김병록 경영지배인 선임 -
4 약가유연계약 제도화…신약 약가협상 방식 바뀐다 -
5 ‘살 빼는 약’ 넘어 ‘만성질환 플랫폼’으로…위고비 새 데이터 대거 공개 -
6 ‘새 시대’ 꺼낸 다케다…대규모 감원과 신약 출시 전략 병행 -
7 에이비엘바이오, 그랩바디-B 'RNA 치료제' 뇌 전달 허들 넘나 -
8 제네릭 약가 45% 시대 개막… 정부의 보상 핀셋 '수급안정·원료자립' 향했다 -
9 약가유연계약제 6월 전면 시행… 제약업계 글로벌 진출 든든한 방어막 구축 -
10 ‘위고비’ 정제 체중 21.6% 감소‧운동성 2배 향상
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 신은진 기자 ejshin@yakup.com
- 입력 2017.02.07 10:55

에자이(대표 하루오 나이토)는 절제가 불가능한 간세포암에 대한 1차 치료제로서 비교제품인 소라페닙 대비 자사가 연구개발한 항암제인 렌비마(성분명 렌바티닙메실산염, 이하 '렌바티닙')를 평가하는 3상 임상인 'Study 304'가 1차 유효성 평가변수를 만족시켰다고 발표했다.
Study 304는 간세포암 표준 치료제인 소라페닙 대비 절제가 불가능한 간세포암 환자에 대한 1차 치료제로서 렌바티닙의 효능과 안전성을 평가하는 다기관 무작위 공개형 글로벌 3상 임상이다. 해당 연구에서 954명의 참가자는 1:1 비율로 무작위로 배정되어 기준 체중에 따라 렌바티닙 12mg 또는 8mg을 1일 1회 (478명) 또는 소라페닙 400mg을 1일 2회 (476명) 투여 받았다. 해당 치료는 질병이 진행되거나 수용할 수 없는 독성이 발생할 때까지 지속되었다.
해당 임상은 전체생존(OS)을 1차 유효성 평가변수로 채택하여, 전체생존에 있어 비열등성을 입증하는 것을 목표로 설정하였다. 다른 평가변수에는 무진행 생존 (PFS), 질병진행기간(TTP) 객관적 반응률(ORR)이 있었다.
임상 결과에 따르면 렌바티닙은 소라페닙 대비 OS의 비열등성에 대한 통계적 기준을 만족시켰으며 PFS, TTP 및 ORR에 대해 통계학적으로 유의하고 임상적으로 의미가 있는 개선을 보였다.
렌바티닙 치료군에서 가장 많이 나타난 다섯 가지의 이상반응은 고혈압, 설사, 식욕 감퇴, 체중 감소, 피로감이었으며, 이는 렌바티닙의 기 알려진 부작용 프로파일과 일치한다. 삶의 질, 혈장 약동학 변수, 안전성과 같은 기타 2차 유효성 평가변수에 대한 분석은 현재 진행 중이다.
에자이는 일본, 미국, 유럽 및 중국 등 아시아 시장 허가 신청 관련 규제 당국과 논의를 진행할 예정이며, 오는 학회에서도 관련 내용을 소개할 계획이다.
한편 간암은 암으로 인한 사망 가운데 두 번째로 높은 비율을 차지하며 세계적으로 연간 약 70만명이 사망하는 암으로 대부분 중국과 같은 아시아 국가와 아프리카에서 발생한다. 간세포암은 원발성 간암의 85%~90%를 차지한다. 초기 단계의 간세포암은 수술, 고주파 열치료, 에탄올 주입술, 화학색전술 등 다양한 방법으로 치료가 가능하나 절제가 불가능한 간세포암종의 치료는 제한적이고 예후가 좋지 않아 의학적으로 아직 충족되지 못한 요구가 높다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
