CGP·MRD·MCED로 적용 범위 확대…극미량 암 신호 정확도 경쟁 본격화
캔서디텍트·캔서파인드 사례로 본 암 재발 추적부터 조기검진까지
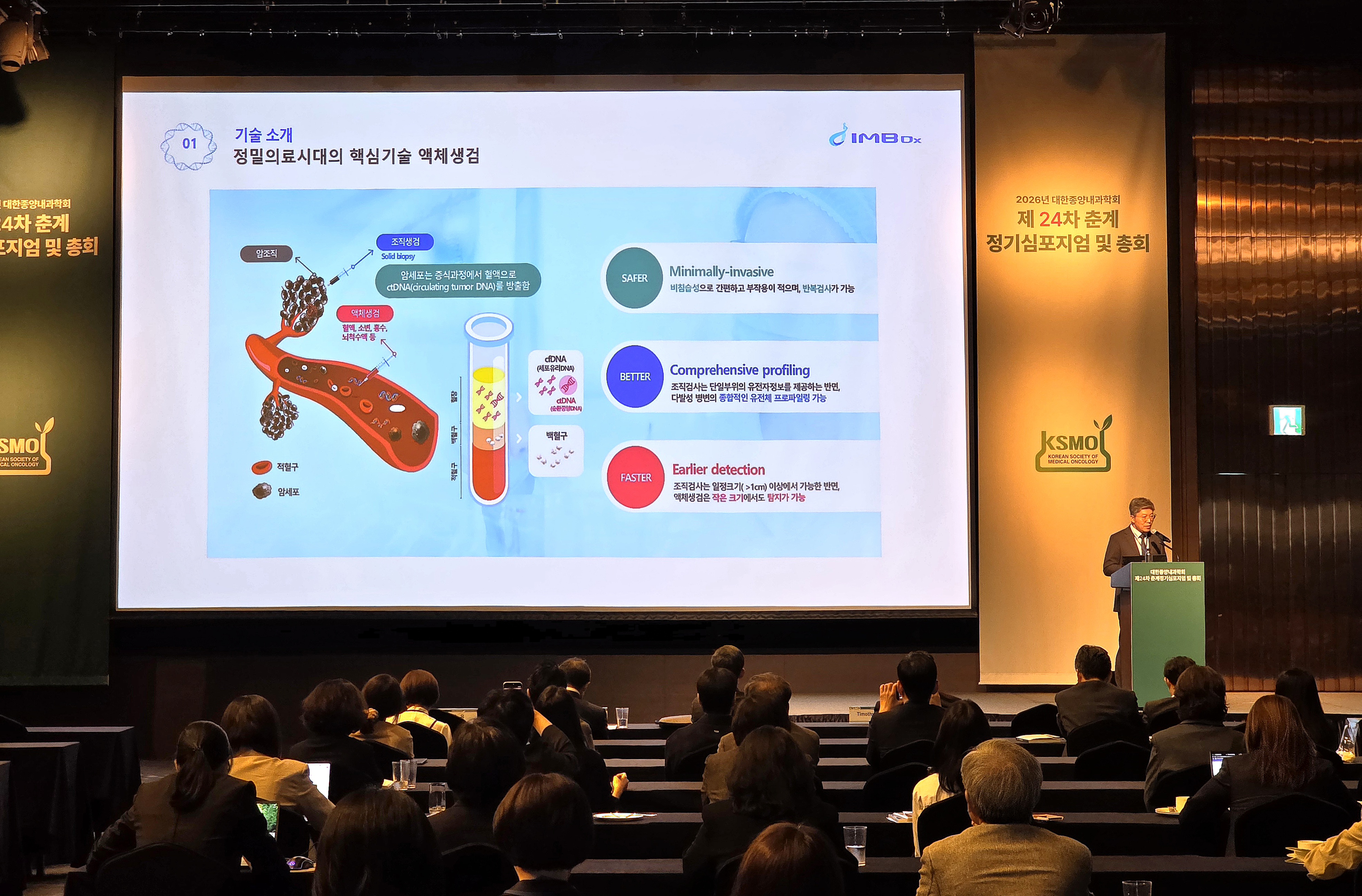

순환종양DNA(ctDNA) 기반 액체생검이 암 유전체 분석을 넘어 암 전주기 정밀의료 기술로 확장하고 있다. 진행암 치료 표적 탐색, 수술 후 미세잔존암(MRD) 추적, 다중암 조기검진(MCED)까지 적용 범위가 넓어지면서 혈액 기반 진단 기술의 임상적 역할도 커지고 있다.
대한종양내과학회(KSMO, 이사장 박준오)는 15일 서울 그랜드 인터컨티넨탈 서울 파르나스에서 ‘2026년 대한종양내과학회 제24차 춘계 정기심포지엄 및 총회’를 개최했다. 이날 행사에서는 종양학 발전에 기여한 연구자를 기리는 김노경상 시상이 진행됐다.
수상자인 김태유 서울대병원 혈액종양내과 교수(아이엠비디엑스 대표)는 ‘벤치에서 병상으로, 다시 스타트업으로: ctDNA 연구 여정과 앞으로 과제(From Bench to Bedside to Startup: The ctDNA Journey and What Lies Ahead)’를 주제로 발표했다.
그는 ctDNA 연구가 실험실 기반 연구를 넘어 실제 임상과 창업, 산업화로 이어진 흐름을 설명하며 액체생검 다음 확장 방향을 제시했다.
액체생검은 혈액 등 체액에 존재하는 암 유래 유전물질을 분석해 종양 유전적 특성과 질병 변화를 파악하는 검사다. 혈액 기반 액체생검은 ctDNA를 활용해 조직검사 없이 암 관련 변이를 확인하고, 치료 과정에서 종양 신호 변화를 반복적으로 추적할 수 있다.
김 교수는 “액체생검이 특정 시점에만 쓰이는 검사가 아니라 암 치료 전 과정을 연결하는 정밀의료 기술”이라고 강조했다. 그는 “액체생검 기반 CGP, MRD, MCED는 모두 같은 액체생검 기술을 기반으로 한다”면서 “이 세 가지 기술은 진행암부터 수술 후 재발 스크리닝까지 암의 전 주기를 커버할 수 있다”고 말했다. 이어 “혈액 기반 진단은 치료제 선택, 재발 모니터링, 조기검진으로 확장되며 전주기 정밀의료 기술로 발전하고 있다”고 덧붙였다.
액체생검, CGP·MRD·MCED로 확장
김 교수는 액체생검 활용 영역을 포괄적 유전체 프로파일링(CGP), 미세잔존암 탐지, 다중암 조기검진으로 정리했다.
액체생검 기반 CGP는 혈액 내 ctDNA를 분석해 암 관련 유전자 변이를 확인하는 방식이다. 이를 통해 표적치료제 선택에 필요한 유전체 정보를 제공할 수 있다. 조직검사가 어렵거나 반복 채취가 제한적인 환자에서는 치료 의사결정을 보완하는 수단이 된다.
MRD는 수술이나 국소치료 이후 남아 있을 수 있는 암 신호를 혈액에서 추적하는 기술이다. 김 교수는 MRD를 수술 후 재발 위험 평가와 치료 전략 조정에 활용할 수 있는 핵심 기술로 제시했다. 한 번의 양성·음성 판정보다 시간에 따른 ctDNA 농도 변화를 보는 정량 추적이 중요하다는 설명이다.
MCED는 조직 정보 없이 혈액에서 암 신호와 조직 기원, 즉 원발 부위를 예측하는 접근법이다. 발표에서는 DNA 메틸화, 프래그먼토믹스, 복제수 변이(CNV), 바이러스 DNA, 뉴클레오솜 풋프린트 등 여러 분자 특징을 인공지능 모델로 통합하는 방식이 소개됐다.
극미량 ctDNA 분석…종양분율·CHIP·오류 제어가 관건
액체생검 성패는 혈액에서 ctDNA를 검출하는 데서 끝나지 않는다. 핵심은 혈액 속 극미량 신호가 실제 암에서 유래한 것인지 구분하는 정확도다.
종양 크기가 작아질수록 혈장 내 ctDNA 비율은 급격히 낮아진다. 5cm 종양에서는 ctDNA 비율이 약 1% 수준으로 예측되지만, 1cm에서는 약 0.01%, 1mm에서는 약 0.0001% 수준까지 떨어질 수 있다. 조기암이나 수술 후 미세잔존암을 혈액에서 찾기 어려운 이유다.
이 때문에 액체생검 결과를 해석할 때는 ctDNA 종양분율(tumor fraction)을 함께 봐야 한다. ctDNA 종양분율이 1% 이상이면 조직검사와의 일치도가 높지만, 1% 미만에서는 추가 조직검사(reflex tissue biopsy)가 필요할 수 있다. 단순 양성·음성 여부만 보는 방식으로는 액체생검 결과를 충분히 해석하기 어렵다는 의미다.
CHIP도 정확도를 좌우하는 변수다. CHIP은 불확정 잠재력 클론성 조혈(clonal hematopoiesis of indeterminate potential)로, 나이가 들면서 조혈세포에서 생기는 체세포 변이다. 암 유래 ctDNA와 혼동될 수 있어 액체생검 위양성의 주요 원인으로 꼽힌다. 김 교수는 비암 대조군 cfDNA 변이의 81.6%, 암 환자 cfDNA 변이의 53.2%가 CHIP 특징을 보였다는 분석을 제시했다.
시퀀싱 오류 제어도 기술 경쟁력의 핵심이다. ctDNA는 신호 대비 잡음비가 낮다. 0.01% 이하 신호를 구분하려면 시퀀싱 과정에서 발생하는 오류를 줄이는 알고리즘이 필요하다. 김 교수는 UMI, DCS, SSCS 기반 합의 시퀀스를 활용한 HQS(high quality unique sequence) 생성 알고리즘을 통해 오류율을 0.00004%까지 낮췄다고 설명했다.
MRD는 정량 추적, MCED는 임상 검증이 핵심
MRD 영역 핵심은 정량 추적이다. 단일 시점에서 양성 또는 음성을 판정하는 데서 나아가, 시간에 따라 ctDNA 농도가 어떻게 변하는지를 보는 방식이다.
김 교수는 “MRD 검사는 한 번으로 끝나는 검사가 아니라 지속 추적이 중요하다”며 “재발 가능성을 영상검사보다 앞서 파악하고 대응할 수 있다는 점에서 정밀의료의 핵심 기술”이라고 말했다.
아이엠비디엑스 ‘캔서디텍트(CancerDetect)’는 조직 정보 기반(tissue-informed), 하이브리드 캡처 기반 개인 맞춤형 ctDNA 분석 기술이다. 환자의 FFPE 조직과 생식세포 DNA를 기반으로 전장엑솜염기서열분석(WES)을 수행하고, 환자별 변이를 선별해 맞춤형 패널을 만든 뒤 혈액에서 해당 변이를 추적한다.
캔서디텍트는 모니터링 변이 수를 늘려 검출한계(LOD)를 0.001%, 10ppm 수준까지 낮추는 전략을 제시했다. 많은 변이를 동시에 추적할수록 낮은 ctDNA 농도에서도 암 유래 신호를 포착할 가능성이 높아진다는 접근이다.
임상 검증도 병행되고 있다. CLAUDIA Colon Cancer 연구는 고위험 2기 또는 3기 대장암 환자를 대상으로 보조항암치료 후 MRD를 평가하는 플랫폼 연구다. 김 교수에 따르면 2026년 5월 기준 1200명 목표 중 970명(80.8%)이 스크리닝됐고, 수술 후 MRD 양성은 284명(29.3%)이었다.
MCED는 액체생검 조기검진 확장 가능성을 보여주는 영역이다. 김 교수는 cfDNA 기반 MCED로 임상 진단 약 3년 전 암 신호를 확인한 연구를 소개했다. 혈액에서 암 신호를 조기에 포착할 수 있다면, 액체생검은 치료제 선택과 재발 추적을 넘어 검진 영역까지 확장될 수 있다.
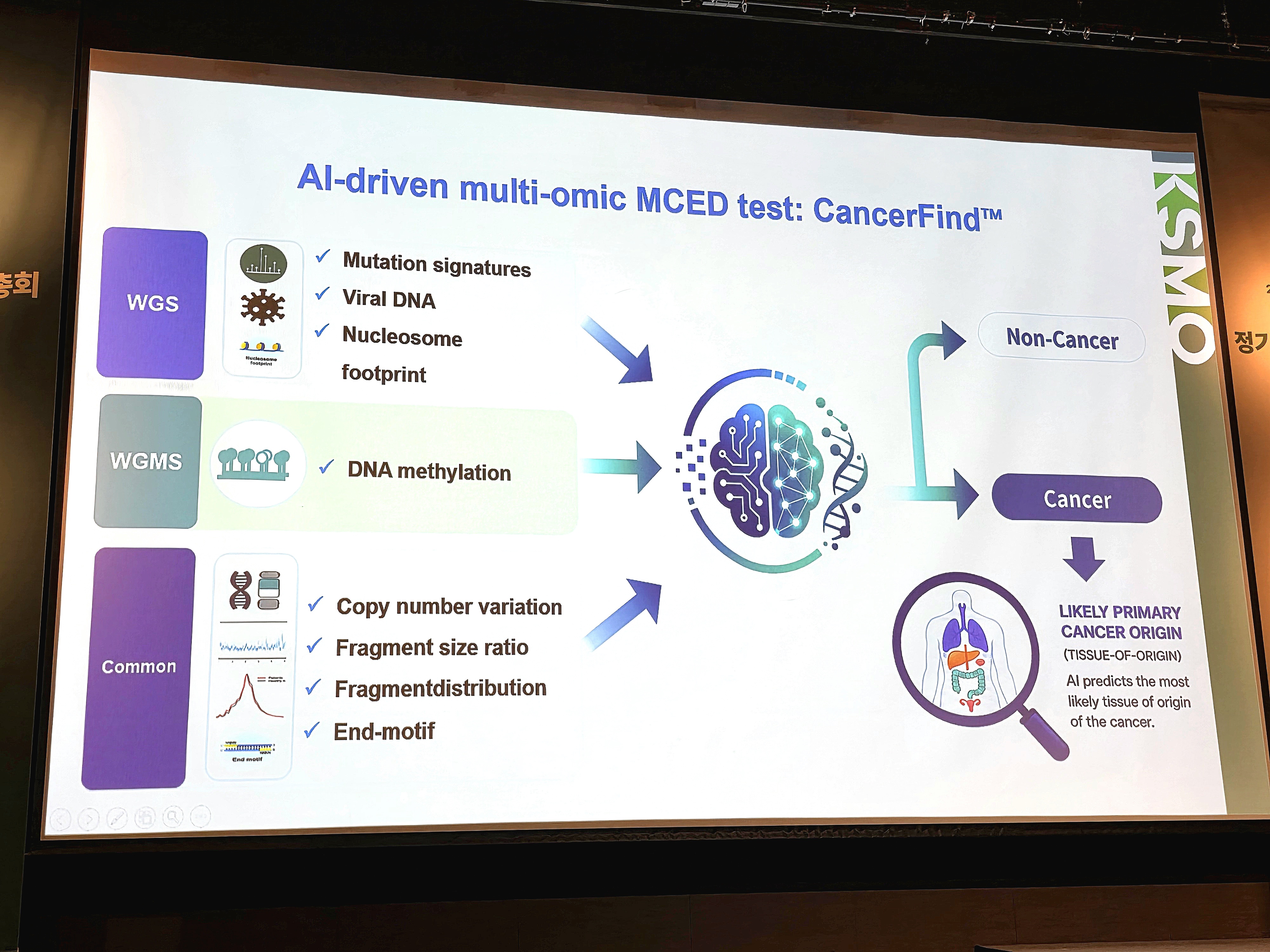
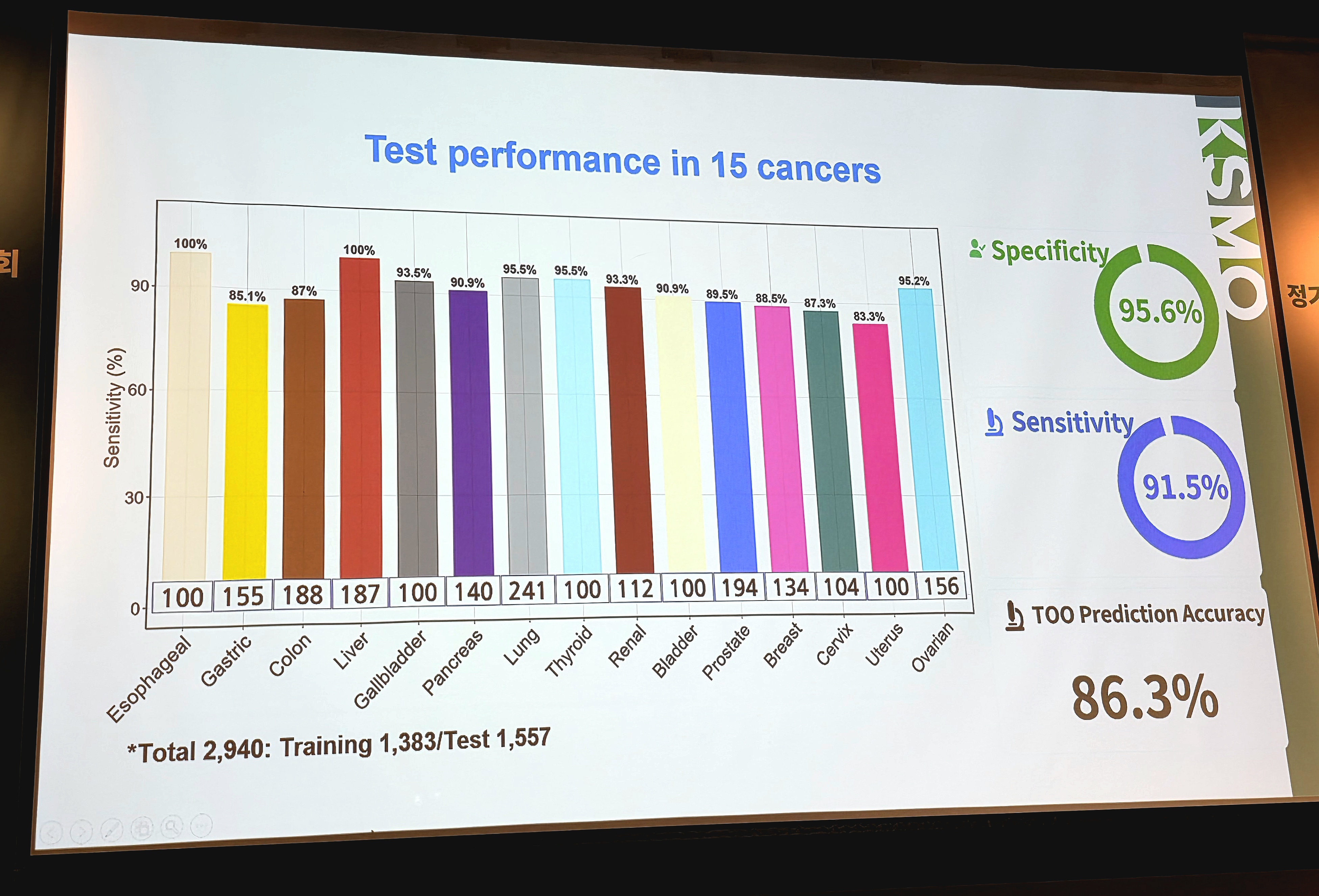
아이엠비디엑스는 AI 기반 멀티오믹스 MCED 검사인 ‘캔서파인드(CancerFind)’도 개발·고도화하고 있다. 캔서파인드는 DNA 메틸화, 변이 시그니처, 바이러스 DNA, 복제수 변이, 절편 크기 비율, 절편 분포, 말단 모티프 등을 통합해 암 여부와 원발 부위를 예측하는 방식이다. 김 교수는 15개 암종 데이터에서 민감도 91.5%, 특이도 95.6%, 원발 부위 예측 정확도 86.3%를 보였다고 밝혔다.
캔서파인드는 한국형 ARPA-H Cancer Detection Innovation project인 PRECISE 연구를 통해 건강인을 대상으로 전향적 평가가 추진된다. 연구 기간은 2026년 7월부터 2028년 6월까지이며, 3000명 등록을 목표로 한다.
김 교수는 “MRD와 MCED가 전혀 다른 기술이라고 보지는 않는다”며 “조직 정보를 이용하느냐, 이용하지 않느냐에 따라 정확성 차이가 있을 뿐”이라고 말했다. 이어 “궁극적으로는 두 기술을 합쳐 조직 없이도 현재 MRD 수준의 성능을 구현하는 것이 액체생검 기술 개발의 마지막 단계가 될 것”이라고 내다봤다.

| 인기기사 | 더보기 + |
-
1 프로티나, 미국 IDT와 MOU 체결... 차세대 항체 치료제 개발 가속 -
2 '조 단위' R&D 시대 명암… 제약업계, 속도와 실속 사이 답 찾다 -
3 약가유연계약 제도화…신약 약가협상 방식 바뀐다 -
4 ‘살 빼는 약’ 넘어 ‘만성질환 플랫폼’으로…위고비 새 데이터 대거 공개 -
5 ‘새 시대’ 꺼낸 다케다…대규모 감원과 신약 출시 전략 병행 -
6 에이비엘바이오, 그랩바디-B 'RNA 치료제' 뇌 전달 허들 넘나 -
7 약가유연계약제 6월 전면 시행… 제약업계 글로벌 진출 든든한 방어막 구축 -
8 제네릭 약가 45% 시대 개막… 정부의 보상 핀셋 '수급안정·원료자립' 향했다 -
9 ‘위고비’ 정제 체중 21.6% 감소‧운동성 2배 향상 -
10 알테오젠, 아일리아 바이오시밀러 ‘아이젠피주’ 품목허가 취득
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 권혁진 기자 hjkwon@yakup.com
- 입력 2026.05.15 14:29 수정 2026.05.15 14:33


순환종양DNA(ctDNA) 기반 액체생검이 암 유전체 분석을 넘어 암 전주기 정밀의료 기술로 확장하고 있다. 진행암 치료 표적 탐색, 수술 후 미세잔존암(MRD) 추적, 다중암 조기검진(MCED)까지 적용 범위가 넓어지면서 혈액 기반 진단 기술의 임상적 역할도 커지고 있다.
대한종양내과학회(KSMO, 이사장 박준오)는 15일 서울 그랜드 인터컨티넨탈 서울 파르나스에서 ‘2026년 대한종양내과학회 제24차 춘계 정기심포지엄 및 총회’를 개최했다. 이날 행사에서는 종양학 발전에 기여한 연구자를 기리는 김노경상 시상이 진행됐다.
수상자인 김태유 서울대병원 혈액종양내과 교수(아이엠비디엑스 대표)는 ‘벤치에서 병상으로, 다시 스타트업으로: ctDNA 연구 여정과 앞으로 과제(From Bench to Bedside to Startup: The ctDNA Journey and What Lies Ahead)’를 주제로 발표했다.
그는 ctDNA 연구가 실험실 기반 연구를 넘어 실제 임상과 창업, 산업화로 이어진 흐름을 설명하며 액체생검 다음 확장 방향을 제시했다.
액체생검은 혈액 등 체액에 존재하는 암 유래 유전물질을 분석해 종양 유전적 특성과 질병 변화를 파악하는 검사다. 혈액 기반 액체생검은 ctDNA를 활용해 조직검사 없이 암 관련 변이를 확인하고, 치료 과정에서 종양 신호 변화를 반복적으로 추적할 수 있다.
김 교수는 “액체생검이 특정 시점에만 쓰이는 검사가 아니라 암 치료 전 과정을 연결하는 정밀의료 기술”이라고 강조했다. 그는 “액체생검 기반 CGP, MRD, MCED는 모두 같은 액체생검 기술을 기반으로 한다”면서 “이 세 가지 기술은 진행암부터 수술 후 재발 스크리닝까지 암의 전 주기를 커버할 수 있다”고 말했다. 이어 “혈액 기반 진단은 치료제 선택, 재발 모니터링, 조기검진으로 확장되며 전주기 정밀의료 기술로 발전하고 있다”고 덧붙였다.
액체생검, CGP·MRD·MCED로 확장
김 교수는 액체생검 활용 영역을 포괄적 유전체 프로파일링(CGP), 미세잔존암 탐지, 다중암 조기검진으로 정리했다.
액체생검 기반 CGP는 혈액 내 ctDNA를 분석해 암 관련 유전자 변이를 확인하는 방식이다. 이를 통해 표적치료제 선택에 필요한 유전체 정보를 제공할 수 있다. 조직검사가 어렵거나 반복 채취가 제한적인 환자에서는 치료 의사결정을 보완하는 수단이 된다.
MRD는 수술이나 국소치료 이후 남아 있을 수 있는 암 신호를 혈액에서 추적하는 기술이다. 김 교수는 MRD를 수술 후 재발 위험 평가와 치료 전략 조정에 활용할 수 있는 핵심 기술로 제시했다. 한 번의 양성·음성 판정보다 시간에 따른 ctDNA 농도 변화를 보는 정량 추적이 중요하다는 설명이다.
MCED는 조직 정보 없이 혈액에서 암 신호와 조직 기원, 즉 원발 부위를 예측하는 접근법이다. 발표에서는 DNA 메틸화, 프래그먼토믹스, 복제수 변이(CNV), 바이러스 DNA, 뉴클레오솜 풋프린트 등 여러 분자 특징을 인공지능 모델로 통합하는 방식이 소개됐다.
극미량 ctDNA 분석…종양분율·CHIP·오류 제어가 관건
액체생검 성패는 혈액에서 ctDNA를 검출하는 데서 끝나지 않는다. 핵심은 혈액 속 극미량 신호가 실제 암에서 유래한 것인지 구분하는 정확도다.
종양 크기가 작아질수록 혈장 내 ctDNA 비율은 급격히 낮아진다. 5cm 종양에서는 ctDNA 비율이 약 1% 수준으로 예측되지만, 1cm에서는 약 0.01%, 1mm에서는 약 0.0001% 수준까지 떨어질 수 있다. 조기암이나 수술 후 미세잔존암을 혈액에서 찾기 어려운 이유다.
이 때문에 액체생검 결과를 해석할 때는 ctDNA 종양분율(tumor fraction)을 함께 봐야 한다. ctDNA 종양분율이 1% 이상이면 조직검사와의 일치도가 높지만, 1% 미만에서는 추가 조직검사(reflex tissue biopsy)가 필요할 수 있다. 단순 양성·음성 여부만 보는 방식으로는 액체생검 결과를 충분히 해석하기 어렵다는 의미다.
CHIP도 정확도를 좌우하는 변수다. CHIP은 불확정 잠재력 클론성 조혈(clonal hematopoiesis of indeterminate potential)로, 나이가 들면서 조혈세포에서 생기는 체세포 변이다. 암 유래 ctDNA와 혼동될 수 있어 액체생검 위양성의 주요 원인으로 꼽힌다. 김 교수는 비암 대조군 cfDNA 변이의 81.6%, 암 환자 cfDNA 변이의 53.2%가 CHIP 특징을 보였다는 분석을 제시했다.
시퀀싱 오류 제어도 기술 경쟁력의 핵심이다. ctDNA는 신호 대비 잡음비가 낮다. 0.01% 이하 신호를 구분하려면 시퀀싱 과정에서 발생하는 오류를 줄이는 알고리즘이 필요하다. 김 교수는 UMI, DCS, SSCS 기반 합의 시퀀스를 활용한 HQS(high quality unique sequence) 생성 알고리즘을 통해 오류율을 0.00004%까지 낮췄다고 설명했다.
MRD는 정량 추적, MCED는 임상 검증이 핵심
MRD 영역 핵심은 정량 추적이다. 단일 시점에서 양성 또는 음성을 판정하는 데서 나아가, 시간에 따라 ctDNA 농도가 어떻게 변하는지를 보는 방식이다.
김 교수는 “MRD 검사는 한 번으로 끝나는 검사가 아니라 지속 추적이 중요하다”며 “재발 가능성을 영상검사보다 앞서 파악하고 대응할 수 있다는 점에서 정밀의료의 핵심 기술”이라고 말했다.
아이엠비디엑스 ‘캔서디텍트(CancerDetect)’는 조직 정보 기반(tissue-informed), 하이브리드 캡처 기반 개인 맞춤형 ctDNA 분석 기술이다. 환자의 FFPE 조직과 생식세포 DNA를 기반으로 전장엑솜염기서열분석(WES)을 수행하고, 환자별 변이를 선별해 맞춤형 패널을 만든 뒤 혈액에서 해당 변이를 추적한다.
캔서디텍트는 모니터링 변이 수를 늘려 검출한계(LOD)를 0.001%, 10ppm 수준까지 낮추는 전략을 제시했다. 많은 변이를 동시에 추적할수록 낮은 ctDNA 농도에서도 암 유래 신호를 포착할 가능성이 높아진다는 접근이다.
임상 검증도 병행되고 있다. CLAUDIA Colon Cancer 연구는 고위험 2기 또는 3기 대장암 환자를 대상으로 보조항암치료 후 MRD를 평가하는 플랫폼 연구다. 김 교수에 따르면 2026년 5월 기준 1200명 목표 중 970명(80.8%)이 스크리닝됐고, 수술 후 MRD 양성은 284명(29.3%)이었다.
MCED는 액체생검 조기검진 확장 가능성을 보여주는 영역이다. 김 교수는 cfDNA 기반 MCED로 임상 진단 약 3년 전 암 신호를 확인한 연구를 소개했다. 혈액에서 암 신호를 조기에 포착할 수 있다면, 액체생검은 치료제 선택과 재발 추적을 넘어 검진 영역까지 확장될 수 있다.
아이엠비디엑스는 AI 기반 멀티오믹스 MCED 검사인 ‘캔서파인드(CancerFind)’도 개발·고도화하고 있다. 캔서파인드는 DNA 메틸화, 변이 시그니처, 바이러스 DNA, 복제수 변이, 절편 크기 비율, 절편 분포, 말단 모티프 등을 통합해 암 여부와 원발 부위를 예측하는 방식이다. 김 교수는 15개 암종 데이터에서 민감도 91.5%, 특이도 95.6%, 원발 부위 예측 정확도 86.3%를 보였다고 밝혔다.
캔서파인드는 한국형 ARPA-H Cancer Detection Innovation project인 PRECISE 연구를 통해 건강인을 대상으로 전향적 평가가 추진된다. 연구 기간은 2026년 7월부터 2028년 6월까지이며, 3000명 등록을 목표로 한다.
김 교수는 “MRD와 MCED가 전혀 다른 기술이라고 보지는 않는다”며 “조직 정보를 이용하느냐, 이용하지 않느냐에 따라 정확성 차이가 있을 뿐”이라고 말했다. 이어 “궁극적으로는 두 기술을 합쳐 조직 없이도 현재 MRD 수준의 성능을 구현하는 것이 액체생검 기술 개발의 마지막 단계가 될 것”이라고 내다봤다.



무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
