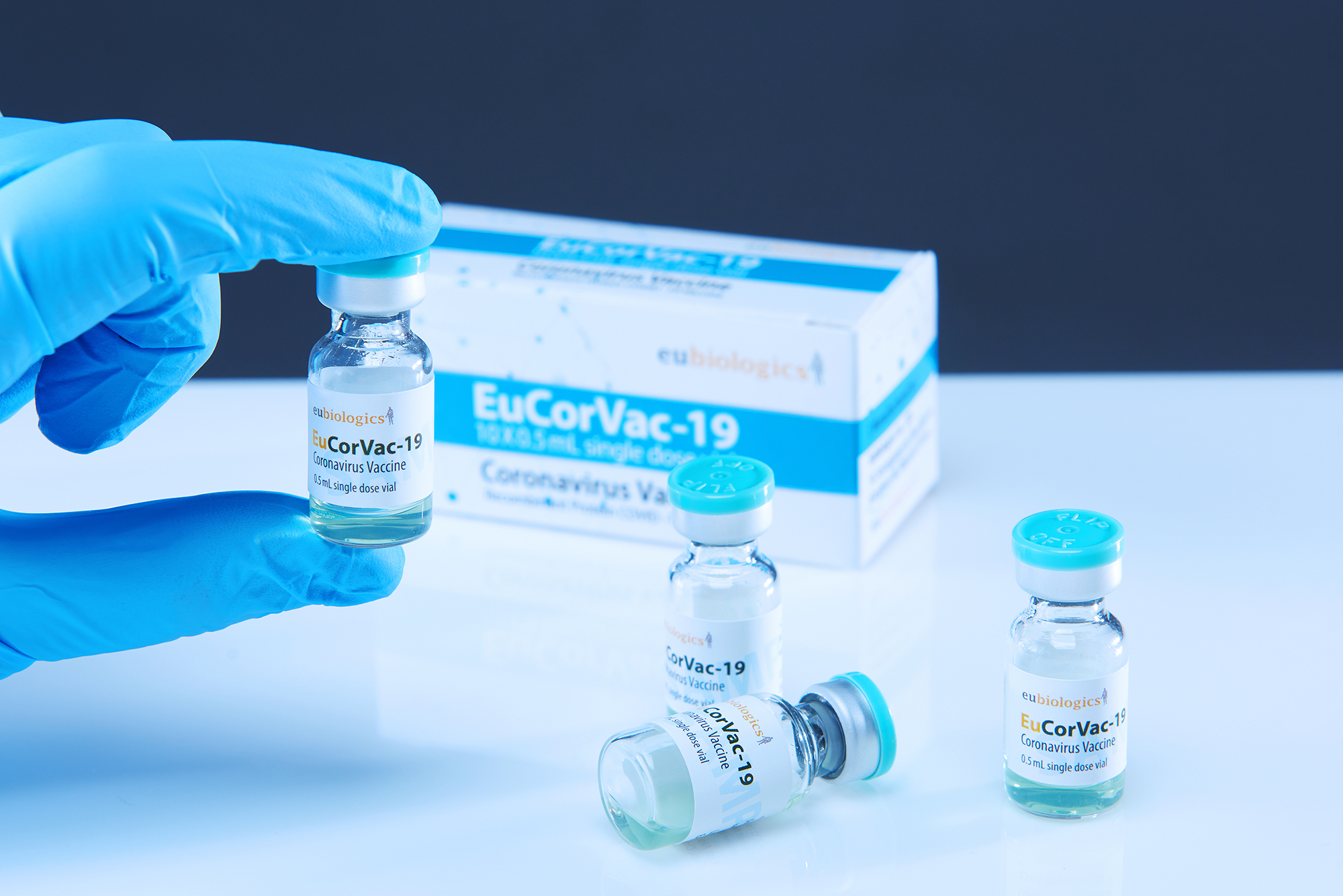
유바이오로직스는 ‘유코백-19’ 임상 3상이 이달 중 최종 2차 접종자의 1년간 추적관찰이 종료된다고 18일 밝혔다.
유바이오로직스가 개발하고 있는 유코백-19 임상 3상은 필리핀과 콩고민주공화국에서 각각 대조백신과의 비교 임상으로 진행됐다. 필리핀 임상의 경우 지난해 6월 2회 접종에 따른 안전성과 면역원성 중간결과를 발표한 바 있다.
이에 따라 유바이오로직스는 임상 3상에서의 안전성과 면역원성에 대한 CSR(임상시험 결과보고서)을 올 2분기 말 받을 것으로 예상된다. 중간 결과 발표 이후 임상 참여자에 대한 관찰에서 특이 사항이 보고된 바 없었기에 최종적으로 3상 임상은 성공적으로 종료될 것으로 기대된다는 게 회사 입장이다.
한편 유코백-19 국내 비교 임상은 지난 2022년 1월 승인 후, 2년간 국내 임상참여자 확보 및 대조백신 확보할 수 없어, 금회 조기종료됐다.
유바이오로직스의 유코백-19 개발 백신은 기존 우한주 모체바이러스에 대한 임상이었지만, 동일 플랫폼으로 개발하고 있는 추가접종용 변이주 백신(현재 XBB1.5)의 임상 및 허가자료에 인용될 수 있다. 국내에서 허가 받은 해외 기업의 변이주 백신들과 면역원성 비교 임상을 토대로 국내 허가를 신청할 수 있을 것으로 기대된다.
유바이오로직스는 현재 미국 FDA 및 국내 식품의약품안전처의 COVID-19 백신 개발 가이드라인에 따라 XBB1.5 대응 백신을 개발하고 있다. 유바이오로직스는 상반기 중 국내 임상을 신청할 예정이다. 또한 계절성 호흡기바이러스가 감염병으로 토착화되어 감에 따라 인플루엔자 백신과 혼합백신 개발에 대해서도 국내외 업체와 긴밀한 협력을 진행 중이다.
유바이오로직스 관계자는 “자체 플랫폼 기술을 바탕으로 코로나-19 백신 임상 3상을 완료할 수 있게 됐다"면서 “동일 플랫폼을 이용하여 호흡기세포융합바이러스 백신(RSV)의 국내 1상 IND 승인 및 대상포진 백신(HZV)의 임상신청으로 이어질 수 있어서 기쁘다”고 말했다.
이어 그는 “정부 지원에 힘입어 이러한 신종 바이러스에 의한 위기대응 백신개발의 플랫폼을 최종적으로 확보할 수 있게 된 것”이라며 "유바이오로직스는 아직도 끝나지 않은 코로나-19 변이주와의 싸움에 필요한 변이주 대응백신 및 혼합백신의 개발을 지속해 국내 백신 자급에 일조하겠다”고 덧붙였다.
| 인기기사 | 더보기 + |
-
1 [AACR] 에이비엘바이오 승부수 이중항체 ADC ‘ABL209’ 첫 청신호 켜졌다 -
2 디앤디파마텍 MASH 치료제 임상2상 48주 데이터베이스 락 완료 -
3 상장 제약·바이오 2025년 평균 부채비율 코스피 88.13%·코스닥 64.01% -
4 큐리옥스,'Pluto Code' 전사적 도입 포괄적 소프트웨어 라이선스 계약 체결 -
5 네이처셀,조인트스템 FDA 가속승인 본격화..브리핑 패키지 제출 -
6 상장 제약·바이오 2025년 평균 유보율 코스피 2142.15%·코스닥 2583.86% -
7 유통업계, 대웅 본사 집결…"거점도매 철회" 결사항전 -
8 코아스템켐온, 15억 규모 범부처재생의료 사업 선정…CRISPR 'ALS 세포·유전자치료제' 개발 -
9 2025 빅파마 TOP5…순위는 유지, 성장 동력은 교체 ① -
10 페니트리움바이오,표적항암제 내성 해결 'Dual-agnostic Basket Trial' 추진
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 권혁진 기자 hjkwon@yakup.com
- 입력 2024.01.18 11:23

유바이오로직스는 ‘유코백-19’ 임상 3상이 이달 중 최종 2차 접종자의 1년간 추적관찰이 종료된다고 18일 밝혔다.
유바이오로직스가 개발하고 있는 유코백-19 임상 3상은 필리핀과 콩고민주공화국에서 각각 대조백신과의 비교 임상으로 진행됐다. 필리핀 임상의 경우 지난해 6월 2회 접종에 따른 안전성과 면역원성 중간결과를 발표한 바 있다.
이에 따라 유바이오로직스는 임상 3상에서의 안전성과 면역원성에 대한 CSR(임상시험 결과보고서)을 올 2분기 말 받을 것으로 예상된다. 중간 결과 발표 이후 임상 참여자에 대한 관찰에서 특이 사항이 보고된 바 없었기에 최종적으로 3상 임상은 성공적으로 종료될 것으로 기대된다는 게 회사 입장이다.
한편 유코백-19 국내 비교 임상은 지난 2022년 1월 승인 후, 2년간 국내 임상참여자 확보 및 대조백신 확보할 수 없어, 금회 조기종료됐다.
유바이오로직스의 유코백-19 개발 백신은 기존 우한주 모체바이러스에 대한 임상이었지만, 동일 플랫폼으로 개발하고 있는 추가접종용 변이주 백신(현재 XBB1.5)의 임상 및 허가자료에 인용될 수 있다. 국내에서 허가 받은 해외 기업의 변이주 백신들과 면역원성 비교 임상을 토대로 국내 허가를 신청할 수 있을 것으로 기대된다.
유바이오로직스는 현재 미국 FDA 및 국내 식품의약품안전처의 COVID-19 백신 개발 가이드라인에 따라 XBB1.5 대응 백신을 개발하고 있다. 유바이오로직스는 상반기 중 국내 임상을 신청할 예정이다. 또한 계절성 호흡기바이러스가 감염병으로 토착화되어 감에 따라 인플루엔자 백신과 혼합백신 개발에 대해서도 국내외 업체와 긴밀한 협력을 진행 중이다.
유바이오로직스 관계자는 “자체 플랫폼 기술을 바탕으로 코로나-19 백신 임상 3상을 완료할 수 있게 됐다"면서 “동일 플랫폼을 이용하여 호흡기세포융합바이러스 백신(RSV)의 국내 1상 IND 승인 및 대상포진 백신(HZV)의 임상신청으로 이어질 수 있어서 기쁘다”고 말했다.
이어 그는 “정부 지원에 힘입어 이러한 신종 바이러스에 의한 위기대응 백신개발의 플랫폼을 최종적으로 확보할 수 있게 된 것”이라며 "유바이오로직스는 아직도 끝나지 않은 코로나-19 변이주와의 싸움에 필요한 변이주 대응백신 및 혼합백신의 개발을 지속해 국내 백신 자급에 일조하겠다”고 덧붙였다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
