HER2-low·ultra-low까지 확장…ADC 약물 전달 플랫폼 진화 기대
차세대 항암 플랫폼 이중특이항체 부상, 항체 기반 치료 경쟁 확대

“항암제 중에서 여전히, 그리고 당분간 대세는 ADC가 될 것입니다. 그다음 세대를 이끌 플랫폼으로는 이중특이항체가 빠르게 부상하고 있습니다.”
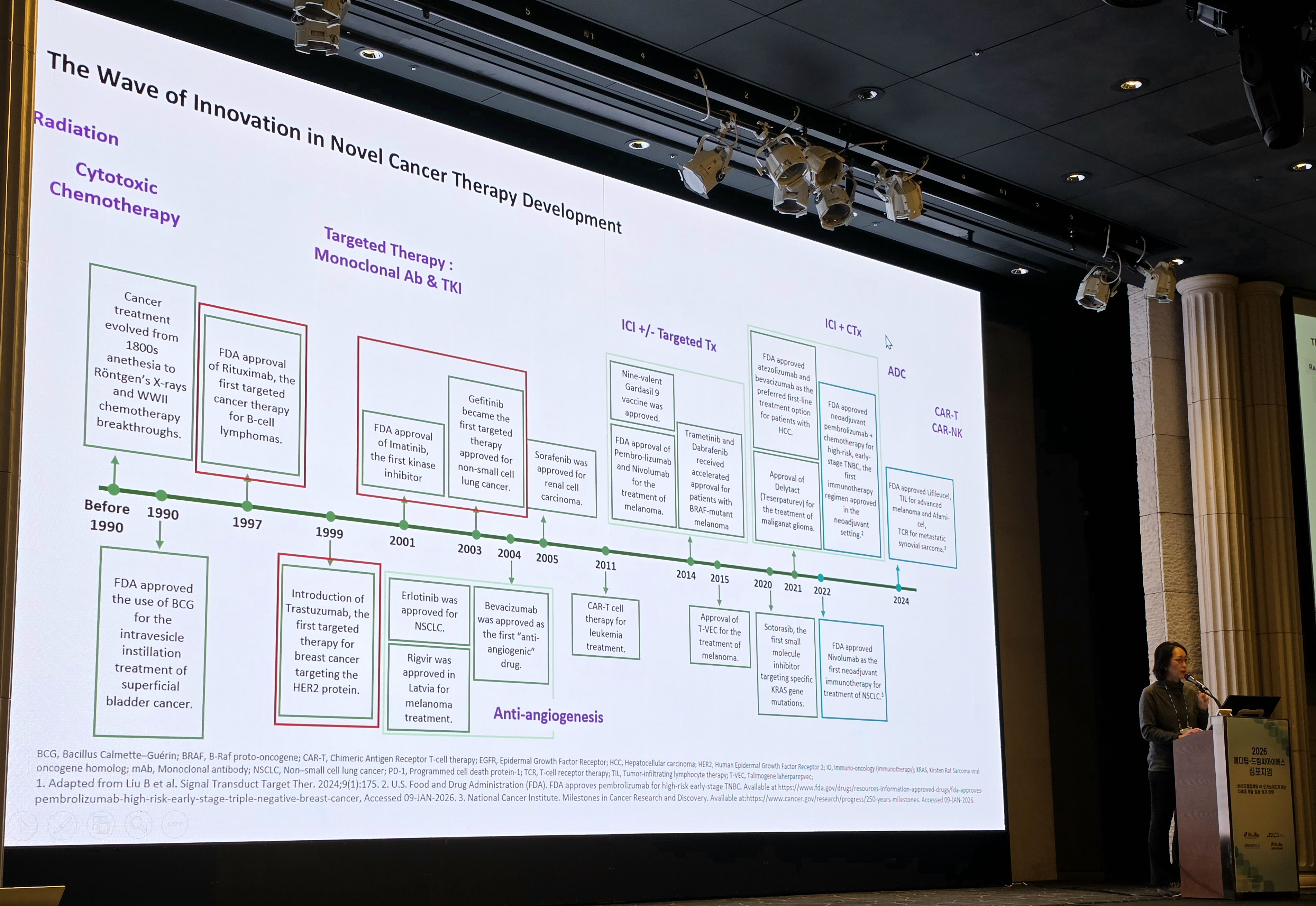
고려대학교 안암병원 종양내과 이수현 교수는 최근 서울 양재 엘타워에서 열린 ‘2026 메디팁-드림CIS 심포지엄’에서 ‘최근 종양학 신약 개발 및 임상시험 동향(Recent Updates of Oncology Drug Development & Clinical Trials)’을 주제로 발표하며 이같이 말했다.
이 교수는 최근 항암제 핵심으로 항체약물접합체(ADC, Antibody Drug Conjugate)와 이중특이항체(BsAb, Bispecific Antibody)를 꼽았다. 그는 ADC가 이미 여러 암종에서 임상적 유효성을 입증하며, 사실상 차세대 표준 치료 옵션으로 자리 잡고 있다고 평가했다.
또한 이중특이항체는 면역관문억제제 이후 항암 치료 패러다임을 확장할 수 있는 새로운 플랫폼으로 빠르게 부상하고 있다는 점에 주목할 필요가 있다고 강조했다.
이 교수는 “결국 항암제 혁신의 핵심은 새로운 타깃을 찾는 것보다, 어떤 방식으로 약물을 전달하고 면역 반응을 조절하느냐에 달려 있다”라고 말했다.
ADC, 임상 성과로 항암제 대세 자리
현재 항암제 가운데 가장 뚜렷한 임상 성과를 보이고 있는 분야는 ADC다. ADC는 항체가 암세포 표적에 결합한 뒤 세포 내부로 들어가 강력한 세포독성 약물을 전달하는 구조의 치료제다. 항체의 표적 선택성과 화학요법의 세포독성을 결합한 형태로, 일종의 표적화된 화학요법(targeted chemotherapy)으로 이해할 수 있다.
ADC 분야에서 대표적인 사례는 다이이찌산쿄와 아스트라제네카가 공동 개발한 HER2 표적 ADC ‘트라스투주맙 데룩스테칸(T-DXd, 제품명 엔허투)’다.
DESTINY-Breast03 임상시험 최종 분석 결과, T-DXd는 로슈가 개발한 HER2 ADC ‘트라스투주맙 엠탄신(T-DM1, 제품명 캐싸일라)’ 대비 무진행생존기간(PFS)에서 29.0개월 대 7.8개월을 기록했다. 전체 생존기간(OS)은 56.4개월 대 42.7개월로 약 13.7개월 연장됐다. 5년 전체 생존율도 48.1% 대 36.9%로 약 11.2%포인트 차이를 보이며 우위를 확인했다.
ADC 적용 범위가 HER2 고발현 환자에서 저발현자까지 확장되고 있다. DESTINY-Breast04 연구에서는 HER2 저발현(low) 환자군에서도 의미 있는 치료 효과가 확인됐다. 호르몬수용체 양성(HR+) HER2 저발현 환자군에서 T-DXd는 무진행생존기간 10.1개월, 전체 생존기간 23.9개월을 기록, 기존 화학요법 대비 생존기간을 유의하게 연장했다. 전체 환자 기준으로도 PFS 9.9개월, OS 23.4개월이 보고됐다.
이 교수는 “HER2 발현이 낮은 환자에게서도 효과가 나타난다는 점은 ADC의 작용 기전에 대한 기존 인식을 바꾸는 결과”라며 “ADC가 단순한 표적치료제를 넘어 새로운 약물 전달 플랫폼으로 발전하고 있다는 점을 보여준다”고 말했다.
표적 발현만으로 설명 어려운 ADC 효과
ADC 임상 결과에서 주목되는 점은 표적 단백질 발현 수준만으로 치료 효과를 설명하기 어렵다는 점이다. T-DXd의 DAISY 임상 연구에서는 HER2 고발현 환자에서 객관적 반응률(ORR) 70.6%, HER2 저발현 환자에서는 37.5%가 확인됐다.
흥미로운 점은 HER2 발현이 거의 없는 환자에게서도 29.7%의 반응률이 관찰됐다는 사실이다. 연구자들은 이러한 결과가 ADC에서 나타나는 바이스탠더 효과(bystander effect) 등 복합적인 약물 전달 기전과 관련될 가능성을 제시하고 있다.
ADC는 암세포 내부에서 페이로드(payload)가 방출된 뒤 주변 세포로 확산될 수 있다. 이 과정에서 표적 발현이 낮은 종양 세포도 영향을 받을 수 있다. 이 교수는 “이러한 특성은 ADC가 단순한 표적치료제를 넘어 새로운 형태의 약물 전달 플랫폼으로 작동할 수 있음을 보여준다”고 말했다.
ADC 내성 문제와 바이오마커 필요성
ADC가 빠르게 확산되면서 새로운 과제도 떠오르고 있다. 대표적인 문제는 내성(resistance)이다. △표적 항원 발현 감소 △ADC 세포 내 흡수 및 엔도좀·리소좀 처리 과정 변화 △페이로드 약물에 대한 세포 내 저항성 △ATP- cassette(ABC) transporter 활성 증가에 따른 약물 유출 증가 등이 문제로 지목되고 있다.
이 때문에 향후 ADC 개발에서는 치료 반응을 예측할 수 있는 바이오마커 개발이 중요한 과제가 될 전망이다. 현재 연구 단계에서 제시되는 후보 지표로는 TOP1 변이, TACSTD2/TROP2 관련 변이, Cathepsin L(CTSL), p95HER2 등이 있다. 해당 지표는 아직 탐색적 연구 단계에 머물러 있으며, 임상에서 확립된 동반진단 바이오마커는 아니다.
전문가들은 ADC 치료 전략에서도 환자 선별(patient selection)과 치료 순서(sequence) 결정이 더 중요해질 것으로 보고 있다.
이중특이항체, 차세대 플랫폼으로 부상
ADC가 현재 항암제 시장을 주도하는 플랫폼이라면, 이중특이항체는 다음 세대를 준비하는 기술로 평가된다. 이중특이항체는 두 개의 서로 다른 항원을 동시에 인식하도록 설계된 항체다.
대표적인 접근법 중 하나는 T세포와 종양세포를 직접 연결하는 T-cell 결합(engager) 구조다. CD3와 종양 항원을 동시에 결합해 T세포가 암세포를 직접 공격하도록 유도하는 방식이다. DLL3와 CD3를 동시에 표적하는 이중특이항체 암젠의 ‘탈라타맙(tarlatamab)’이 대표 사례다.
탈라타맙은 재발성 소세포폐암 환자를 대상으로 한 임상 연구에서 전체 생존기간 약 13.6개월을 기록했다. 이는 같은 연구에서 보고된 화학요법 대조군 약 8.3개월 대비 생존기간이 연장된 결과로 평가된다.
또 다른 접근은 면역관문을 동시에 차단하는 전략이다. PD-1과 TIGIT을 동시에 표적하는 이중특이항체 아스트라제네카의 '릴베고스토미그(rilvegostomig)'는 비소세포폐암 초기 임상에서 면역관문억제제 치료 경험이 없는 전이성 비소세포폐암 환자를 대상으로 평가했다.
그 결과, PD-L1 발현 1~49% 환자군에서는 객관적 반응률 약 29%, PD-L1 발현 50% 이상 환자군에서는 61.8%의 반응률이 보고됐다. 업계에서는 이러한 결과가 차세대 면역항암 전략의 가능성을 보여주는 신호로 해석하고 있다.
차세대 ADC 기술 경쟁 시작
ADC 플랫폼 자체도 빠르게 발전하고 있다. 최근 연구에서는 이중 페이로드 ADC(dual-payload ADC), 이중특이 ADC(bispecific ADC), 면역 자극형 페이로드(immunostimulatory payload) 등 다양한 설계 전략이 시도되고 있다.
이 교수는 “최근 기존 ADC에서 나타나는 내성 문제를 극복하기 위한 연구가 활발히 진행되고 있으며, 향후 기술 경쟁의 핵심은 페이로드 종류와 링커 기술, 항체 설계가 될 것”이라면서 “면역 반응을 자극하는 페이로드가 개발되면, ADC는 단순한 세포독성 약물이 아니라 면역항암 효과까지 동시에 유도하는 플랫폼으로 확장될 수 있다”라고 말했다.
이어 그는 “HER2 발현이 매우 낮은 HER2 초저발현(ultra-low) 환자군에서도 ADC 치료 가능성이 논의되고 있는 것도 중요한 사안"이라면서 "ADC는 특정 표적 발현 여부를 넘어서는 새로운 약물 전달 플랫폼으로 진화하고 있다”고 설명했다.
이 교수는 “ADC는 이미 화학요법 대비 일관된 생존 개선 효과를 보여주며 항암 치료의 핵심 플랫폼으로 자리 잡았다”며 “향후 항암제 개발 경쟁은 ADC와 이중특이항체 같은 항체 기반 모달리티를 중심으로 전개될 가능성이 높다”고 덧붙였다.


- 권혁진 기자 hjkwon@yakup.com
- 입력 2026.03.16 06:00 수정 2026.03.16 06:01


“항암제 중에서 여전히, 그리고 당분간 대세는 ADC가 될 것입니다. 그다음 세대를 이끌 플랫폼으로는 이중특이항체가 빠르게 부상하고 있습니다.”
고려대학교 안암병원 종양내과 이수현 교수는 최근 서울 양재 엘타워에서 열린 ‘2026 메디팁-드림CIS 심포지엄’에서 ‘최근 종양학 신약 개발 및 임상시험 동향(Recent Updates of Oncology Drug Development & Clinical Trials)’을 주제로 발표하며 이같이 말했다.
이 교수는 최근 항암제 핵심으로 항체약물접합체(ADC, Antibody Drug Conjugate)와 이중특이항체(BsAb, Bispecific Antibody)를 꼽았다. 그는 ADC가 이미 여러 암종에서 임상적 유효성을 입증하며, 사실상 차세대 표준 치료 옵션으로 자리 잡고 있다고 평가했다.
또한 이중특이항체는 면역관문억제제 이후 항암 치료 패러다임을 확장할 수 있는 새로운 플랫폼으로 빠르게 부상하고 있다는 점에 주목할 필요가 있다고 강조했다.
이 교수는 “결국 항암제 혁신의 핵심은 새로운 타깃을 찾는 것보다, 어떤 방식으로 약물을 전달하고 면역 반응을 조절하느냐에 달려 있다”라고 말했다.
ADC, 임상 성과로 항암제 대세 자리
현재 항암제 가운데 가장 뚜렷한 임상 성과를 보이고 있는 분야는 ADC다. ADC는 항체가 암세포 표적에 결합한 뒤 세포 내부로 들어가 강력한 세포독성 약물을 전달하는 구조의 치료제다. 항체의 표적 선택성과 화학요법의 세포독성을 결합한 형태로, 일종의 표적화된 화학요법(targeted chemotherapy)으로 이해할 수 있다.
ADC 분야에서 대표적인 사례는 다이이찌산쿄와 아스트라제네카가 공동 개발한 HER2 표적 ADC ‘트라스투주맙 데룩스테칸(T-DXd, 제품명 엔허투)’다.
DESTINY-Breast03 임상시험 최종 분석 결과, T-DXd는 로슈가 개발한 HER2 ADC ‘트라스투주맙 엠탄신(T-DM1, 제품명 캐싸일라)’ 대비 무진행생존기간(PFS)에서 29.0개월 대 7.8개월을 기록했다. 전체 생존기간(OS)은 56.4개월 대 42.7개월로 약 13.7개월 연장됐다. 5년 전체 생존율도 48.1% 대 36.9%로 약 11.2%포인트 차이를 보이며 우위를 확인했다.
ADC 적용 범위가 HER2 고발현 환자에서 저발현자까지 확장되고 있다. DESTINY-Breast04 연구에서는 HER2 저발현(low) 환자군에서도 의미 있는 치료 효과가 확인됐다. 호르몬수용체 양성(HR+) HER2 저발현 환자군에서 T-DXd는 무진행생존기간 10.1개월, 전체 생존기간 23.9개월을 기록, 기존 화학요법 대비 생존기간을 유의하게 연장했다. 전체 환자 기준으로도 PFS 9.9개월, OS 23.4개월이 보고됐다.
이 교수는 “HER2 발현이 낮은 환자에게서도 효과가 나타난다는 점은 ADC의 작용 기전에 대한 기존 인식을 바꾸는 결과”라며 “ADC가 단순한 표적치료제를 넘어 새로운 약물 전달 플랫폼으로 발전하고 있다는 점을 보여준다”고 말했다.
표적 발현만으로 설명 어려운 ADC 효과
ADC 임상 결과에서 주목되는 점은 표적 단백질 발현 수준만으로 치료 효과를 설명하기 어렵다는 점이다. T-DXd의 DAISY 임상 연구에서는 HER2 고발현 환자에서 객관적 반응률(ORR) 70.6%, HER2 저발현 환자에서는 37.5%가 확인됐다.
흥미로운 점은 HER2 발현이 거의 없는 환자에게서도 29.7%의 반응률이 관찰됐다는 사실이다. 연구자들은 이러한 결과가 ADC에서 나타나는 바이스탠더 효과(bystander effect) 등 복합적인 약물 전달 기전과 관련될 가능성을 제시하고 있다.
ADC는 암세포 내부에서 페이로드(payload)가 방출된 뒤 주변 세포로 확산될 수 있다. 이 과정에서 표적 발현이 낮은 종양 세포도 영향을 받을 수 있다. 이 교수는 “이러한 특성은 ADC가 단순한 표적치료제를 넘어 새로운 형태의 약물 전달 플랫폼으로 작동할 수 있음을 보여준다”고 말했다.
ADC 내성 문제와 바이오마커 필요성
ADC가 빠르게 확산되면서 새로운 과제도 떠오르고 있다. 대표적인 문제는 내성(resistance)이다. △표적 항원 발현 감소 △ADC 세포 내 흡수 및 엔도좀·리소좀 처리 과정 변화 △페이로드 약물에 대한 세포 내 저항성 △ATP- cassette(ABC) transporter 활성 증가에 따른 약물 유출 증가 등이 문제로 지목되고 있다.
이 때문에 향후 ADC 개발에서는 치료 반응을 예측할 수 있는 바이오마커 개발이 중요한 과제가 될 전망이다. 현재 연구 단계에서 제시되는 후보 지표로는 TOP1 변이, TACSTD2/TROP2 관련 변이, Cathepsin L(CTSL), p95HER2 등이 있다. 해당 지표는 아직 탐색적 연구 단계에 머물러 있으며, 임상에서 확립된 동반진단 바이오마커는 아니다.
전문가들은 ADC 치료 전략에서도 환자 선별(patient selection)과 치료 순서(sequence) 결정이 더 중요해질 것으로 보고 있다.
이중특이항체, 차세대 플랫폼으로 부상
ADC가 현재 항암제 시장을 주도하는 플랫폼이라면, 이중특이항체는 다음 세대를 준비하는 기술로 평가된다. 이중특이항체는 두 개의 서로 다른 항원을 동시에 인식하도록 설계된 항체다.
대표적인 접근법 중 하나는 T세포와 종양세포를 직접 연결하는 T-cell 결합(engager) 구조다. CD3와 종양 항원을 동시에 결합해 T세포가 암세포를 직접 공격하도록 유도하는 방식이다. DLL3와 CD3를 동시에 표적하는 이중특이항체 암젠의 ‘탈라타맙(tarlatamab)’이 대표 사례다.
탈라타맙은 재발성 소세포폐암 환자를 대상으로 한 임상 연구에서 전체 생존기간 약 13.6개월을 기록했다. 이는 같은 연구에서 보고된 화학요법 대조군 약 8.3개월 대비 생존기간이 연장된 결과로 평가된다.
또 다른 접근은 면역관문을 동시에 차단하는 전략이다. PD-1과 TIGIT을 동시에 표적하는 이중특이항체 아스트라제네카의 '릴베고스토미그(rilvegostomig)'는 비소세포폐암 초기 임상에서 면역관문억제제 치료 경험이 없는 전이성 비소세포폐암 환자를 대상으로 평가했다.
그 결과, PD-L1 발현 1~49% 환자군에서는 객관적 반응률 약 29%, PD-L1 발현 50% 이상 환자군에서는 61.8%의 반응률이 보고됐다. 업계에서는 이러한 결과가 차세대 면역항암 전략의 가능성을 보여주는 신호로 해석하고 있다.
차세대 ADC 기술 경쟁 시작
ADC 플랫폼 자체도 빠르게 발전하고 있다. 최근 연구에서는 이중 페이로드 ADC(dual-payload ADC), 이중특이 ADC(bispecific ADC), 면역 자극형 페이로드(immunostimulatory payload) 등 다양한 설계 전략이 시도되고 있다.
이 교수는 “최근 기존 ADC에서 나타나는 내성 문제를 극복하기 위한 연구가 활발히 진행되고 있으며, 향후 기술 경쟁의 핵심은 페이로드 종류와 링커 기술, 항체 설계가 될 것”이라면서 “면역 반응을 자극하는 페이로드가 개발되면, ADC는 단순한 세포독성 약물이 아니라 면역항암 효과까지 동시에 유도하는 플랫폼으로 확장될 수 있다”라고 말했다.
이어 그는 “HER2 발현이 매우 낮은 HER2 초저발현(ultra-low) 환자군에서도 ADC 치료 가능성이 논의되고 있는 것도 중요한 사안"이라면서 "ADC는 특정 표적 발현 여부를 넘어서는 새로운 약물 전달 플랫폼으로 진화하고 있다”고 설명했다.
이 교수는 “ADC는 이미 화학요법 대비 일관된 생존 개선 효과를 보여주며 항암 치료의 핵심 플랫폼으로 자리 잡았다”며 “향후 항암제 개발 경쟁은 ADC와 이중특이항체 같은 항체 기반 모달리티를 중심으로 전개될 가능성이 높다”고 덧붙였다.

무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
