의약품 품질시스템 도입 등 GMP 종합 개편안 발간
식약처, 2월~10월 시행한 주요 제도 개선사항 현장 적용 위해 마련
입력 2020.12.02 09:41
수정 2020.12.02 09:50
식품의약품안전처(처장 김강립)는 올해 추진한 의약품 제조 및 품질관리기준(GMP)에 관한 평가 방법 개편사항 등을 종합한 안내서를 발간했다.
이번 안내서는 올해 2월부터 10월까지 시행한 주요 제도 개선사항을 제약 현장에서 원활하게 적용할 수 있도록 마련됐으며, 업계의 이해도를 높이기 위해 그간의 주요 질의·답변 내용을 추가했다.
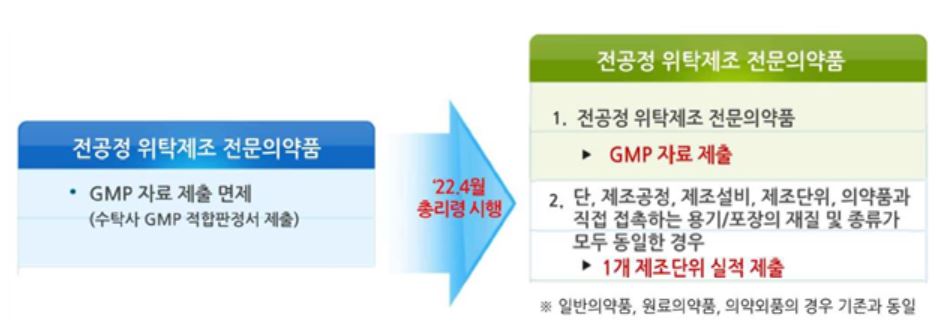
주요 내용으로 동일한 제조공정으로 위탁생산하는 전문의약품에 대한 자료제출 요건 강화를 위해 전공정 위탁제조 품목(전문의약품) GMP 평가 자료제출 의무화했다.
또한 전주기 관리를 위한 ‘의약품 품질시스템(Pharmaceutical Quality System)’을 도입
해 의약품 개발부터 생산 및 판매종료까지 지속적 개선을 촉진하는 관리 시스템으로 의약품 제조 및 품질관리기준과 품질위험관리를 포함한다.
이를 통해 품질 결함에 대한 조사를 위해 유통 중인 제품을 수거하는 경우에는 이를 회수로 간주하지 않도록 개선하고 위탁자 및 수탁자 간 책임과 기준 등에 대한 의약품 제조 및 품질관리 기준의 명확화할 수 있다.
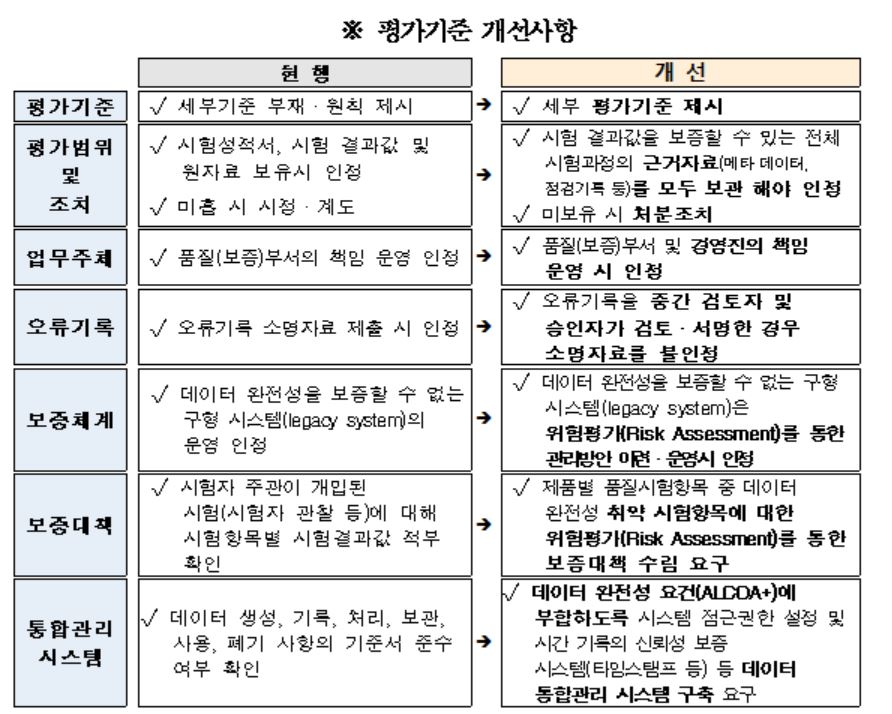
더불어 식약처는 의약품 허가신청 자료 및 품질관리의 신뢰성 향상을 위한 ‘의약품 제조·수입업체 데이터 완전성 평가지침’을 마련했다.

‘의약품 제조업체 데이터 완전성 평가지침’에 적합하도록 당해 업체의 품질관리기준서 등 4대 기준서를 반영한다. 적용대상은 2021년 1월 1일 이후 식약처에 허가 신청하는 신약(신물질 원료의약품 포함)에 한정(행정 지시일 이전 작성된 자료는 적용대상에서 제외)한다.

‘의약품 제조업체 데이터 완전성 평가지침’에 적합하도록 당해 업체의 품질관리기준서 등 4대 기준서를 반영한다. 적용대상은 2021년 1월 1일 이후 식약처에 허가 신청하는 신약(신물질 원료의약품 포함)에 한정(행정 지시일 이전 작성된 자료는 적용대상에서 제외)한다.
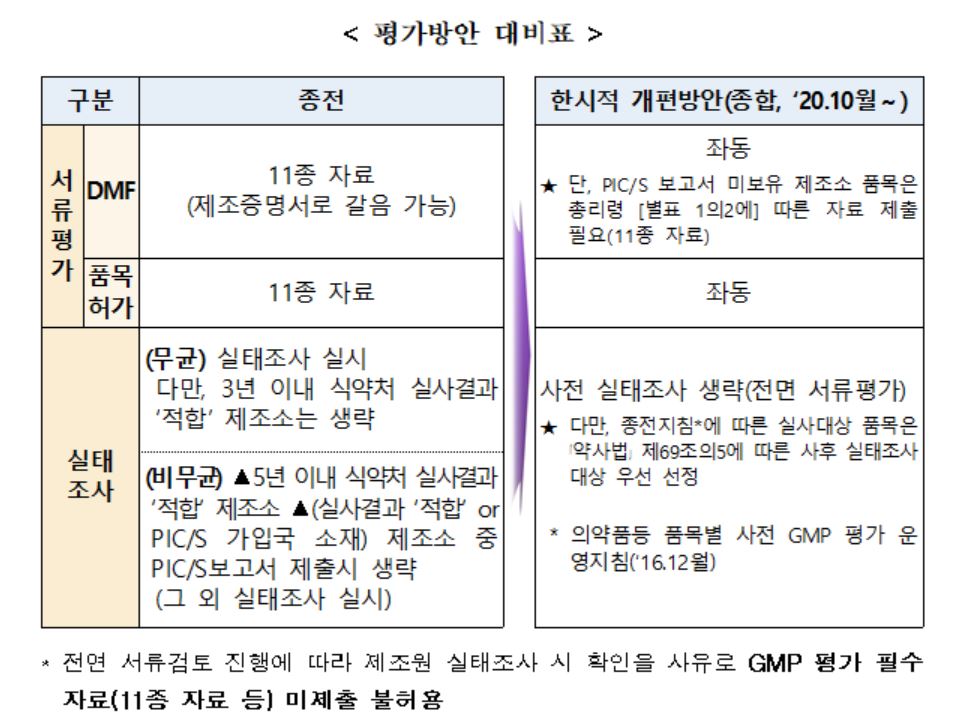
더불어 코로나19 확산 및 장기화에 따라 단계적으로 시행하는 수입의약품 GMP 평가 도 개편했다. ‘코로나 19’ 상황 종료시까지 접수되는 허가 또는 등록 신청 건(기 접수 품목 및 변경 포함)에 대해 평가방안(1~3차 종합)을 적용할 계획이다.
식약처는 앞으로도 국내 제약업계에서 국제적 수준의 제조 및 품질관리기준(GMP)을 도입·활용하도록 하여 보다 우수한 품질의 의약품을 국민께 공급하기 위해 노력하겠다고 밝혔다.
오늘의 헤드라인
전체댓글 0개
등록된 댓글이 없습니다.
| 인기기사 | 더보기 + |
-
1 [AACR] 에이비엘바이오 승부수 이중항체 ADC ‘ABL209’ 첫 청신호 켜졌다 -
2 디앤디파마텍 MASH 치료제 임상2상 48주 데이터베이스 락 완료 -
3 상장 제약·바이오 2025년 평균 부채비율 코스피 88.13%·코스닥 64.01% -
4 큐리옥스,'Pluto Code' 전사적 도입 포괄적 소프트웨어 라이선스 계약 체결 -
5 네이처셀,조인트스템 FDA 가속승인 본격화..브리핑 패키지 제출 -
6 상장 제약·바이오 2025년 평균 유보율 코스피 2142.15%·코스닥 2583.86% -
7 코아스템켐온, 15억 규모 범부처재생의료 사업 선정…CRISPR 'ALS 세포·유전자치료제' 개발 -
8 [AACR] 리가켐바이오가 던진 ‘BCMA ADC 신약’ 비임상 결과의 의미 -
9 유통업계, 대웅 본사 집결…"거점도매 철회" 결사항전 -
10 2025 빅파마 TOP5…순위는 유지, 성장 동력은 교체 ①
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

의약품 품질시스템 도입 등 GMP 종합 개편안 발간
식약처, 2월~10월 시행한 주요 제도 개선사항 현장 적용 위해 마련
- 박선혜 기자 loveloveslee@yakup.com
- 입력 2020.12.02 09:41 수정 2020.12.02 09:50
식품의약품안전처(처장 김강립)는 올해 추진한 의약품 제조 및 품질관리기준(GMP)에 관한 평가 방법 개편사항 등을 종합한 안내서를 발간했다.
이번 안내서는 올해 2월부터 10월까지 시행한 주요 제도 개선사항을 제약 현장에서 원활하게 적용할 수 있도록 마련됐으며, 업계의 이해도를 높이기 위해 그간의 주요 질의·답변 내용을 추가했다.
주요 내용으로 동일한 제조공정으로 위탁생산하는 전문의약품에 대한 자료제출 요건 강화를 위해 전공정 위탁제조 품목(전문의약품) GMP 평가 자료제출 의무화했다.

또한 전주기 관리를 위한 ‘의약품 품질시스템(Pharmaceutical Quality System)’을 도입
해 의약품 개발부터 생산 및 판매종료까지 지속적 개선을 촉진하는 관리 시스템으로 의약품 제조 및 품질관리기준과 품질위험관리를 포함한다.
이를 통해 품질 결함에 대한 조사를 위해 유통 중인 제품을 수거하는 경우에는 이를 회수로 간주하지 않도록 개선하고 위탁자 및 수탁자 간 책임과 기준 등에 대한 의약품 제조 및 품질관리 기준의 명확화할 수 있다.
더불어 식약처는 의약품 허가신청 자료 및 품질관리의 신뢰성 향상을 위한 ‘의약품 제조·수입업체 데이터 완전성 평가지침’을 마련했다.

‘의약품 제조업체 데이터 완전성 평가지침’에 적합하도록 당해 업체의 품질관리기준서 등 4대 기준서를 반영한다. 적용대상은 2021년 1월 1일 이후 식약처에 허가 신청하는 신약(신물질 원료의약품 포함)에 한정(행정 지시일 이전 작성된 자료는 적용대상에서 제외)한다.

‘의약품 제조업체 데이터 완전성 평가지침’에 적합하도록 당해 업체의 품질관리기준서 등 4대 기준서를 반영한다. 적용대상은 2021년 1월 1일 이후 식약처에 허가 신청하는 신약(신물질 원료의약품 포함)에 한정(행정 지시일 이전 작성된 자료는 적용대상에서 제외)한다.

더불어 코로나19 확산 및 장기화에 따라 단계적으로 시행하는 수입의약품 GMP 평가 도 개편했다. ‘코로나 19’ 상황 종료시까지 접수되는 허가 또는 등록 신청 건(기 접수 품목 및 변경 포함)에 대해 평가방안(1~3차 종합)을 적용할 계획이다.

식약처는 앞으로도 국내 제약업계에서 국제적 수준의 제조 및 품질관리기준(GMP)을 도입·활용하도록 하여 보다 우수한 품질의 의약품을 국민께 공급하기 위해 노력하겠다고 밝혔다.
Copyright © Yakup.com All rights reserved.
약업신문 의 모든 컨텐츠(기사)는 저작권법의 보호를 받습니다.
무단 전재·복사·배포 등을 금지합니다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
