 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
유방암 및 난소암 치료제인 '파클리탁셀' 함유제제를 투여받은 환자들에게 과민반응과 대사 및 영양 이상반응 등이 발생된 것으로 보고됐다.
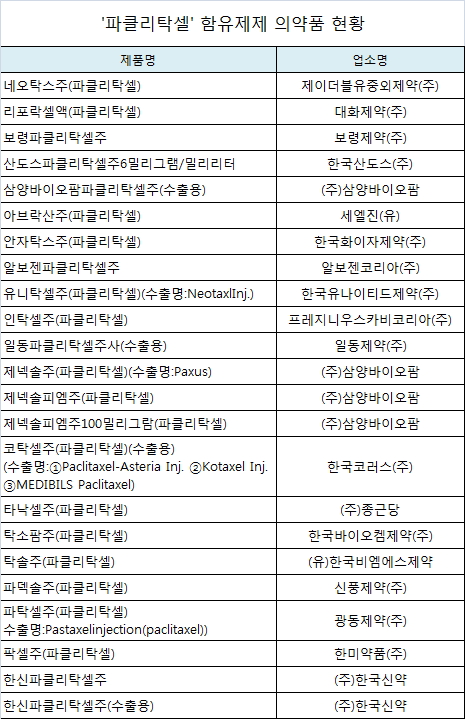
식품의약품안전처는 유럽 의약품청(EMA) 및 미국 식품의약품청(FDA)의 '파클리탁셀' 함유제제 관련 안전성 정보에 대한 검토결과에 따라 19개 제약사 23개 품목의 허가사항을 변경할 계획이라고 13일 밝혔다.
식약처에 따르면 '파클리탁셀' 함유제제의 시판 후 조사에서 과민반응과 대사 및 영양이상반응 보고가 있었던 것으로 파악됐다.
구체적으로 '파클리탁셀' 함유제제 시판 후 조사에서 아브락산 제제와 다른 탁산(taxane)계 제제들 간에 아나필락시스와 같은 중증의 반응을 포함한 교차과민반응이 보고됐다는 것.
또 '파클리탁셀' 함유제제를 투여받은 환자에게서 대사 및 영양 이상반응인 종양용해증후군도 보고됐다고 식약처는 설명했다.
유럽 의약품청(EMA) 및 미국 식품의약품청(FDA)의 안전성 정보에 따라 식약처는 '파클리탁셀' 함유제제 의약품 제조 및 수입업체에 허가사항 변경을 준비하라는 입장을 전달했다.
| 인기기사 | 더보기 + |
-
1 상장 제약·바이오 2025년 평균 자기자본이익률 코스피 0.30%·코스닥 -2.57% -
2 네이처셀,미국FDA 승인 알츠하이머병 임상 2b상 본격 개시 -
3 경구 GLP-1 시장 개막…노보 ‘선점’, 릴리 ‘추격’ -
4 "유럽 의료진 85%가 쓴다…'생성형 AI' 임상 현장 이미 장악" -
5 '혁신형 제약기업' 신규 인증… '절대평가·65점'이 당락 가른다 -
6 애브비, 주름개선제 허가신청 FDA 반려 주름살? -
7 “규제에서 현실로” DIA Korea Annual Meeting 2026 성료 -
8 코오롱티슈진 ‘TG-C’, 17년 안전성 국제골관절염학회서 공개 -
9 로슈, 환율 직격탄…1분기 실적 기대치 하회 -
10 상장 바이오헬스기업, 2025년 성장·수익성 개선 흐름 지속
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 김용주 기자 yjkim@yakup.com
- 입력 2019.03.13 12:00 수정 2019.03.13 12:21
유방암 및 난소암 치료제인 '파클리탁셀' 함유제제를 투여받은 환자들에게 과민반응과 대사 및 영양 이상반응 등이 발생된 것으로 보고됐다.
식품의약품안전처는 유럽 의약품청(EMA) 및 미국 식품의약품청(FDA)의 '파클리탁셀' 함유제제 관련 안전성 정보에 대한 검토결과에 따라 19개 제약사 23개 품목의 허가사항을 변경할 계획이라고 13일 밝혔다.
식약처에 따르면 '파클리탁셀' 함유제제의 시판 후 조사에서 과민반응과 대사 및 영양이상반응 보고가 있었던 것으로 파악됐다.
구체적으로 '파클리탁셀' 함유제제 시판 후 조사에서 아브락산 제제와 다른 탁산(taxane)계 제제들 간에 아나필락시스와 같은 중증의 반응을 포함한 교차과민반응이 보고됐다는 것.
또 '파클리탁셀' 함유제제를 투여받은 환자에게서 대사 및 영양 이상반응인 종양용해증후군도 보고됐다고 식약처는 설명했다.
유럽 의약품청(EMA) 및 미국 식품의약품청(FDA)의 안전성 정보에 따라 식약처는 '파클리탁셀' 함유제제 의약품 제조 및 수입업체에 허가사항 변경을 준비하라는 입장을 전달했다.

무단 전재·복사·배포 등을 금지합니다.



