티쎈트릭 초기 폐암 보조요법 확대 인정…브레즈트리·보노프라잔 계열도 적정성 확보
건강보험심사평가원 약제급여평가위원회(약평위)가 CAR-T 치료제 ‘예스카타’와 미만성 거대 B세포 림프종(DLBCL) 치료제 ‘폴라이비’, RET 변이 표적항암제 ‘레테브모’ 등에 대해 급여 적정성이 있다고 판단했다.
반면 한국얀센의 비소세포폐암 치료제 ‘리브리반트’는 재심의 결정을 받았다.
건강보험심사평가원은 7일 ‘2026년 제5차 약제급여평가위원회 심의 결과’를 공개했다.
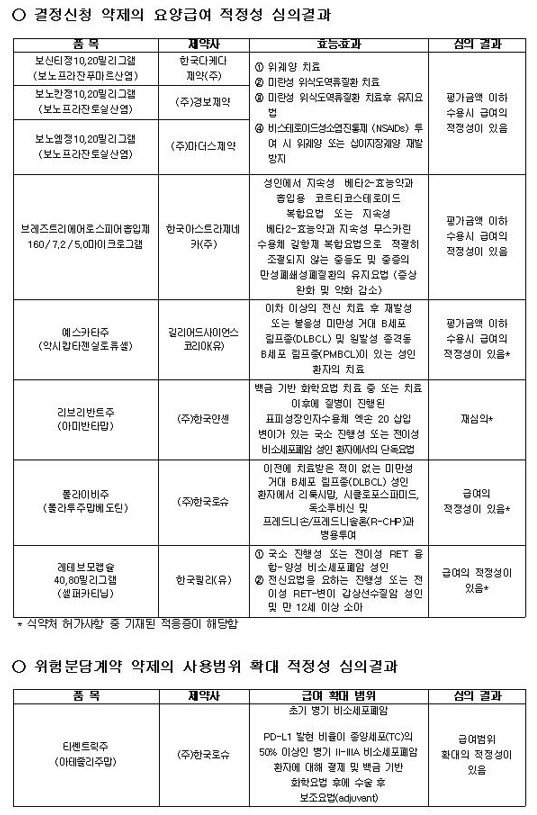
이번 심의에서 길리어드사이언스코리아의 CAR-T 치료제 예스카타주(악시캅타젠실로류셀)는 이차 이상 전신 치료 후 재발성 또는 불응성 미만성 거대 B세포 림프종(DLBCL) 및 원발성 종격동 B세포 림프종(PMBCL) 성인 환자 치료 적응증에 대해 ‘평가금액 이하 수용 시 급여의 적정성이 있음’으로 판단됐다.
한국로슈의 폴라이비주(폴라투주맙베도틴)는 이전 치료 경험이 없는 DLBCL 성인 환자에서 R-CHP 요법과 병용 투여하는 적응증에 대해 급여 적정성을 인정받았다.
한국릴리의 레테브모캡슐(셀퍼카티닙) 역시 RET 융합 양성 비소세포폐암과 RET 변이 갑상선수질암 적응증에 대해 급여 적정성이 있다고 평가됐다.
반면 한국얀센의 리브리반트주(아미반타맙)는 EGFR 엑손20 삽입 변이 비소세포폐암 단독요법 적응증으로 급여 평가를 받았으나 재심의 결정이 내려졌다.
이와 함께 위험분담계약(RSA) 약제 사용범위 확대 심의에서는 한국로슈의 티쎈트릭주(아테졸리주맙)가 PD-L1 발현 비율이 종양세포(TC)의 50% 이상인 병기 II~IIIA 초기 비소세포폐암 환자 대상 수술 후 보조요법(adjuvant) 적응증에 대해 급여범위 확대의 적정성을 인정받았다.
비항암제 분야에서는 한국다케다제약의 보신티정(보노프라잔푸마르산염), 경보제약 보노칸정, 마더스제약 보노엠정 등 보노프라잔 계열 치료제가 위궤양 및 위식도역류질환 치료 적응증 등에서 평가금액 이하 수용 시 급여 적정성이 있는 것으로 판단됐다.
또 한국아스트라제네카의 COPD 치료제 브레즈트리에어로스피어흡입제 역시 중등도·중증 만성폐쇄성폐질환 유지요법 적응증에 대해 평가금액 이하 수용 시 급여 적정성이 있다고 평가됐다.
| 인기기사 | 더보기 + |
-
1 [기고] 김 변호사의 쉽게 읽는 바이오 ②알테오젠 -
2 메지온 “ ADPKD 치료제 임상,진행 중 전임상 종료후 2상 시작 가능” -
3 복지부 "첨단재생의료 치료 1호, 희귀질환 극복의 실질적 이정표" -
4 유통협회, '이지메디컴' 정조준…병원도매 합류로 대웅 압박 전면전 -
5 로킷헬스케어, 사우디 만성신장질환 AI 플랫폼 계약 체결 -
6 상장 제약바이오 환율변동손익 ‘뚝’…코스피 55.3%↓·코스닥 손실 전환 -
7 에임드바이오,베링거 인겔하임서 'ODS025' 기술이전 연구개발비 수령 -
8 2027년도 수가협상 시작…의약단체 "보상 필요" 공단 "재정 부담" -
9 알파타우, 미국 췌장암 임상 범위 확대… FDA IDE 보충안 승인 획득 -
10 대웅제약, 2억3900만불 규모 한올바이오 기술이전 계약 지위 승계
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 전하연 기자 hayeon@yakup.com
- 입력 2026.05.07 23:26

건강보험심사평가원 약제급여평가위원회(약평위)가 CAR-T 치료제 ‘예스카타’와 미만성 거대 B세포 림프종(DLBCL) 치료제 ‘폴라이비’, RET 변이 표적항암제 ‘레테브모’ 등에 대해 급여 적정성이 있다고 판단했다.
반면 한국얀센의 비소세포폐암 치료제 ‘리브리반트’는 재심의 결정을 받았다.
건강보험심사평가원은 7일 ‘2026년 제5차 약제급여평가위원회 심의 결과’를 공개했다.
이번 심의에서 길리어드사이언스코리아의 CAR-T 치료제 예스카타주(악시캅타젠실로류셀)는 이차 이상 전신 치료 후 재발성 또는 불응성 미만성 거대 B세포 림프종(DLBCL) 및 원발성 종격동 B세포 림프종(PMBCL) 성인 환자 치료 적응증에 대해 ‘평가금액 이하 수용 시 급여의 적정성이 있음’으로 판단됐다.
한국로슈의 폴라이비주(폴라투주맙베도틴)는 이전 치료 경험이 없는 DLBCL 성인 환자에서 R-CHP 요법과 병용 투여하는 적응증에 대해 급여 적정성을 인정받았다.
한국릴리의 레테브모캡슐(셀퍼카티닙) 역시 RET 융합 양성 비소세포폐암과 RET 변이 갑상선수질암 적응증에 대해 급여 적정성이 있다고 평가됐다.
반면 한국얀센의 리브리반트주(아미반타맙)는 EGFR 엑손20 삽입 변이 비소세포폐암 단독요법 적응증으로 급여 평가를 받았으나 재심의 결정이 내려졌다.
이와 함께 위험분담계약(RSA) 약제 사용범위 확대 심의에서는 한국로슈의 티쎈트릭주(아테졸리주맙)가 PD-L1 발현 비율이 종양세포(TC)의 50% 이상인 병기 II~IIIA 초기 비소세포폐암 환자 대상 수술 후 보조요법(adjuvant) 적응증에 대해 급여범위 확대의 적정성을 인정받았다.
비항암제 분야에서는 한국다케다제약의 보신티정(보노프라잔푸마르산염), 경보제약 보노칸정, 마더스제약 보노엠정 등 보노프라잔 계열 치료제가 위궤양 및 위식도역류질환 치료 적응증 등에서 평가금액 이하 수용 시 급여 적정성이 있는 것으로 판단됐다.
또 한국아스트라제네카의 COPD 치료제 브레즈트리에어로스피어흡입제 역시 중등도·중증 만성폐쇄성폐질환 유지요법 적응증에 대해 평가금액 이하 수용 시 급여 적정성이 있다고 평가됐다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
