박셀바이오(대표 이제중)가 24일 진행성 간세포암을 표적으로 한 2세대 NK 치료법에 대한 특허를 출원했다고 밝혔다.
진행성 간암 치료제 Vax-NK/HCC의 임상2a상 종료에 따라 조만간 최종보고서를 식품의약품안전처에 제출하고, 해당 치료제의 조건부허가를 위한 신속처리 대상 지정 신청 절차도 진행하는 과정에서 상업화 기반을 공고히 하려는 조치로 풀이된다.
Vax-NK/HCC는 진행성 간세포암을 대상으로 한 박셀바이오의 대표적인 파이프라인 중 하나다. 임상 1상과 2a상에서 객관적 반응률과 질병조절률이 높게 나타나 관련 업계가 상업화 과정에 주목하고 있다.
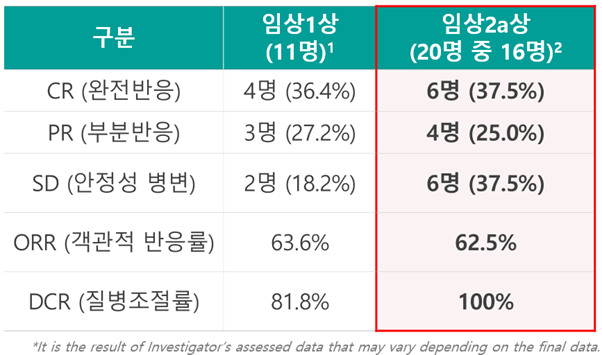
박셀바이오에 따르면 Vax-NK/HCC 치료제는 임상 1상에서 투약 환자 11명 중 4명이 완전반응(CR, Complete Response)을 보이는 등 63.6%의 객관적 반응률(ORR, Objective Response Rate)과 81.8%의 질병조절률(DCR, Disease Control Rate)을 기록했다. 이어 진행한 임상2a상에서는 16명의 환자 중 6명이 완전반응을 나타내는 등 100%의 질병조절률을 기록했다.
임상시험은 다음 단계로 진행할 때 치료 확률이 낮아지는 것이 통계적으로 나타나고 있지만, Vax-NK/HCC의 경우 임상1상과 임상2a상 둘 다 높은 수준의 유사한 반응률과 질병조절률을 보여 신약 개발의 가늠자 중 하나인 재현성을 확보한 것으로 확인됐다.
박셀바이오 이제중 대표이사는 “치료가 어려운 진행성 간암의 치료제는 임상연구에서 수차례의 스크리닝 중 한 번이라도 완전반응이나 부분반응이 나오면 암에 객관적으로 반응한다는 평가를 받는다"면서 “또 안정성 병변 이상만 나와도 치료 효과가 있는 것으로 간주된다”고 말했다 반면 Vax-NK/HCC는 1상과 2a상 둘 다 완전 및 부분 반응률이 상당히 높게 나와 관련 학계와 제약업계가 주목하고 있다.
이 대표는 "박셀바이오가 이 같은 연구 데이터를 바탕으로 특허를 출원한 것은 Vax-NK/HCC의 조건부 승인을 위한 신속처리 대상 신청을 진행하면서 해당 치료제의 상용화 기반을 강화하기 위한 것”이라고 설명했다.
한편 박셀바이오는 간세포암과 소세포폐암 등을 타깃으로 한 Vax-NK 플랫폼, 다발골수종 등 혈액암과 위암 등 고형암을 표적으로 한 Vax-CAR 플랫폼, 반려동물 전용 항암치료제인 박스루킨-15 플랫폼 등을 주요 파이프라인으로 갖춘 항암면역세포치료제 개발 전문 회사이다. 올해 상반기 중 Vax-NK/HCC 임상 2a상 최종 결과 보고서를 식약처에 제출하고 조건부 허가를 위한 신속처리 대상 지정도 신청할 계획이다. 농림축산검역본부에서 박스루킨-15에 대한 품목허가를 받으면 빠르게 치료제 생산 및 출시를 진행해 주요 파이프라인이 매출로 이어지는 통로를 본격적으로 열 수 있을 것으로 기대하고 있다.
| 인기기사 | 더보기 + |
-
1 유통업계, 대웅 본사 집결…"거점도매 철회" 결사항전 -
2 [2026 기대 신약 TOP 10] ④ 피부근염 치료제 '브레포시티닙' -
3 의료현장 난제 푸는 '한국형 ARPA-H'… 열쇠는 에이전트 AI 생태계 -
4 에이비엘바이오, 이중항체 ADC 'ABL209' AACR 학술지 게재…"독성 한계 극복" -
5 미국 의약품 제조업을 다시 강하게? 알고 보니.. -
6 약포지·시럽병 숨통 트였지만…현장은 '재고 격차' 여전 -
7 김준 고려대 교수팀·하엘,캔디다증 치료제 미국·유럽·중국 특허 획득 -
8 지투지바이오,비만-치매 치료제 등 파이프라인 진행상황 공개 -
9 갤럭스 -GC녹십자 ,자가면역질환 항체 신약 공동개발 계약 -
10 [기업분석] 화장품 기업 82개사 2025년 타사품 유통매출 평균 402억…전년比 18.8%↑
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 권혁진 기자 hjkwon@yakup.com
- 입력 2024.04.24 14:14
박셀바이오(대표 이제중)가 24일 진행성 간세포암을 표적으로 한 2세대 NK 치료법에 대한 특허를 출원했다고 밝혔다.
진행성 간암 치료제 Vax-NK/HCC의 임상2a상 종료에 따라 조만간 최종보고서를 식품의약품안전처에 제출하고, 해당 치료제의 조건부허가를 위한 신속처리 대상 지정 신청 절차도 진행하는 과정에서 상업화 기반을 공고히 하려는 조치로 풀이된다.
Vax-NK/HCC는 진행성 간세포암을 대상으로 한 박셀바이오의 대표적인 파이프라인 중 하나다. 임상 1상과 2a상에서 객관적 반응률과 질병조절률이 높게 나타나 관련 업계가 상업화 과정에 주목하고 있다.

박셀바이오에 따르면 Vax-NK/HCC 치료제는 임상 1상에서 투약 환자 11명 중 4명이 완전반응(CR, Complete Response)을 보이는 등 63.6%의 객관적 반응률(ORR, Objective Response Rate)과 81.8%의 질병조절률(DCR, Disease Control Rate)을 기록했다. 이어 진행한 임상2a상에서는 16명의 환자 중 6명이 완전반응을 나타내는 등 100%의 질병조절률을 기록했다.
임상시험은 다음 단계로 진행할 때 치료 확률이 낮아지는 것이 통계적으로 나타나고 있지만, Vax-NK/HCC의 경우 임상1상과 임상2a상 둘 다 높은 수준의 유사한 반응률과 질병조절률을 보여 신약 개발의 가늠자 중 하나인 재현성을 확보한 것으로 확인됐다.
박셀바이오 이제중 대표이사는 “치료가 어려운 진행성 간암의 치료제는 임상연구에서 수차례의 스크리닝 중 한 번이라도 완전반응이나 부분반응이 나오면 암에 객관적으로 반응한다는 평가를 받는다"면서 “또 안정성 병변 이상만 나와도 치료 효과가 있는 것으로 간주된다”고 말했다 반면 Vax-NK/HCC는 1상과 2a상 둘 다 완전 및 부분 반응률이 상당히 높게 나와 관련 학계와 제약업계가 주목하고 있다.
이 대표는 "박셀바이오가 이 같은 연구 데이터를 바탕으로 특허를 출원한 것은 Vax-NK/HCC의 조건부 승인을 위한 신속처리 대상 신청을 진행하면서 해당 치료제의 상용화 기반을 강화하기 위한 것”이라고 설명했다.
한편 박셀바이오는 간세포암과 소세포폐암 등을 타깃으로 한 Vax-NK 플랫폼, 다발골수종 등 혈액암과 위암 등 고형암을 표적으로 한 Vax-CAR 플랫폼, 반려동물 전용 항암치료제인 박스루킨-15 플랫폼 등을 주요 파이프라인으로 갖춘 항암면역세포치료제 개발 전문 회사이다. 올해 상반기 중 Vax-NK/HCC 임상 2a상 최종 결과 보고서를 식약처에 제출하고 조건부 허가를 위한 신속처리 대상 지정도 신청할 계획이다. 농림축산검역본부에서 박스루킨-15에 대한 품목허가를 받으면 빠르게 치료제 생산 및 출시를 진행해 주요 파이프라인이 매출로 이어지는 통로를 본격적으로 열 수 있을 것으로 기대하고 있다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
