-
 HOME
HOME
- >
- 타이틀 텍스트
- >
- 서브 타이틀 텍스트

1998년부터 후생노동성에서는 수출용 의약품에 대하여 WHO certification system에 따른 의약품 허가·승인 관련 증명서를 발급하고 있다. 승인·허가의 유무, GMP 이행 유무, 제품정보 등에 관련한 내용을 포함한다.
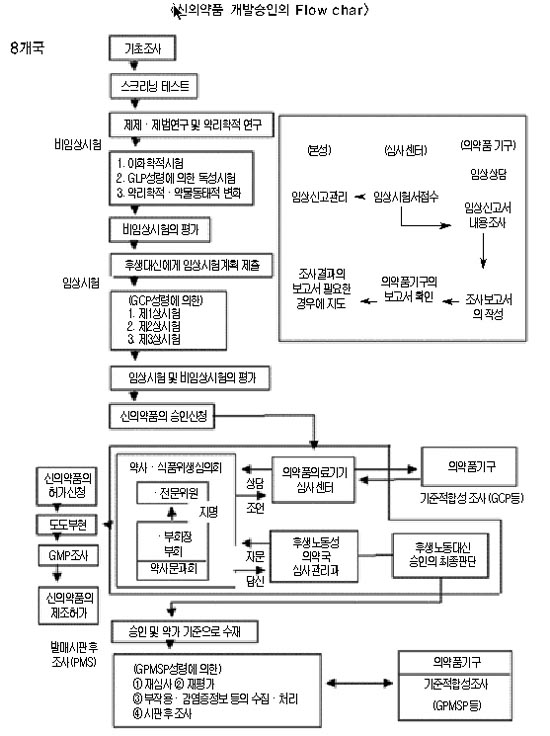 |
4. 신약의 개발·승인
신약의 개발 및 승인의 흐름은 다음의 그림과 같다(승인 세부 절차는 그림 참조).
일본의 의약품 승인신청은「의약품 승인 신청에 대해」(1999년 4월 8일, 의약발 제481호)에 의하여 새로운 체계를 갖추었다. 또한 '의약품 개발의 국제화' 등의 상황에 의하여 ICH 가이드라인을 따르는 것으로 CTD가「의약품 승인신청에 첨부하여야 할 자료 취급에 대하여」(2001년 6월 21일, 의약발 제663호)로 통지되었다.
의약품의 승인 신청시 첨부하여야 할 자료는 다음과 같다(2001년 6월 21일, 의약심발 899호).
표 2-1 의약품 승인신청 첨부자료 목록
|
1. 제1부 (신청서 등 행정정보 및 첨부문서에 관한 정보) (1) 제1부 목차 (2) 승인신청서 (3) 증명서류 (승인신청 자료의 수집 작성 업무를 통괄한 책임자의 진술서, GP·GCP 관련 자료, 공동개발과 관련된 계약서) (4) 특허상황 (5) 기원 또는 발견의 경위 및 개발의 경위 (6) 외국에 있어서의 사용 상황 등에 관한 자료 (7) 동종 동효과 시나이치람표 (8) 첨부 문서서(안) (9) 일반적 명칭과 관련된 문서 (10) 독약·극약등의 지정 심사 자료의 통계 (11) 시판 후 조사 기본계획 서안 (12) 첨부자료 일람표 (13) 그 외 2. 제2부(자료 개요) (1) CTD 전체의 목차 (2) 머리말 (3) 품질에 관한 개괄 자료 (4) 비임상에 관한 개괄 평가 (5) 임상에 관한 개괄 평가 |
(6) 비임상 개요 ① 약리 ② 약물 동태 ③ 독성 (7) 임상 개요 ① 생물 약제학 및 관련 한 분석법의 개요 ② 임상 약리의 개요 ③ 임상적 유효성의 개요 ④ 임상적 안전성의 개요 ⑤ 개개의 시험의 통계 3. 제3부(품질에 관한 문서) (1) 목차 (2) 데이터 또는 보고서 (3) 참고 문헌 4. 제4부(비임상시험 보고서) (1) 목차 (2) 시험 보고서 (3) 참고 문헌 5. 제5부(임상시험 보고서) (1) 목차 (2) 임상시험 일람표 (3) 임상시험 보고서 및 관련 정보(치험의 총괄보고서 등을 말함) (4) 참고 문헌 |
5. 의약품 시판 후 조사
의약품 시판 후의 품질과 안전성·유효성의 확보를 위하여 PMS는 부작용·감영증 정보의 수집·처리제도(이하 부작용 보고제도), 재심사제도 및 재평가제도의 3개로 구성되어 있다(아래 그림).
| 인기기사 | 더보기 + |
-
1 [약업분석] HLB그룹 이자비용 489억원…총차입금의존도 평균 27% -
2 메지온,AEPC 2026서 'JURVIGO' 3상 추가임상 인지도 확대 '전력' -
3 [약업분석] HLB그룹 자기자본이익률 8곳 마이너스 -
4 [약업분석] 현대약품, 1Q 전 부문 ' 흑전'… 재무 건전성까지 질적 성장 -
5 코아스템켐온, 오송 공장 세포처리시설 허가 획득…첨단재생의료 사업 본격화 -
6 “왜 제약·바이오 공장은 일반 스마트팩토리로 부족한가” -
7 프로티나, 미국 IDT와 MOU 체결... 차세대 항체 치료제 개발 가속 -
8 차백신연구소, 김병록 경영지배인 선임 -
9 제21회 경기약사학술대회 개막…AI 시대 약사 미래 역할 모색 -
10 "체중감량 15% 장벽 넘은 GLP-1…대사질환 치료 ‘큰 파도’ 온다"
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 기자
- 입력 2005-12-07 15:40 수정 최종수정 2006-09-01 18:05

1998년부터 후생노동성에서는 수출용 의약품에 대하여 WHO certification system에 따른 의약품 허가·승인 관련 증명서를 발급하고 있다. 승인·허가의 유무, GMP 이행 유무, 제품정보 등에 관련한 내용을 포함한다.
 |
4. 신약의 개발·승인
신약의 개발 및 승인의 흐름은 다음의 그림과 같다(승인 세부 절차는 그림 참조).
일본의 의약품 승인신청은「의약품 승인 신청에 대해」(1999년 4월 8일, 의약발 제481호)에 의하여 새로운 체계를 갖추었다. 또한 '의약품 개발의 국제화' 등의 상황에 의하여 ICH 가이드라인을 따르는 것으로 CTD가「의약품 승인신청에 첨부하여야 할 자료 취급에 대하여」(2001년 6월 21일, 의약발 제663호)로 통지되었다.
의약품의 승인 신청시 첨부하여야 할 자료는 다음과 같다(2001년 6월 21일, 의약심발 899호).
표 2-1 의약품 승인신청 첨부자료 목록
|
1. 제1부 (신청서 등 행정정보 및 첨부문서에 관한 정보) (1) 제1부 목차 (2) 승인신청서 (3) 증명서류 (승인신청 자료의 수집 작성 업무를 통괄한 책임자의 진술서, GP·GCP 관련 자료, 공동개발과 관련된 계약서) (4) 특허상황 (5) 기원 또는 발견의 경위 및 개발의 경위 (6) 외국에 있어서의 사용 상황 등에 관한 자료 (7) 동종 동효과 시나이치람표 (8) 첨부 문서서(안) (9) 일반적 명칭과 관련된 문서 (10) 독약·극약등의 지정 심사 자료의 통계 (11) 시판 후 조사 기본계획 서안 (12) 첨부자료 일람표 (13) 그 외 2. 제2부(자료 개요) (1) CTD 전체의 목차 (2) 머리말 (3) 품질에 관한 개괄 자료 (4) 비임상에 관한 개괄 평가 (5) 임상에 관한 개괄 평가 |
(6) 비임상 개요 ① 약리 ② 약물 동태 ③ 독성 (7) 임상 개요 ① 생물 약제학 및 관련 한 분석법의 개요 ② 임상 약리의 개요 ③ 임상적 유효성의 개요 ④ 임상적 안전성의 개요 ⑤ 개개의 시험의 통계 3. 제3부(품질에 관한 문서) (1) 목차 (2) 데이터 또는 보고서 (3) 참고 문헌 4. 제4부(비임상시험 보고서) (1) 목차 (2) 시험 보고서 (3) 참고 문헌 5. 제5부(임상시험 보고서) (1) 목차 (2) 임상시험 일람표 (3) 임상시험 보고서 및 관련 정보(치험의 총괄보고서 등을 말함) (4) 참고 문헌 |
5. 의약품 시판 후 조사
의약품 시판 후의 품질과 안전성·유효성의 확보를 위하여 PMS는 부작용·감영증 정보의 수집·처리제도(이하 부작용 보고제도), 재심사제도 및 재평가제도의 3개로 구성되어 있다(아래 그림).
무단 전재·복사·배포 등을 금지합니다.



