-
 HOME
HOME
- >
- 타이틀 텍스트
- >
- 서브 타이틀 텍스트
서브 타이틀 텍스트
세계 각국의 의약품 허가 및 관리제도<8>
입력 2005-09-26 09:35
수정 최종수정 2006-09-05 17:27

Ⅰ. 미국 제네릭의약품 허가제도
미국 FDA는 1984년 Hatch-Waxman Act (Drug Price Competition and Patent Term Restoration Act)를 도입함으로써 제네릭 의약품 시장 규제에 큰 진보를 이루었다. Hatch-Waxman Act에서는 FDA에서 이미 승인받은 신약의 제네릭 의약품에 대하여 약식의 허가 절차 (Abbreviated New Drug Application; ANDA)를 적용하기로 하였다. 이에 해당하는 제네릭 의약품은 기존의 약과 활성성분, 용량, 강도, 복용경로, 사용조건이 모두 동일한 의약품이다. 이로써 오늘날 사용되고 있는 ANDA 절차가 생겨났고 이는 FDA의 의약품 평가 및 조사 센터 (CDER)와 제네릭 의약품국 (OGD)의 통합 보호 하에 관리되고 있다.
1. ANDA 절차
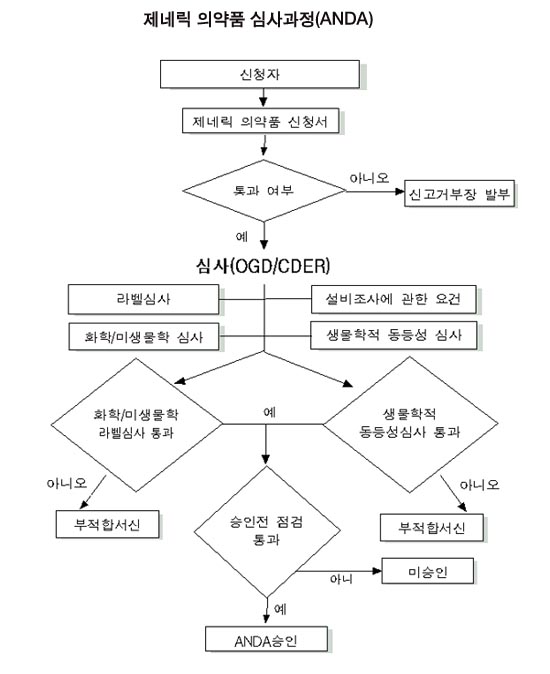 |
▣ 신청자
신청자란 약식 신의약품 신청서 (abbreviated new drug application, ANDA)나 제네릭 의약품을 시장 출시하기 위해 FDA의 승인을 획득하기 위한 수정안 또는 추가정보를 제출한 자 (일반적으로 제약회사를 이름) 및 승인된 신청서 또는 약식 신청서를 지닌 자를 이른다.
▣ 제네릭의약품 신청서
제네릭 의약품은 신약 (FDA의 치료적 동일 성분 평가를 거친 승인된 의약품리스트에 나온 의약품 (reference listed drug, 이하 RLD))과 복용량, 강도, 투여경로, 품질, 효과적 특징과 사용 의도면에서 동일하다.
"ANDA"는 "Abbreviated New Drug Application"의 약자이다. FDA의 Center for Drug Evaluation and Research(이하 CDER), Office of Generic Drugs(이하 OGD)에 제출시 제네릭 의약품에 대한 조사와 최종승인을 위한 자료를 포함한다. 일단 승인이 되면 신청자는 특허보호에 관한 문제 및 RLD와 연관된 독점권 문제가 해결이 되면 해당 제네릭 의약품을 제조, 출시할 수 있다.
제네릭 의약품 신청서는 일반적으로 안전성과 효능을 입증하기 위한 동물 및 인간 임상 데이터가 필요하지 않기 때문에 약식이라는 이름이 붙는다. 이러한 조건은 FDA가 승인한 의약품의 첫 상품인 신약이 받은 승인에 근거하여 성립된다.
▣ 통과 여부
신청서는 효과적이고 빠르게 의약품심사가 진행될 수 있도록 충분한 정보를 갖춰야 한다. 신청서를 받으면 OGD의 Regulatory Support Branch의 프로젝트 매니저는 신청서가 완벽하게 작성되었고 통과 가능한지에 대해 신고전 평가를 실시한다. 이 초기 의약품 심사에서 모든 필요한 사항을 포함하고 있다고 증명이 되면 심사를 받을 수 있고 신고날짜를 확인하는 "승인장"이 신청자에게 발송된다.
신청서가 생물학적 동등성 신고를 하기에 적절하다고 판단나면 화학/미생물학 및 라벨부착 심사가 시작된다.
▣ 신고거부장 발부
신청자가 한두 개의 중요한 사항을 빠뜨린다면 "신고거부장"이 신청자에게 발송된다. 이 신고거부장은 누락된 사항을 알려주고 이 사항을 보충할 때까지 신청 신고가 이루어지지 않는다는 점을 신청자에게 알린다. 신청자가 이 필요한 데이터를 제공해서 접수할 수 있고 완벽하다고 판단이 될 때까지 신청서 심사는 중단된다.
▣ 생물학적 동등성 심사
생물학적 동등성 심사과정에서는 해당 제네릭 의약품의 활성 성분이 체내에 흡수되는 속도와 양이 모두 RLD와 비교했을 때 설정된 범위안에 해당된다는 점에 근거해 RLD와 같은 생물학적 동등성을 지닌다는 점을 입증하게 된다.
FDA는 신청자로 하여금 생물학적 동등성을 입증하기 위한 상세한 정보를 제공하도록 한다. 신청자는 생체이용률 (활성성분 또는 활성 성분 일부분이 의약품 사용으로 신체내 흡수되어 효능이 일어나는 지점에 머무르는 속도와 양이 다음과 같은 데이터 제출로 증명될 수 있는 특정 의약품에 대해서는 인체내 생물학적 동등성 실험을 실시하지 않도록 하는 예외조항을 요구할 수 있다. 1) 성분이 동일한 구강용 물약, 주입 가능한 의약품, 안약류와 같이 생체이용률이 자명한 상품에 대한 성분비교 자료 2) 비교용출자료
하지만 해당 제네릭 의약품과 브랜드 의약품간의 성분 흡수속도와 양을 비교하는 인체내 생물학적 동등성 시험은 대다수의 정제와 캡슐제에는 필수적이다. 특정 상품에 대해서는 임상적 종료시점에 기반한 효능비교에 대한 상세한 평가가 필요할 수 있다.
▣ 라벨 심사
라벨심사과정에서는 해당 제네릭 의약품 라벨링 (포장된 삽입물, 삽입물 용기, 포장라벨, 환자용 참조정보)이 제조자, 유통, 계류중인 독점에 관한 문제 혹은 기타 제네릭 의약품 고유의 특성상의 변화에 의한 차이점을 제외하고 RLD와 동일한지를 확인하게 된다. 또한 라벨심사는 비슷한 음 또는 그렇게 들리는 의약품명, 읽기 쉬운 정도 또는 의약품명이 눈에 띄는 정도 혹은 강도와 같이 투약오류를 일으킬 수 있는 문제를 확인하고 해결하기 위해서 실시한다.
▣ 설비조사에 관한 요건
ANDA를 신고하면 해당 제네릭 의약품 제조자, 대량 의약품성분 제조자와 그 외 다른 외부 테스트 또는 포장 설비가 21 CFR 211의 규정에 요약된 current Good Manufacturing Practice(이하 cGMP)법규에 준수하여 운영되는지 알아보기 위해 시설 평가 의뢰서가 법무부서에 전송된다. 평가 요건에 목록화된 각각의 설비는 개별적으로 평가되고 신청에 대한 전반적인 평가는 법무부서에서 한다. 또한 승인전 상품 자체 조사는 신청서상의 데이터가 사실임을 확실히 하기 위해 실시될 수 있다.
▣ 화학/미생물학 심사
화학/미생물학 심사과정에서는 해당 제네릭 의약품이 통제된 조건하에서 재생가능한 방식으로 제조되는지 확인한다. 신청자의 제조 과정, 원료사양과 제어요건, 살균과정, 용기 및 밀폐 방식, 가속 및 상온 온도 안정성 데이터가 해당 의약품이 수용할 만한 방식으로 제조되고 있음을 입증하기 위해 심사된다.
▣ 화학/미생물학/라벨심사 통과
신청서상 화학/제조/제어, 미생물학 또는 라벨링과 관련해 정보가 부족하다면 팩스를 통해 이 사실을 신청자에게 알린다. 이 알림을 통해 신청자에게 부족한 사항에 대한 정보와 데이터를 요구하고 신청서를 수정 방식에 관한 규제상의 지침을 전달한다. 승인전 조사와 신청서상의 생물학적 동등성에 관한 사항뿐만 아니라 위에 언급한 사항이 충분하다고 판단되면 해당 신청건은 남은 승인절차를 진행하게 된다. 더 이상 미비사항 없이 모든 심사규칙에 의해 최종 행정상의 승인심사를 받은 후, 해당 신청건은 승인을 받을 수 있다. (ANDA 승인 참조)
▣ 생물학적 동등성 심사통과
생물학적 동등성 심사결론에서 신청서상에 생물학적 동등성 부분이 누락되었다고 판단되면 생물학적 동등성 부서는 생물학적 동등성 정보 누락에 관한 서신을 발부한다. 이 누락에 관한 서신은 누락에 대한 자세한 사항을 기재하고 이를 해결하기 위한 정보나 데이터를 요구한다. 또는 심사를 통해 신청자가 생물학적 동등성에 관한 요구사항을 만족스럽게 설명했다고 판단하면 생물학적 동등성에 관한 부서는 현재로서는 추가적인 의문사항이 없다는 점을 명기한 예비적인 정보서신을 발부할 것이다.
▣ 승인전 점검 통과
통과된 승인전 점검에 기반해서 법무부서로부터 만족한다라는 추천서는 승인전에 반드시 필요하다. 승인전 점검에서는 해당 신청건의 제조과정과 관련한 상품 자체 평가뿐 만 아니라 cGMP를 준수하는지 확인한다. 부적격 판정을 받게 된다면 승인장은 발부되지 않는다. 이 경우, 만족할 만한 재점검과 통과가능하다는 추천을 받을 때까지 승인이 연기 될 것이다.
전체댓글 0개
등록된 댓글이 없습니다.
| 인기기사 | 더보기 + |
-
1 메지온,AEPC 2026서 'JURVIGO' 3상 추가임상 인지도 확대 '전력' -
2 [약업분석] HLB그룹 이자비용 489억원…총차입금의존도 평균 27% -
3 [약업분석] HLB그룹 자기자본이익률 8곳 마이너스 -
4 [약업분석] 현대약품, 1Q 전 부문 ' 흑전'… 재무 건전성까지 질적 성장 -
5 코아스템켐온, 오송 공장 세포처리시설 허가 획득…첨단재생의료 사업 본격화 -
6 “왜 제약·바이오 공장은 일반 스마트팩토리로 부족한가” -
7 차백신연구소, 김병록 경영지배인 선임 -
8 프로티나, 미국 IDT와 MOU 체결... 차세대 항체 치료제 개발 가속 -
9 "체중감량 15% 장벽 넘은 GLP-1…대사질환 치료 ‘큰 파도’ 온다" -
10 제21회 경기약사학술대회 개막…AI 시대 약사 미래 역할 모색
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

세계 각국의 의약품 허가 및 관리제도<8>
- 기자
- 입력 2005-09-26 09:35 수정 최종수정 2006-09-05 17:27

Ⅰ. 미국 제네릭의약품 허가제도
미국 FDA는 1984년 Hatch-Waxman Act (Drug Price Competition and Patent Term Restoration Act)를 도입함으로써 제네릭 의약품 시장 규제에 큰 진보를 이루었다. Hatch-Waxman Act에서는 FDA에서 이미 승인받은 신약의 제네릭 의약품에 대하여 약식의 허가 절차 (Abbreviated New Drug Application; ANDA)를 적용하기로 하였다. 이에 해당하는 제네릭 의약품은 기존의 약과 활성성분, 용량, 강도, 복용경로, 사용조건이 모두 동일한 의약품이다. 이로써 오늘날 사용되고 있는 ANDA 절차가 생겨났고 이는 FDA의 의약품 평가 및 조사 센터 (CDER)와 제네릭 의약품국 (OGD)의 통합 보호 하에 관리되고 있다.
1. ANDA 절차
 |
▣ 신청자
신청자란 약식 신의약품 신청서 (abbreviated new drug application, ANDA)나 제네릭 의약품을 시장 출시하기 위해 FDA의 승인을 획득하기 위한 수정안 또는 추가정보를 제출한 자 (일반적으로 제약회사를 이름) 및 승인된 신청서 또는 약식 신청서를 지닌 자를 이른다.
▣ 제네릭의약품 신청서
제네릭 의약품은 신약 (FDA의 치료적 동일 성분 평가를 거친 승인된 의약품리스트에 나온 의약품 (reference listed drug, 이하 RLD))과 복용량, 강도, 투여경로, 품질, 효과적 특징과 사용 의도면에서 동일하다.
"ANDA"는 "Abbreviated New Drug Application"의 약자이다. FDA의 Center for Drug Evaluation and Research(이하 CDER), Office of Generic Drugs(이하 OGD)에 제출시 제네릭 의약품에 대한 조사와 최종승인을 위한 자료를 포함한다. 일단 승인이 되면 신청자는 특허보호에 관한 문제 및 RLD와 연관된 독점권 문제가 해결이 되면 해당 제네릭 의약품을 제조, 출시할 수 있다.
제네릭 의약품 신청서는 일반적으로 안전성과 효능을 입증하기 위한 동물 및 인간 임상 데이터가 필요하지 않기 때문에 약식이라는 이름이 붙는다. 이러한 조건은 FDA가 승인한 의약품의 첫 상품인 신약이 받은 승인에 근거하여 성립된다.
▣ 통과 여부
신청서는 효과적이고 빠르게 의약품심사가 진행될 수 있도록 충분한 정보를 갖춰야 한다. 신청서를 받으면 OGD의 Regulatory Support Branch의 프로젝트 매니저는 신청서가 완벽하게 작성되었고 통과 가능한지에 대해 신고전 평가를 실시한다. 이 초기 의약품 심사에서 모든 필요한 사항을 포함하고 있다고 증명이 되면 심사를 받을 수 있고 신고날짜를 확인하는 "승인장"이 신청자에게 발송된다.
신청서가 생물학적 동등성 신고를 하기에 적절하다고 판단나면 화학/미생물학 및 라벨부착 심사가 시작된다.
▣ 신고거부장 발부
신청자가 한두 개의 중요한 사항을 빠뜨린다면 "신고거부장"이 신청자에게 발송된다. 이 신고거부장은 누락된 사항을 알려주고 이 사항을 보충할 때까지 신청 신고가 이루어지지 않는다는 점을 신청자에게 알린다. 신청자가 이 필요한 데이터를 제공해서 접수할 수 있고 완벽하다고 판단이 될 때까지 신청서 심사는 중단된다.
▣ 생물학적 동등성 심사
생물학적 동등성 심사과정에서는 해당 제네릭 의약품의 활성 성분이 체내에 흡수되는 속도와 양이 모두 RLD와 비교했을 때 설정된 범위안에 해당된다는 점에 근거해 RLD와 같은 생물학적 동등성을 지닌다는 점을 입증하게 된다.
FDA는 신청자로 하여금 생물학적 동등성을 입증하기 위한 상세한 정보를 제공하도록 한다. 신청자는 생체이용률 (활성성분 또는 활성 성분 일부분이 의약품 사용으로 신체내 흡수되어 효능이 일어나는 지점에 머무르는 속도와 양이 다음과 같은 데이터 제출로 증명될 수 있는 특정 의약품에 대해서는 인체내 생물학적 동등성 실험을 실시하지 않도록 하는 예외조항을 요구할 수 있다. 1) 성분이 동일한 구강용 물약, 주입 가능한 의약품, 안약류와 같이 생체이용률이 자명한 상품에 대한 성분비교 자료 2) 비교용출자료
하지만 해당 제네릭 의약품과 브랜드 의약품간의 성분 흡수속도와 양을 비교하는 인체내 생물학적 동등성 시험은 대다수의 정제와 캡슐제에는 필수적이다. 특정 상품에 대해서는 임상적 종료시점에 기반한 효능비교에 대한 상세한 평가가 필요할 수 있다.
▣ 라벨 심사
라벨심사과정에서는 해당 제네릭 의약품 라벨링 (포장된 삽입물, 삽입물 용기, 포장라벨, 환자용 참조정보)이 제조자, 유통, 계류중인 독점에 관한 문제 혹은 기타 제네릭 의약품 고유의 특성상의 변화에 의한 차이점을 제외하고 RLD와 동일한지를 확인하게 된다. 또한 라벨심사는 비슷한 음 또는 그렇게 들리는 의약품명, 읽기 쉬운 정도 또는 의약품명이 눈에 띄는 정도 혹은 강도와 같이 투약오류를 일으킬 수 있는 문제를 확인하고 해결하기 위해서 실시한다.
▣ 설비조사에 관한 요건
ANDA를 신고하면 해당 제네릭 의약품 제조자, 대량 의약품성분 제조자와 그 외 다른 외부 테스트 또는 포장 설비가 21 CFR 211의 규정에 요약된 current Good Manufacturing Practice(이하 cGMP)법규에 준수하여 운영되는지 알아보기 위해 시설 평가 의뢰서가 법무부서에 전송된다. 평가 요건에 목록화된 각각의 설비는 개별적으로 평가되고 신청에 대한 전반적인 평가는 법무부서에서 한다. 또한 승인전 상품 자체 조사는 신청서상의 데이터가 사실임을 확실히 하기 위해 실시될 수 있다.
▣ 화학/미생물학 심사
화학/미생물학 심사과정에서는 해당 제네릭 의약품이 통제된 조건하에서 재생가능한 방식으로 제조되는지 확인한다. 신청자의 제조 과정, 원료사양과 제어요건, 살균과정, 용기 및 밀폐 방식, 가속 및 상온 온도 안정성 데이터가 해당 의약품이 수용할 만한 방식으로 제조되고 있음을 입증하기 위해 심사된다.
▣ 화학/미생물학/라벨심사 통과
신청서상 화학/제조/제어, 미생물학 또는 라벨링과 관련해 정보가 부족하다면 팩스를 통해 이 사실을 신청자에게 알린다. 이 알림을 통해 신청자에게 부족한 사항에 대한 정보와 데이터를 요구하고 신청서를 수정 방식에 관한 규제상의 지침을 전달한다. 승인전 조사와 신청서상의 생물학적 동등성에 관한 사항뿐만 아니라 위에 언급한 사항이 충분하다고 판단되면 해당 신청건은 남은 승인절차를 진행하게 된다. 더 이상 미비사항 없이 모든 심사규칙에 의해 최종 행정상의 승인심사를 받은 후, 해당 신청건은 승인을 받을 수 있다. (ANDA 승인 참조)
▣ 생물학적 동등성 심사통과
생물학적 동등성 심사결론에서 신청서상에 생물학적 동등성 부분이 누락되었다고 판단되면 생물학적 동등성 부서는 생물학적 동등성 정보 누락에 관한 서신을 발부한다. 이 누락에 관한 서신은 누락에 대한 자세한 사항을 기재하고 이를 해결하기 위한 정보나 데이터를 요구한다. 또는 심사를 통해 신청자가 생물학적 동등성에 관한 요구사항을 만족스럽게 설명했다고 판단하면 생물학적 동등성에 관한 부서는 현재로서는 추가적인 의문사항이 없다는 점을 명기한 예비적인 정보서신을 발부할 것이다.
▣ 승인전 점검 통과
통과된 승인전 점검에 기반해서 법무부서로부터 만족한다라는 추천서는 승인전에 반드시 필요하다. 승인전 점검에서는 해당 신청건의 제조과정과 관련한 상품 자체 평가뿐 만 아니라 cGMP를 준수하는지 확인한다. 부적격 판정을 받게 된다면 승인장은 발부되지 않는다. 이 경우, 만족할 만한 재점검과 통과가능하다는 추천을 받을 때까지 승인이 연기 될 것이다.
Copyright © Yakup.com All rights reserved.
약업신문 의 모든 컨텐츠(기사)는 저작권법의 보호를 받습니다.
무단 전재·복사·배포 등을 금지합니다.
무단 전재·복사·배포 등을 금지합니다.



