SMA 치료제 스핀라자·에브리스디, 위험분담제 급여범위 확대
2026년 첫 약제급여평가위원회에서 항암·희귀질환 치료제의 급여 향방이 엇갈렸다.
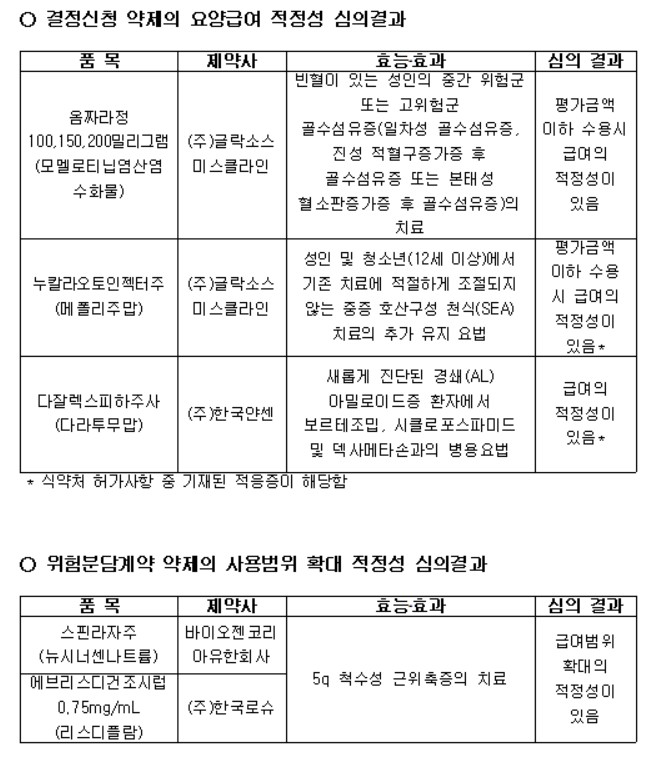
경쇄(AL) 아밀로이드증 치료제 다잘렉스는 급여 적정성을 인정받은 반면, GSK의 옴짜라와 누칼라는 평가금액 이하 수용을 전제로 한 조건부 통과에 그쳤다.
건강보험심사평가원은 15일 2026년 제1차 약제급여평가위원회 심의 결과를 공개했다. 이번 약평위는 지난해 9월 기존 위원 임기 만료 이후 새로 구성된 위원회가 처음 연 회의다.
△다잘렉스, AL 아밀로이드증서 급여 적정성 인정
한국얀센의 다잘렉스 피하주사(다라투무맙)는 ‘새롭게 진단된 경쇄(AL) 아밀로이드증 환자에서 보르테조밉·시클로포스파미드·덱사메타손과의 병용요법’에 대해 급여 적정성을 인정받았다.
다잘렉스는 지난해 7월 암질환심의위원회를 통과한 이후 이번 약평위에서도 긍정적인 평가를 받으며 급여 적용을 향한 절차를 한 단계 더 밟게 됐다.
경쇄 아밀로이드증은 극히 드문 희귀질환으로, 그동안 다발골수종 치료제가 제한적으로 활용돼 왔으나, 다잘렉스가 해당 적응증을 확보하면서 글로벌 치료 환경에서는 표준요법으로 빠르게 자리 잡고 있다.
△옴짜라·누칼라, ‘평가금액 이하 수용’ 조건 달려
글락소스미스클라인의 골수섬유증 치료제 ‘옴짜라정(모멜로티닙염산염수화물)’과 중증 호산구성 천식 치료제 ‘누칼라 오토인젝터주(메폴리주맙)’는 조건부로 급여 적정성을 인정받았다.
옴짜라는 ‘빈혈이 있는 성인의 중간 위험군 또는 고위험군 골수섬유증’ 치료를 적응증으로 심의를 받았으며, 약평위는 제약사가 평가금액 이하를 수용할 경우 급여의 적정성이 있다고 판단했다.
누칼라 오토인젝터주 역시 ‘성인 및 청소년(12세 이상)에서 기존 치료로 적절히 조절되지 않는 중증 호산구성 천식의 추가 유지요법’에 대해 평가금액 이하 수용을 전제로 한 급여 적정성이 인정됐다.
두 약제 모두 임상적 필요성은 인정됐으나, 재정 영향과 약가 수준을 고려한 조건이 명확히 달린 셈이다.
△SMA 치료제 2종, 위험분담제 급여범위 확대
이번 약평위에서는 위험분담계약 약제의 사용범위 확대에 대한 심의 결과도 함께 공개됐다.
바이오젠코리아의 스핀라자주(뉴시너센나트륨)와 한국로슈의 에브리스디건조시럽(리스디플람)은 모두 ‘5q 척수성 근위축증(SMA)의 치료’에 대해 급여범위 확대의 적정성을 인정받았다.
두 약제는 이미 위험분담계약(RSA) 체계 하에 급여가 이뤄지고 있는 만큼, 이번 결정은 치료 접근성 확대 측면에서 의미가 있다는 평가다.
한편, 약평위를 통과한 약제는 향후 국민건강보험공단과 최대 60일간의 약가 협상을 거친 뒤, 보건복지부 건강보험정책심의위원회에서 최종 급여 여부가 결정된다.
| 인기기사 | 더보기 + |
-
1 고령화 시대의 시한폭탄 ‘심방세동’… 국내 제약사, 항응고제 시장 정조준 -
2 초고령사회 심방세동 관리, 웨어러블 심전도 역할 확대 -
3 K-뷰티, 미국 세포라·울타 잇단 진입 -
4 20·30대 5년 새 40% 증가…궤양성 대장염 치료 목표가 달라졌다 -
5 노보노디스크, 미국 외 GLP-1 제제 제조역량 ↑ -
6 5년간 두 배 성장한 릭시아나…심방세동 항응고 시장 판도 변화 -
7 로슈, 한국 바이오헬스에 7,100억 베팅… ‘아시아 임상 허브’ 도약 정조준 -
8 노보, ‘세계 비만의 날’ 맞아 보건의료 전문가 좌담회 개최 -
9 한미그룹, , 故 임성기 선대회장 철학 담은 동판 조형물 제막식 거행 -
10 티카로스, 208억원 시리즈D 유치 성공…"CAR-T 임상 가속"
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 전하연 기자 hayeon@yakup.com
- 입력 2026.01.16 06:00 수정 2026.01.16 06:01

2026년 첫 약제급여평가위원회에서 항암·희귀질환 치료제의 급여 향방이 엇갈렸다.
경쇄(AL) 아밀로이드증 치료제 다잘렉스는 급여 적정성을 인정받은 반면, GSK의 옴짜라와 누칼라는 평가금액 이하 수용을 전제로 한 조건부 통과에 그쳤다.
건강보험심사평가원은 15일 2026년 제1차 약제급여평가위원회 심의 결과를 공개했다. 이번 약평위는 지난해 9월 기존 위원 임기 만료 이후 새로 구성된 위원회가 처음 연 회의다.
△다잘렉스, AL 아밀로이드증서 급여 적정성 인정
한국얀센의 다잘렉스 피하주사(다라투무맙)는 ‘새롭게 진단된 경쇄(AL) 아밀로이드증 환자에서 보르테조밉·시클로포스파미드·덱사메타손과의 병용요법’에 대해 급여 적정성을 인정받았다.
다잘렉스는 지난해 7월 암질환심의위원회를 통과한 이후 이번 약평위에서도 긍정적인 평가를 받으며 급여 적용을 향한 절차를 한 단계 더 밟게 됐다.
경쇄 아밀로이드증은 극히 드문 희귀질환으로, 그동안 다발골수종 치료제가 제한적으로 활용돼 왔으나, 다잘렉스가 해당 적응증을 확보하면서 글로벌 치료 환경에서는 표준요법으로 빠르게 자리 잡고 있다.
△옴짜라·누칼라, ‘평가금액 이하 수용’ 조건 달려
글락소스미스클라인의 골수섬유증 치료제 ‘옴짜라정(모멜로티닙염산염수화물)’과 중증 호산구성 천식 치료제 ‘누칼라 오토인젝터주(메폴리주맙)’는 조건부로 급여 적정성을 인정받았다.
옴짜라는 ‘빈혈이 있는 성인의 중간 위험군 또는 고위험군 골수섬유증’ 치료를 적응증으로 심의를 받았으며, 약평위는 제약사가 평가금액 이하를 수용할 경우 급여의 적정성이 있다고 판단했다.
누칼라 오토인젝터주 역시 ‘성인 및 청소년(12세 이상)에서 기존 치료로 적절히 조절되지 않는 중증 호산구성 천식의 추가 유지요법’에 대해 평가금액 이하 수용을 전제로 한 급여 적정성이 인정됐다.
두 약제 모두 임상적 필요성은 인정됐으나, 재정 영향과 약가 수준을 고려한 조건이 명확히 달린 셈이다.
△SMA 치료제 2종, 위험분담제 급여범위 확대
이번 약평위에서는 위험분담계약 약제의 사용범위 확대에 대한 심의 결과도 함께 공개됐다.
바이오젠코리아의 스핀라자주(뉴시너센나트륨)와 한국로슈의 에브리스디건조시럽(리스디플람)은 모두 ‘5q 척수성 근위축증(SMA)의 치료’에 대해 급여범위 확대의 적정성을 인정받았다.
두 약제는 이미 위험분담계약(RSA) 체계 하에 급여가 이뤄지고 있는 만큼, 이번 결정은 치료 접근성 확대 측면에서 의미가 있다는 평가다.
한편, 약평위를 통과한 약제는 향후 국민건강보험공단과 최대 60일간의 약가 협상을 거친 뒤, 보건복지부 건강보험정책심의위원회에서 최종 급여 여부가 결정된다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
