한국·미국·중국·일본 등 핵심 시장 특허 포트폴리오 구축 완료
 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
마이크로바이옴 신약 개발 기업 고바이오랩(대표이사 고광표)은 건강기능식품 자회사 위바이옴이 경구용 섭취가 가능한 대사증후군 개선 기능성 균주 Akkermansia muciniphila(아커만시아 뮤시니필라) KBL983(이하 ‘KBL983)에 대해 미국 자체검증 GRAS (Self-Affirmed Generally Recognized As Safe)를 획득했다고 24일 밝혔다.
KBL983은 지난 10여 년간 당뇨·비만·지방간 등 주요 대사질환 개선 효과 및 기전 연구를 마친 고바이오랩 핵심 균주로, 특히 대사 관련 호르몬인 글루카곤 유사 펩타이드(GLP-1) 발현을 유도하고 갈색지방 활성을 증가시키는 효과가 있다. 고바이오랩은 국가신약개발사업을 통해 장 점막 강화, 산화스트레스 보호 효과 및 장내 미생물 불균형 개선 효과 등을 갖춘 삼제병용 경구형 생균 비만치료제를 성공적으로 개발하였으며, 글로벌 제약사와 파트너십 발굴 등 후속 사업화 논의를 진행하고 있다.
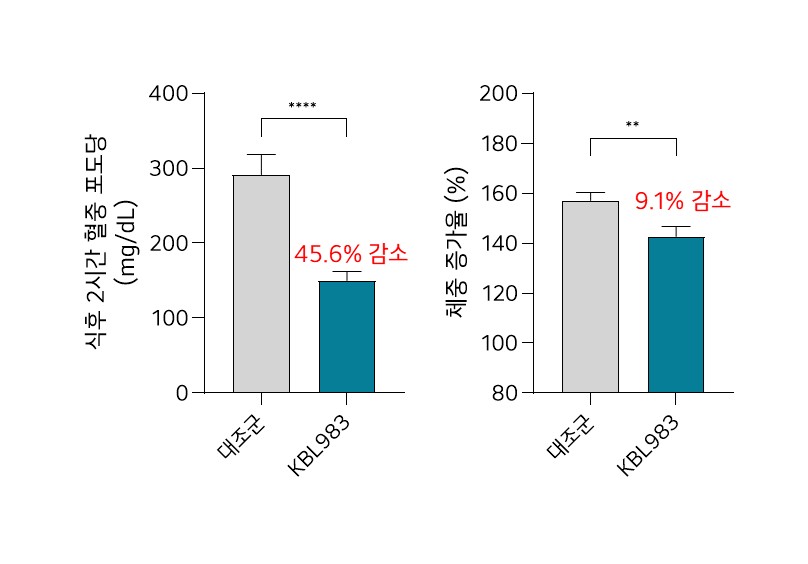
위바이옴은 KBL983의 활용성을 식품 등으로 확장하기 위해, 국가식품클러스터에 위치한 자체 GMP 공장을 활용해 안정성이 높은 열처리사균체로 개발을 앞장서왔다. 위바이옴-한국식품산업클러스터진흥원-전북대학교병원 유효성평가센터 공동연구진은 KBL983 열처리 사균체를 제2형 당뇨 동물 모델에서 10주 투여한 후 유의한 식후 2시간 혈당 감소(대조군 대비 54.4%, p < 0.0001) 및 체중 증가 억제(대조군 대비 9.1%, p < 0.01) 효능을 확인했다<하기 그림 참조>. 공동 연구진은 해당 결과를 국제학술지에 게재할 예정이다.
자체검증 GRAS는 미국 FDA에서 인정한 영양 및 독성학 분야의 전문가들이 ▲안전성 자료 ▲독성시험 결과 ▲섭취 이력 ▲과학적 문헌 등을 종합적으로 검토해 인체 섭취에 안전하다고 판단할 경우 부여되는 인증이다. 특히 이번 KBL983 열처리사균체 자체검증 GRAS 획득은 미국 시장에서 상업적 활용이 가능한 안전성 요건을 충족했다는 점에서, 글로벌 비만·대사질환 시장 진출을 위한 실질적인 상업화 관문을 통과했다는 의미를 갖는다.
특히 고바이오랩은 이미 KBL983에 대한 대한민국, 미국, 중국, 일본, 캐나다 등 핵심 시장들에 대한 지식재산권을 확보하는 등 글로벌 독점 권리망을 완성하고 있다. 열처리사균체는 다양한 제형에도 높은 안정성을 가져 치료제 및 건강기능식품 등 다양한 산업분야에 활용하기 적합하다. 향후 위바이옴은 최적화한 사균화 공정을 바탕으로 바탕으로 KBL983 열처리사균체 대량 양산에 나설 계획이다.
위바이옴 관계자는 “‘KBL983 열처리사균체는 충분한 과학적 근거, 뛰어난 안전성-안정성, 배타적인 글로벌 권리 등 삼박자를 모두 갖춘 대사증후군 개선 핵심 소재”라며 “특히 본 자체검증 GRAS 취득을 바탕으로 본격적인 글로벌 시장 진출에 주력할 것”이라며 기대를 감추지 않았다.
한편, 최근 노보노디스크 경구용 GLP-1 비만 치료제가 미국 FDA 승인을 획득하며, 주사제 중심이던 비만 치료 시장이 경구용 제형으로 빠르게 확장되고 있다.
업계에서는 복약 편의성을 갖춘 경구용 솔루션이 비만을 포함한 대사질환 관리 시장의 새로운 표준으로 자리 잡을 것으로 보고 있으며, 이러한 흐름 속에서 위바이옴 KBL983 열처리사균체도 경구 섭취 기반 대사질환 관리 소재로서 글로벌 시장에서 활용 가능성을 확대해 나가고 있다.
| 인기기사 | 더보기 + |
-
1 빗장 풀린 비대면 진료... 제약업계, ‘디지털 헬스케어’ 대전환 서막 -
2 2025년 글로벌 제약업계 10대 뉴스 -
3 [2025년 결산 ] 2025, GLP-1 이후 준비한 해…한국이 마주한 마운자로 -
4 [2025년 결산]"동물실험 이후를 준비하라" 오가노이드·신규접근법의 시간 -
5 2025년 글로벌 화장품업계 10대 뉴스 -
6 엘앤씨바이오,휴메딕스와 주식 스왑 통한 유상증자 -
7 유바이오로직스, mRNA백신 'mCOV' 임상1상 IND 승인 -
8 “이제는 시험이 아니라 공정이다” 대용량 수액제 GMP의 구조적 전환 -
9 [2025년 결산] 저마진 고착에 ‘비용·규제·플랫폼’ 겹악재…유통업계 생존 압박 -
10 대봉그룹 송도 B&H Plex, ‘통합 개발 플랫폼’ 시대 연다
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 이권구 기자 kwon9@yakup.com
- 입력 2025.12.24 09:04 수정 2025.12.24 09:07

마이크로바이옴 신약 개발 기업 고바이오랩(대표이사 고광표)은 건강기능식품 자회사 위바이옴이 경구용 섭취가 가능한 대사증후군 개선 기능성 균주 Akkermansia muciniphila(아커만시아 뮤시니필라) KBL983(이하 ‘KBL983)에 대해 미국 자체검증 GRAS (Self-Affirmed Generally Recognized As Safe)를 획득했다고 24일 밝혔다.
KBL983은 지난 10여 년간 당뇨·비만·지방간 등 주요 대사질환 개선 효과 및 기전 연구를 마친 고바이오랩 핵심 균주로, 특히 대사 관련 호르몬인 글루카곤 유사 펩타이드(GLP-1) 발현을 유도하고 갈색지방 활성을 증가시키는 효과가 있다. 고바이오랩은 국가신약개발사업을 통해 장 점막 강화, 산화스트레스 보호 효과 및 장내 미생물 불균형 개선 효과 등을 갖춘 삼제병용 경구형 생균 비만치료제를 성공적으로 개발하였으며, 글로벌 제약사와 파트너십 발굴 등 후속 사업화 논의를 진행하고 있다.
위바이옴은 KBL983의 활용성을 식품 등으로 확장하기 위해, 국가식품클러스터에 위치한 자체 GMP 공장을 활용해 안정성이 높은 열처리사균체로 개발을 앞장서왔다. 위바이옴-한국식품산업클러스터진흥원-전북대학교병원 유효성평가센터 공동연구진은 KBL983 열처리 사균체를 제2형 당뇨 동물 모델에서 10주 투여한 후 유의한 식후 2시간 혈당 감소(대조군 대비 54.4%, p < 0.0001) 및 체중 증가 억제(대조군 대비 9.1%, p < 0.01) 효능을 확인했다<하기 그림 참조>. 공동 연구진은 해당 결과를 국제학술지에 게재할 예정이다.
자체검증 GRAS는 미국 FDA에서 인정한 영양 및 독성학 분야의 전문가들이 ▲안전성 자료 ▲독성시험 결과 ▲섭취 이력 ▲과학적 문헌 등을 종합적으로 검토해 인체 섭취에 안전하다고 판단할 경우 부여되는 인증이다. 특히 이번 KBL983 열처리사균체 자체검증 GRAS 획득은 미국 시장에서 상업적 활용이 가능한 안전성 요건을 충족했다는 점에서, 글로벌 비만·대사질환 시장 진출을 위한 실질적인 상업화 관문을 통과했다는 의미를 갖는다.
특히 고바이오랩은 이미 KBL983에 대한 대한민국, 미국, 중국, 일본, 캐나다 등 핵심 시장들에 대한 지식재산권을 확보하는 등 글로벌 독점 권리망을 완성하고 있다. 열처리사균체는 다양한 제형에도 높은 안정성을 가져 치료제 및 건강기능식품 등 다양한 산업분야에 활용하기 적합하다. 향후 위바이옴은 최적화한 사균화 공정을 바탕으로 바탕으로 KBL983 열처리사균체 대량 양산에 나설 계획이다.
위바이옴 관계자는 “‘KBL983 열처리사균체는 충분한 과학적 근거, 뛰어난 안전성-안정성, 배타적인 글로벌 권리 등 삼박자를 모두 갖춘 대사증후군 개선 핵심 소재”라며 “특히 본 자체검증 GRAS 취득을 바탕으로 본격적인 글로벌 시장 진출에 주력할 것”이라며 기대를 감추지 않았다.
한편, 최근 노보노디스크 경구용 GLP-1 비만 치료제가 미국 FDA 승인을 획득하며, 주사제 중심이던 비만 치료 시장이 경구용 제형으로 빠르게 확장되고 있다.
업계에서는 복약 편의성을 갖춘 경구용 솔루션이 비만을 포함한 대사질환 관리 시장의 새로운 표준으로 자리 잡을 것으로 보고 있으며, 이러한 흐름 속에서 위바이옴 KBL983 열처리사균체도 경구 섭취 기반 대사질환 관리 소재로서 글로벌 시장에서 활용 가능성을 확대해 나가고 있다.
무단 전재·복사·배포 등을 금지합니다.



