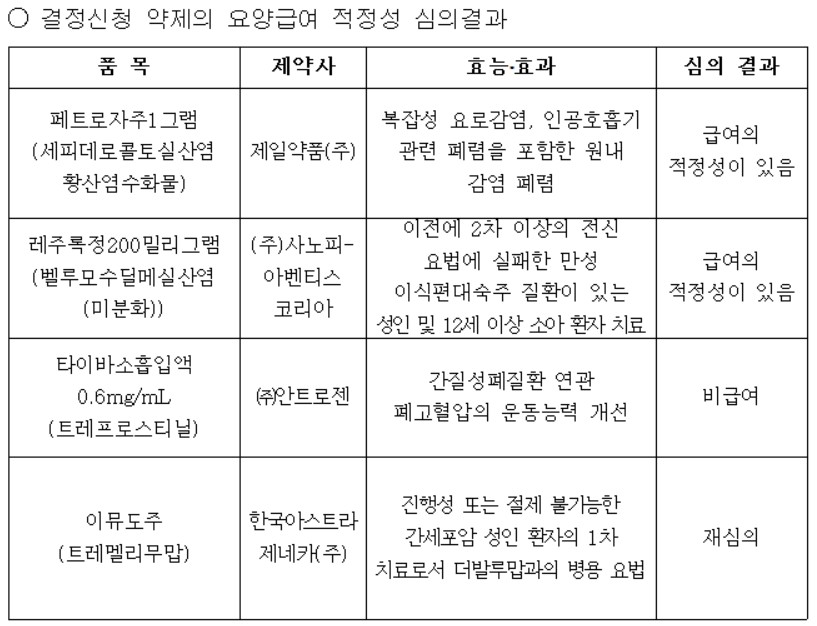
타이바소 비급여·이뮤도·임핀지는 재심의
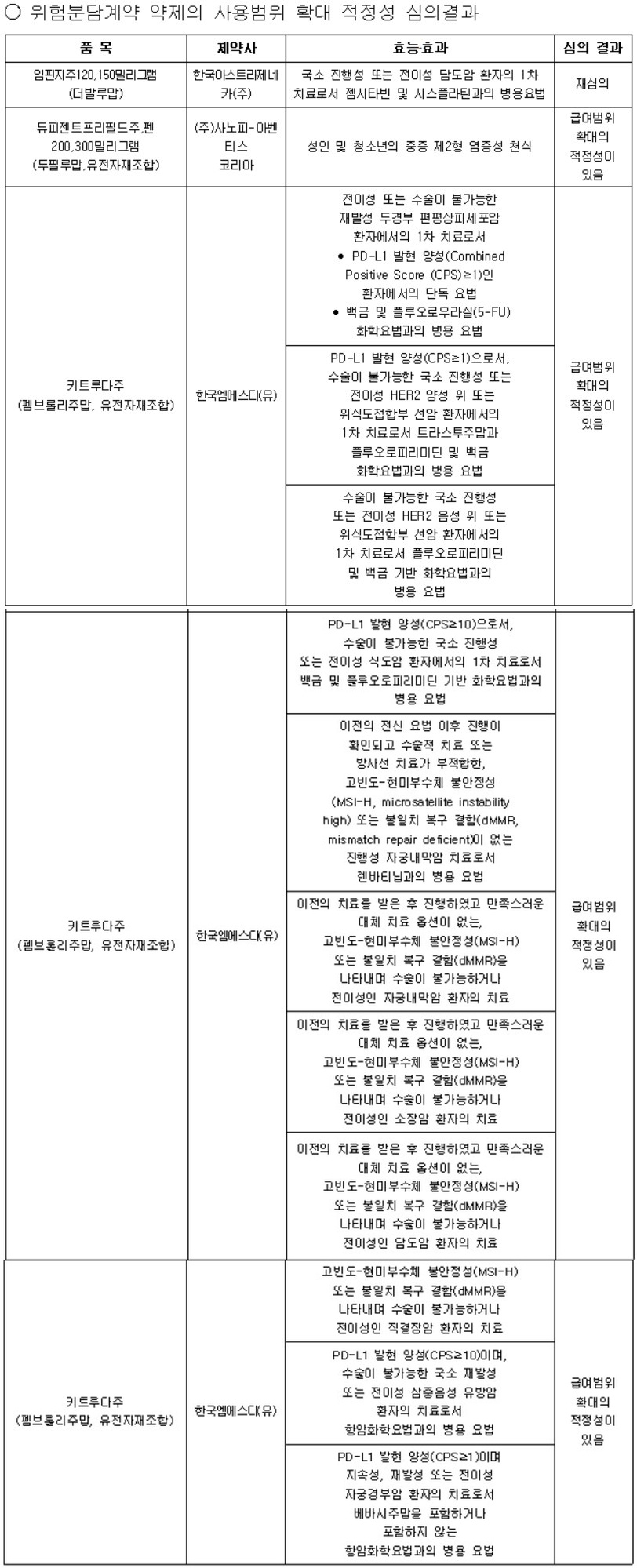
건강보험심사평가원 제9차 약제급여평가위원회가 4일 회의를 열고 한국MSD의 ‘키트루다(펨브롤리주맙)’ 11개 적응증의 급여범위 확대 적정성을 인정했다.
사노피-아벤티스코리아의 ‘듀피젠트(두필루맙)’는 중증 제2형 염증성 천식에서 급여 확대를, 제일약품의 ‘페트로자주(세피데로콜토실산염황산염수화물)’와 ‘레주록정(벨루모수딜메실산염)’도 각각 감염·이식 관련 질환에서 급여 적정성을 확보했다.
반면 안트로젠의 ‘타이바소흡입액(트레프로스티닐)’은 비급여로 결론났으며, 아스트라제네카의 ‘이뮤도주(트레멜리무맙)’와 ‘임핀지주(더발루맙)’는 재심의로 판단이 유보됐다.
키트루다, 3년 연속 확대 신청 끝에 11개 적응증 통과
키트루다는 2023년 13개, 2024년 4개 적응증에 대해 급여 확대를 신청해 왔으며, 올해까지 총 17개 적응증이 검토 대상에 올랐다. 지난 2월 중증암질환심의위원회에서 11개 적응증이 우선 급여기준을 마련한 데 이어 이번 약평위 심의를 통해 공식 확대의 길이 열렸다.
이번에 통과된 적응증은 △두경부암·위식도암군(PD-L1 양성 두경부 편평상피세포암, HER2 양성·음성 위암 및 위식도접합부 선암, PD-L1 CPS≥10 식도암) △MSI-H/dMMR 암종군(자궁내막암, 소장암, 담도암, 직결장암) △여성암군(삼중음성 유방암, 자궁경부암)으로, 1차 병용요법부터 고빈도 불일치 복구 결함 암종까지 적용 범위가 넓어졌다. 이를 통해 국내 면역항암제 치료 영역이 크게 확장될 전망이다.
듀피젠트·페트로자·레주록도 긍정 평가
듀피젠트는 성인·청소년 중증 제2형 염증성 천식에서 급여 확대 적정성을 인정받아 호흡기 면역질환 치료 옵션이 강화됐다. 페트로자주는 복잡성 요로감염·인공호흡기 관련 폐렴 등 원내감염성 폐렴에, 레주록정은 2차 이상 전신요법에 실패한 만성 이식편대숙주질환(cGVHD)에 대해 각각 급여 적정성이 인정됐다.
타이바소 비급여, 이뮤도·임핀지 재심의
한편, 타이바소흡입액은 간질성 폐질환 연관 폐고혈압 환자의 운동능력 개선 효과에 대해 비급여로 결정됐다. 이뮤도주는 간세포암 1차 치료, 임핀지는 담도암 1차 치료에서 신청됐으나 모두 재심의 결론이 내려졌다.
| 인기기사 | 더보기 + |
-
1 다이이찌산쿄, ADC 생체지표 발굴 AI 접목 제휴 -
2 상장 제약·바이오 2025년 누적 평균 순이익 코스피 917억원·코스닥 175억원 -
3 서울시유통협회, 대웅 거점도매 전면 투쟁 선언 -
4 제2의 키트루다, 새 타깃 아닌 '조합·구조 설계'에서 나온다 -
5 EDGC, 최대주주 '해밀리'로 변경 -
6 에스엘티지, AI 검사 기반 통합장비 'PRINS25'…"인쇄·검사 올인원" -
7 제일약품, '상품' 비중 줄이고 내실 잡았다… 신약 '자큐보' 효과로 수익성 대폭 개선 -
8 넥스트바이오메디컬,혈관색전 제품 'Nexsphere-F™' 독점 판권 계약 -
9 알지노믹스-서지넥스, LNP 기반 RNA 유전자 신약 공동개발 나선다 -
10 B형·C형 간염 시장 엇갈린 흐름…길리어드 전략 통했다
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 전하연 기자 hayeon@yakup.com
- 입력 2025.09.05 06:00 수정 2025.09.05 06:01


건강보험심사평가원 제9차 약제급여평가위원회가 4일 회의를 열고 한국MSD의 ‘키트루다(펨브롤리주맙)’ 11개 적응증의 급여범위 확대 적정성을 인정했다.
사노피-아벤티스코리아의 ‘듀피젠트(두필루맙)’는 중증 제2형 염증성 천식에서 급여 확대를, 제일약품의 ‘페트로자주(세피데로콜토실산염황산염수화물)’와 ‘레주록정(벨루모수딜메실산염)’도 각각 감염·이식 관련 질환에서 급여 적정성을 확보했다.
반면 안트로젠의 ‘타이바소흡입액(트레프로스티닐)’은 비급여로 결론났으며, 아스트라제네카의 ‘이뮤도주(트레멜리무맙)’와 ‘임핀지주(더발루맙)’는 재심의로 판단이 유보됐다.
키트루다, 3년 연속 확대 신청 끝에 11개 적응증 통과
키트루다는 2023년 13개, 2024년 4개 적응증에 대해 급여 확대를 신청해 왔으며, 올해까지 총 17개 적응증이 검토 대상에 올랐다. 지난 2월 중증암질환심의위원회에서 11개 적응증이 우선 급여기준을 마련한 데 이어 이번 약평위 심의를 통해 공식 확대의 길이 열렸다.
이번에 통과된 적응증은 △두경부암·위식도암군(PD-L1 양성 두경부 편평상피세포암, HER2 양성·음성 위암 및 위식도접합부 선암, PD-L1 CPS≥10 식도암) △MSI-H/dMMR 암종군(자궁내막암, 소장암, 담도암, 직결장암) △여성암군(삼중음성 유방암, 자궁경부암)으로, 1차 병용요법부터 고빈도 불일치 복구 결함 암종까지 적용 범위가 넓어졌다. 이를 통해 국내 면역항암제 치료 영역이 크게 확장될 전망이다.
듀피젠트·페트로자·레주록도 긍정 평가
듀피젠트는 성인·청소년 중증 제2형 염증성 천식에서 급여 확대 적정성을 인정받아 호흡기 면역질환 치료 옵션이 강화됐다. 페트로자주는 복잡성 요로감염·인공호흡기 관련 폐렴 등 원내감염성 폐렴에, 레주록정은 2차 이상 전신요법에 실패한 만성 이식편대숙주질환(cGVHD)에 대해 각각 급여 적정성이 인정됐다.
타이바소 비급여, 이뮤도·임핀지 재심의
한편, 타이바소흡입액은 간질성 폐질환 연관 폐고혈압 환자의 운동능력 개선 효과에 대해 비급여로 결정됐다. 이뮤도주는 간세포암 1차 치료, 임핀지는 담도암 1차 치료에서 신청됐으나 모두 재심의 결론이 내려졌다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
