글로벌 규제 맞는 약물감시 전략 수립해 고객사의 규제 대응 최적화

신약개발의 마지막 관문인 임상시험, 그 신뢰성을 보증하는 품질보증. 이 중요한 과정에서 QVIS(큐앤비스)는 보이지 않는 ‘파수꾼’ 역할을 수행하며, 국내 제약바이오 산업이 글로벌 시장에서 경쟁력을 갖추는 데 핵심적인 역할을 하고 있다.
QVIS는 글로벌 수준의 임상시험 품질보증(Quality Management) 및 약물감시(Pharmacovigilance) 서비스를 제공하며 2014년 8월 설립 이후 꾸준한 성장을 이어왔다. 품질보증 전문기업으로는 국내 최초로 설립됐다. QVIS는 출범 이후 글로벌 수준의 품질보증 시스템을 구축하며 국내외 제약바이오 업계에서 확고한 입지를 다져왔다.
QVIS 현수미 대표는 국내 임상시험 품질보증 및 약물감시 분야에서 20년 이상의 경력을 쌓아온 전문가다. 현 대표는 숙명여자대학교 약학대학 제약학과에서 학사 및 석사 학위를 취득한 후, 성균관대학교 약학대학에서 약학 박사 학위를 받았다.
현 대표는 LG생명과학 임상개발팀, GSK Biological 임상개발팀, C&R Research 품질보증부서에서 다양한 실무 경험을 쌓으며 임상시험 품질보증 및 규제 대응 역량을 키웠다. 또한 Pan-Asia Pacific Clinical Research Association에서 Regional Director로 활동하며 아시아·태평양 지역의 임상시험 품질관리와 글로벌 규제 대응을 주도했다.
현 대표는 미국 Registered Quality Assurance Professional(공인 품질보증 전문가)로서 국내외 제약바이오 기업이 국제 기준을 준수하도록 돕는 데 앞장서고 있다.
2014년부터 약 800건 이상 임상 품질 점검 수행…28%는 해외 임상 글로벌 점검
QVIS는 국내 및 해외 제약사, 바이오텍, CRO를 대상으로 국제의약품규제조화위원회(ICH-GCP) 및 각국 규제 지침에 부합하는 맞춤형 품질보증 서비스를 제공한다. 의약품뿐만 아니라 의료기기, 첨단재생의료, 디지털치료제 등 다양한 치료 분야에서도 품질보증과 약물감시 업무를 수행한다. 특히 한국을 넘어 중국, 일본, 동남아, 미국, 유럽 등 글로벌에서도 활약 중이다.
QVIS는 2020년부터 2024년까지 식품의약품안전처가 승인한 국내 3상 임상시험의 약 49.8%에 대해 품질 점검을 수행했다. 이는 QVIS의 높은 위상을 증명한다. 국내 CRO 업계에서도 독보적인 성과로, QVIS는 임상시험의 신뢰성과 품질 향상을 위한 필수적인 역할을 수행하고 있다.
글로벌 품질보증 분야에서도 QVIS 영향력은 점점 커지고 있다. 영국 ADAMAS Consulting, ZigZag Associate를 비롯해, 미국 The FDA Group, G&L Scientific, Quality Systems International 등 해외 유수의 품질보증 컨설팅 및 CRO 업체들과 포괄적 협력계약(Mutual Service Agreement)을 체결, 글로벌 파트너십을 확대했다.
이러한 네트워크와 파트너십를 활용해 아시아 지역의 품질 점검은 QVIS가, 미주·유럽 지역은 파트너사가 담당하는 방식으로 각 지역의 강점을 극대화하는 상호 보완적 서비스가 가능해졌다. 그 결과, 의뢰사가 원하는 시기에 신속하고 효율적인 품질 점검이 이뤄지고 있다. 또 의뢰사들은 국가 간 이동 비용 절감, 다국가 임상시험 효율화 등의 효과도 누릴 수 있게 됐다.
현재까지 QVIS와 글로벌 파트너사가 협력해 수행한 다국가 임상시험 품질 점검만 100건 이상에 달한다. 그뿐만 아니라, 2014년부터 2024년까지 수행한 총 800건 이상의 품질 점검 중 28%가 해외 임상시험 점검이었다. 이는 국내 CRO를 넘어, 국내 제약바이오 기업이 해외 임상시험을 성공적으로 수행할 수 있도록 돕는 중요한 가교 역할을 수행하고 있음을 의미한다.
QVIS는 다국적 임상시험 품질보증 경험뿐 아니라 FDA, EMA, PMDA 등 글로벌 주요 규제기관들의 실태조사 대응 경험을 축적해왔다. 2021년 이후 매년 100건 이상의 임상시험 품질보증 업무를 수행하며, 국제 규제기관의 까다로운 실태조사에 대비해 철저한 검증 시스템을 구축했다.
글로벌 약물감시 선도 기업 PrimeVigilance와 손잡고 글로벌 도약 나선다
임상시험의 품질보증뿐만 아니라 약물감시 서비스에서도 QVIS의 확장이 이어지고 있다. 2022년부터 QVIS는 유럽계 글로벌 약물감시 전문 CRO인 PrimeVigilance와 협력 관계를 맺고, 국내 제약바이오 기업들에게 국제적 수준의 약물감시 아웃소싱 서비스를 제공 중이다.
PrimeVigilance는 Ergomed plc산하의 세계적인 약물감시 및 의약정보 서비스 전문기업으로, 유럽에서 강력한 운영 네트워크를 구축했으며, 미국에서도 유수의 기업을 인수하며 입지를 넓혀왔다. 현재는 전 세계 주요 권역에서 약물감시 운영망을 확장하며 글로벌 약물감시 분야를 선도하는 기업으로 자리 잡았다.
QVIS는 PrimeVigilance와의 협력을 통해 국내외 제약바이오 기업들이 각국 규제 기관의 약물감시 요구사항을 철저히 준수할 수 있도록 지원하는 체계를 구축했다. QVIS는 현재 △임상시험 단계부터 시판 후까지전 주기적인 약물감시 지원 △의약품 안전성 정보 관리및 데이터 분석 △정기보고서(PSUR, PBRER) 작성및 제출 △신속한 이상사례(ADR) 보고 시스템 운영 등의 서비스를 제공하고 있다.
QVIS 현수미 대표는 "앞으로도 변화하는 국제 규제 환경에 발맞춰 품질보증과 약물감시 서비스를 지속적으로 발전시켜, 해당 분야의 글로벌 리더로 성장해 나갈 것”이라고 밝혔다.
[QVIS 주요 서비스]
·품질보증(Quality Management)
QVIS는 임상시험 및 약물감시 활동의 품질을 보장하기 위해 GCP, GLP, GVP 기준에 따른 점검을 수행하며, 위험 기반 품질보증(Risk-based QM Service) 접근법을 통해 최적화된 품질보증 시스템(QMS)을 구축하고 운영한다. 또한, 임상시험 및 약물감시 관련 SOP의 GAP 분석 및 최신 규제 반영을 지원하며, 실태조사 대비(Mock Inspection) 서비스를 통해 고객사의 규제 대응 역량을 강화한다.
·약물감시(Pharmacovigilance)
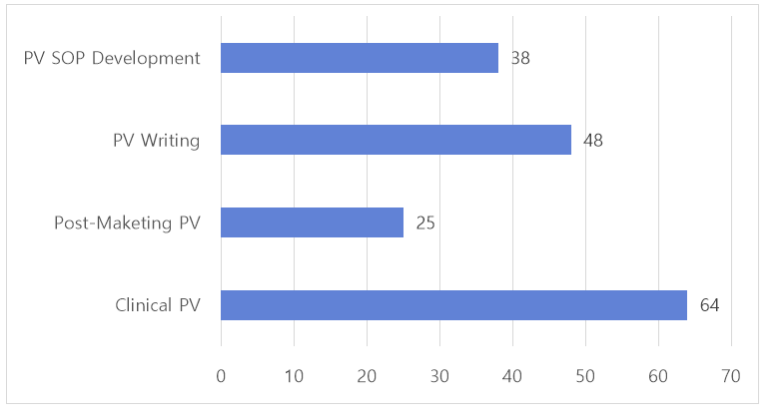
QVIS는 임상시험 및 시판 후 단계에서의 안전성 평가를 포함한 약물감시 서비스를 제공하며, DSUR, RMP, PBRER, PSMF 등의 안전성 보고서를 작성하고, 원시자료 분석을 통해 의약품의 안전성 평가 및 품목 갱신을 지원한다. 임상시험 중 발생하는 안전성 정보에 대한 평가와 관리뿐만 아니라, 글로벌 규제 요구사항에 맞춘 약물감시 전략을 수립하여 고객사의 규제 대응을 최적화한다.
·프로젝트 관리(Project Management)
QVIS는 임상시험 및 약물감시 프로젝트 전반에 대한 체계적인 관리 서비스를 제공하며, 벤더 선정, 계약 관리, 연구 진행 모니터링, 일정 및 비용 조정을 수행한다. 고객사의 연구가 계획대로 원활히 진행될 수 있도록 프로젝트 계획을 수립하고, 운영상의 리스크를 최소화하는 전략을 제시하여 효율적인 연구 진행을 보장한다.
·교육 및 컨설팅(Training & Consulting)
QVIS는 임상시험 및 약물감시 관련 교육 프로그램을 운영하여 고객사의 내부 역량 강화를 지원하며, 규제 변화 및 최신 기준을 반영한 맞춤형 교육을 제공한다. 또한, 품질보증시스템(QMS) 구축, SOP 개발, 실태조사 대응 등과 관련된 컨설팅을 통해 고객사가 글로벌 규제 기준을 충족할 수 있도록 돕는다.
[QVIS 주요 경험]
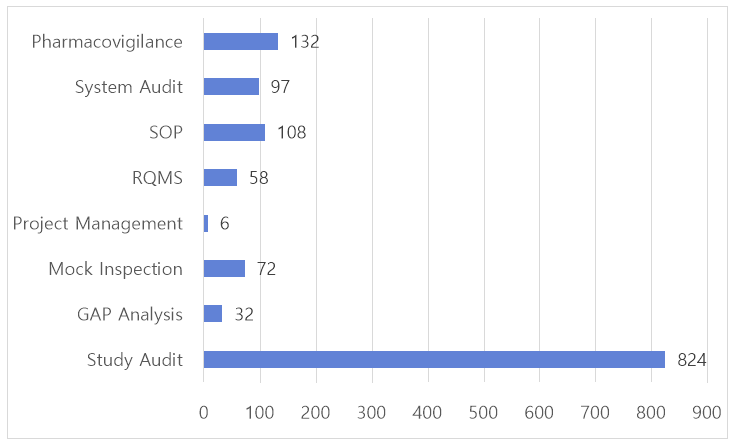
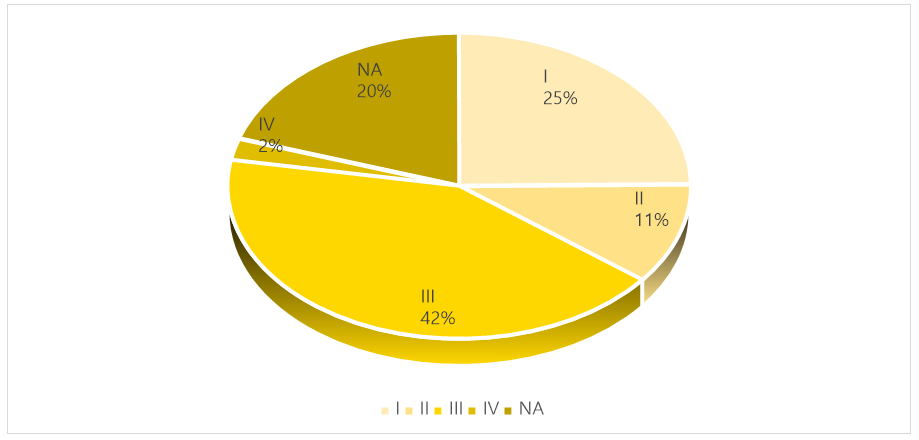
QVIS는 2014년 설립 이후 800건 이상의 임상시험 품질 점검을 수행했다. 이 중 28%는 해외 임상시험에 대한 글로벌 점검으로 이뤄졌다(2024년 기준). 특히, 2020년부터 2024년까지 식품의약품안전처 승인 국내 3상 임상시험의 약 49.8%에 대한 품질 점검을 수행, 국내 임상시험 품질보증 분야를 선도하고 있다.
| 인기기사 | 더보기 + |
-
1 JW중외제약, 중국 Gan & Lee제약과 대사질환치료제 라이선스인 계약 -
2 큐라티스,인벤티지랩과 의약품 위탁 개발-생산 계약 -
3 카나프테라퓨틱스, AACR 2026서 이중항체 항암신약 ‘KNP-101’ 연구성과 공개 -
4 “증상 전 시작됩니다”..'세계 파킨슨의 날',환자들 행동 나선다 -
5 인트론바이오, 박테리오파지 ‘드롭인’ 제형 특허 출원…동물용 항생제 대체재 시장 공략 -
6 대한약사회 권영희 집행부 1년…약준모 회원 83% '부정' -
7 “주사에서 알약으로”…K-바이오, '포스트 릴리' 향한 경구용 비만치료제 대격돌 -
8 셀트리온, ADC 신약 'CT-P71' 미국 FDA 패스트트랙 지정 -
9 보령, 국내 최초로 청소년 그림 달 표면 보낸다… 'HIS Youth' 수상작 탑재 -
10 동아제약, 오펠라와 일반약 4종 국내 독점 유통 계약 체결
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 권혁진 기자 hjkwon@yakup.com
- 입력 2025.03.26 06:00 수정 2025.03.26 10:40

신약개발의 마지막 관문인 임상시험, 그 신뢰성을 보증하는 품질보증. 이 중요한 과정에서 QVIS(큐앤비스)는 보이지 않는 ‘파수꾼’ 역할을 수행하며, 국내 제약바이오 산업이 글로벌 시장에서 경쟁력을 갖추는 데 핵심적인 역할을 하고 있다.
QVIS는 글로벌 수준의 임상시험 품질보증(Quality Management) 및 약물감시(Pharmacovigilance) 서비스를 제공하며 2014년 8월 설립 이후 꾸준한 성장을 이어왔다. 품질보증 전문기업으로는 국내 최초로 설립됐다. QVIS는 출범 이후 글로벌 수준의 품질보증 시스템을 구축하며 국내외 제약바이오 업계에서 확고한 입지를 다져왔다.
QVIS 현수미 대표는 국내 임상시험 품질보증 및 약물감시 분야에서 20년 이상의 경력을 쌓아온 전문가다. 현 대표는 숙명여자대학교 약학대학 제약학과에서 학사 및 석사 학위를 취득한 후, 성균관대학교 약학대학에서 약학 박사 학위를 받았다.
현 대표는 LG생명과학 임상개발팀, GSK Biological 임상개발팀, C&R Research 품질보증부서에서 다양한 실무 경험을 쌓으며 임상시험 품질보증 및 규제 대응 역량을 키웠다. 또한 Pan-Asia Pacific Clinical Research Association에서 Regional Director로 활동하며 아시아·태평양 지역의 임상시험 품질관리와 글로벌 규제 대응을 주도했다.
현 대표는 미국 Registered Quality Assurance Professional(공인 품질보증 전문가)로서 국내외 제약바이오 기업이 국제 기준을 준수하도록 돕는 데 앞장서고 있다.
2014년부터 약 800건 이상 임상 품질 점검 수행…28%는 해외 임상 글로벌 점검
QVIS는 국내 및 해외 제약사, 바이오텍, CRO를 대상으로 국제의약품규제조화위원회(ICH-GCP) 및 각국 규제 지침에 부합하는 맞춤형 품질보증 서비스를 제공한다. 의약품뿐만 아니라 의료기기, 첨단재생의료, 디지털치료제 등 다양한 치료 분야에서도 품질보증과 약물감시 업무를 수행한다. 특히 한국을 넘어 중국, 일본, 동남아, 미국, 유럽 등 글로벌에서도 활약 중이다.
QVIS는 2020년부터 2024년까지 식품의약품안전처가 승인한 국내 3상 임상시험의 약 49.8%에 대해 품질 점검을 수행했다. 이는 QVIS의 높은 위상을 증명한다. 국내 CRO 업계에서도 독보적인 성과로, QVIS는 임상시험의 신뢰성과 품질 향상을 위한 필수적인 역할을 수행하고 있다.
글로벌 품질보증 분야에서도 QVIS 영향력은 점점 커지고 있다. 영국 ADAMAS Consulting, ZigZag Associate를 비롯해, 미국 The FDA Group, G&L Scientific, Quality Systems International 등 해외 유수의 품질보증 컨설팅 및 CRO 업체들과 포괄적 협력계약(Mutual Service Agreement)을 체결, 글로벌 파트너십을 확대했다.
이러한 네트워크와 파트너십를 활용해 아시아 지역의 품질 점검은 QVIS가, 미주·유럽 지역은 파트너사가 담당하는 방식으로 각 지역의 강점을 극대화하는 상호 보완적 서비스가 가능해졌다. 그 결과, 의뢰사가 원하는 시기에 신속하고 효율적인 품질 점검이 이뤄지고 있다. 또 의뢰사들은 국가 간 이동 비용 절감, 다국가 임상시험 효율화 등의 효과도 누릴 수 있게 됐다.
현재까지 QVIS와 글로벌 파트너사가 협력해 수행한 다국가 임상시험 품질 점검만 100건 이상에 달한다. 그뿐만 아니라, 2014년부터 2024년까지 수행한 총 800건 이상의 품질 점검 중 28%가 해외 임상시험 점검이었다. 이는 국내 CRO를 넘어, 국내 제약바이오 기업이 해외 임상시험을 성공적으로 수행할 수 있도록 돕는 중요한 가교 역할을 수행하고 있음을 의미한다.
QVIS는 다국적 임상시험 품질보증 경험뿐 아니라 FDA, EMA, PMDA 등 글로벌 주요 규제기관들의 실태조사 대응 경험을 축적해왔다. 2021년 이후 매년 100건 이상의 임상시험 품질보증 업무를 수행하며, 국제 규제기관의 까다로운 실태조사에 대비해 철저한 검증 시스템을 구축했다.
글로벌 약물감시 선도 기업 PrimeVigilance와 손잡고 글로벌 도약 나선다
임상시험의 품질보증뿐만 아니라 약물감시 서비스에서도 QVIS의 확장이 이어지고 있다. 2022년부터 QVIS는 유럽계 글로벌 약물감시 전문 CRO인 PrimeVigilance와 협력 관계를 맺고, 국내 제약바이오 기업들에게 국제적 수준의 약물감시 아웃소싱 서비스를 제공 중이다.
PrimeVigilance는 Ergomed plc산하의 세계적인 약물감시 및 의약정보 서비스 전문기업으로, 유럽에서 강력한 운영 네트워크를 구축했으며, 미국에서도 유수의 기업을 인수하며 입지를 넓혀왔다. 현재는 전 세계 주요 권역에서 약물감시 운영망을 확장하며 글로벌 약물감시 분야를 선도하는 기업으로 자리 잡았다.
QVIS는 PrimeVigilance와의 협력을 통해 국내외 제약바이오 기업들이 각국 규제 기관의 약물감시 요구사항을 철저히 준수할 수 있도록 지원하는 체계를 구축했다. QVIS는 현재 △임상시험 단계부터 시판 후까지전 주기적인 약물감시 지원 △의약품 안전성 정보 관리및 데이터 분석 △정기보고서(PSUR, PBRER) 작성및 제출 △신속한 이상사례(ADR) 보고 시스템 운영 등의 서비스를 제공하고 있다.
QVIS 현수미 대표는 "앞으로도 변화하는 국제 규제 환경에 발맞춰 품질보증과 약물감시 서비스를 지속적으로 발전시켜, 해당 분야의 글로벌 리더로 성장해 나갈 것”이라고 밝혔다.
[QVIS 주요 서비스]
·품질보증(Quality Management)
QVIS는 임상시험 및 약물감시 활동의 품질을 보장하기 위해 GCP, GLP, GVP 기준에 따른 점검을 수행하며, 위험 기반 품질보증(Risk-based QM Service) 접근법을 통해 최적화된 품질보증 시스템(QMS)을 구축하고 운영한다. 또한, 임상시험 및 약물감시 관련 SOP의 GAP 분석 및 최신 규제 반영을 지원하며, 실태조사 대비(Mock Inspection) 서비스를 통해 고객사의 규제 대응 역량을 강화한다.
·약물감시(Pharmacovigilance)
QVIS는 임상시험 및 시판 후 단계에서의 안전성 평가를 포함한 약물감시 서비스를 제공하며, DSUR, RMP, PBRER, PSMF 등의 안전성 보고서를 작성하고, 원시자료 분석을 통해 의약품의 안전성 평가 및 품목 갱신을 지원한다. 임상시험 중 발생하는 안전성 정보에 대한 평가와 관리뿐만 아니라, 글로벌 규제 요구사항에 맞춘 약물감시 전략을 수립하여 고객사의 규제 대응을 최적화한다.
·프로젝트 관리(Project Management)
QVIS는 임상시험 및 약물감시 프로젝트 전반에 대한 체계적인 관리 서비스를 제공하며, 벤더 선정, 계약 관리, 연구 진행 모니터링, 일정 및 비용 조정을 수행한다. 고객사의 연구가 계획대로 원활히 진행될 수 있도록 프로젝트 계획을 수립하고, 운영상의 리스크를 최소화하는 전략을 제시하여 효율적인 연구 진행을 보장한다.
·교육 및 컨설팅(Training & Consulting)
QVIS는 임상시험 및 약물감시 관련 교육 프로그램을 운영하여 고객사의 내부 역량 강화를 지원하며, 규제 변화 및 최신 기준을 반영한 맞춤형 교육을 제공한다. 또한, 품질보증시스템(QMS) 구축, SOP 개발, 실태조사 대응 등과 관련된 컨설팅을 통해 고객사가 글로벌 규제 기준을 충족할 수 있도록 돕는다.
[QVIS 주요 경험]
QVIS는 2014년 설립 이후 800건 이상의 임상시험 품질 점검을 수행했다. 이 중 28%는 해외 임상시험에 대한 글로벌 점검으로 이뤄졌다(2024년 기준). 특히, 2020년부터 2024년까지 식품의약품안전처 승인 국내 3상 임상시험의 약 49.8%에 대한 품질 점검을 수행, 국내 임상시험 품질보증 분야를 선도하고 있다.




무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
