 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
신규조성물(NMEs) 신약 및 신규 생물의약품을 포함해 총 22개(12월 28일 현재 기준)의 신약들이 2016년 한해 동안 FDA의 허가관문을 통과한 것으로 나타났다.
FDA 약물평가연구센터(CDER)의 신규조성물 신약 및 신규 생물의약품 허가현황 자료에 따르면 지난 23일 최초의 척수성 근위축증 치료제로 허가를 취득한 바이오젠社의 ‘스핀라자’(Spinraza: 뉴시너센)까지 포함하더라도 전체 승인건수가 지난해의 45개에 미치지 못한 것으로 분석됐다.
참고로 지난해에는 희귀질환 치료제만도 전체 허가취득 신약의 절반에 육박하는 21개에 달하면서 47%를 점유한 것으로 집계됐었다. 그렇다면 전체 신약 허가건수가 지금까지 가장 많은 수의 새로운 희귀질환 치료제들이 FDA로부터 승인받은 해로 기록된 2015년의 21개와 앞‧뒷집 차이를 내보이는 데 그친 셈이다.
당초 애널리스트들은 올해 총 25개의 신규조성물 신약 및 생물의약품 신약들이 FDA의 허가를 취득할 수 있을 것으로 예상해 왔다.
하지만 이 수치는 12월 중으로 허가취득이 기대되었던 로슈社의 다발성 경화증 치료제 ‘오크레버스’(Ocrevus: 오크렐리주맙)과 셈프라社(Cempra)의 마크로라이드 계열 항균제 ‘솔리테라’(Solithera: 솔리스로마이신)까지 포함한 것이다.
‘오크레버스’는 지난 20일 FDA가 검토기간을 3개월 연장키로 했으며, ‘솔리테라’는 29일 FDA로부터 “불허한다”를 통보받았다.
이 중 ‘오크레버스’는 2016년 최대의 허가취득 사례가 될 수 있을 것이라는 전망까지 제기되면서 또 하나의 블록버스터 드럭 출현을 고대하케 했던 기대주이다.
또 다른 기대주였던 일라이 릴리社의 알쯔하이머 치료제 솔라네주맙(solanezumab)의 경우 지난달 개발이 실패로 귀결되면서 새삼 신약개발에 내재된 위험성을 환기시킨 바 있다.
이에 따라 설령 ‘오크레버스’와 ‘솔리테라’가 허가관문을 넘어섰더라도 2016년은 FDA의 허가를 취득한 신약들의 숫자가 크게 감소한 해로 기록되면서 최근 2년 동안 눈에 띄었던 연구‧개발 생산성 향상이 단지 일시적인 상황변화에 불과한 것이었을 수 있다는 관측에 무게가 실리게 할 것으로 보인다.
지난해의 경우 11월 말까지만 하더라도 총 40개의 신규조성물 신약들이 FDA로부터 발매를 승인받아 2014년 및 2013년의 기록을 조기에 훌쩍 뛰어넘은 바 있기 때문이다.
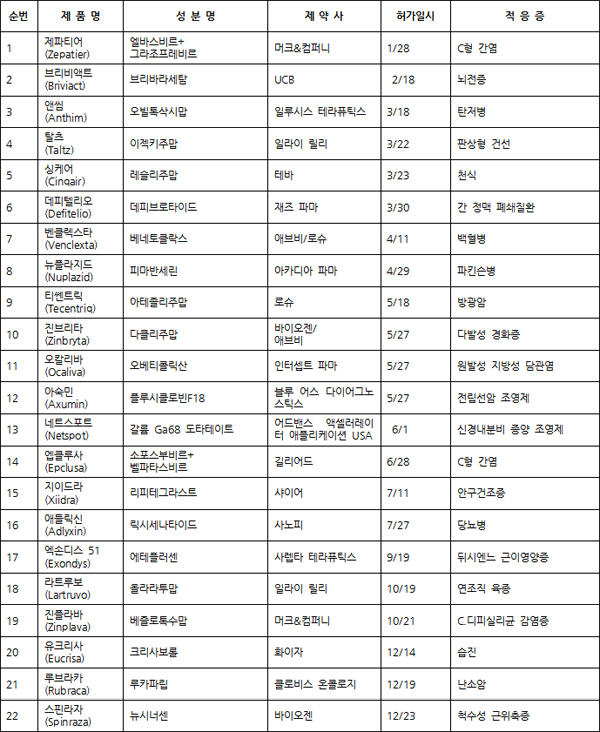
▉ 2016년 FDA 신약 허가현황
| 인기기사 | 더보기 + |
-
1 [기고] 김 변호사의 쉽게 읽는 바이오 ②알테오젠 -
2 로킷헬스케어, 사우디 만성신장질환 AI 플랫폼 계약 체결 -
3 유통협회, '이지메디컴' 정조준…병원도매 합류로 대웅 압박 전면전 -
4 복지부 "첨단재생의료 치료 1호, 희귀질환 극복의 실질적 이정표" -
5 메지온 “ ADPKD 치료제 임상,진행 중 전임상 종료후 2상 시작 가능” -
6 상장 제약바이오 환율변동손익 ‘뚝’…코스피 55.3%↓·코스닥 손실 전환 -
7 에임드바이오,베링거 인겔하임서 'ODS025' 기술이전 연구개발비 수령 -
8 삼성바이오로직스 노사 1대1 면담 취소…8일 노사정 대화로 넘어간 협상 -
9 알파타우, 미국 췌장암 임상 범위 확대… FDA IDE 보충안 승인 획득 -
10 삼익제약,2030년 매출 1300억원-영업익 110억원 도전
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 이덕규 기자 abcd@yakup.com
- 입력 2016.12.30 11:32 수정 2016.12.30 14:06
신규조성물(NMEs) 신약 및 신규 생물의약품을 포함해 총 22개(12월 28일 현재 기준)의 신약들이 2016년 한해 동안 FDA의 허가관문을 통과한 것으로 나타났다.
FDA 약물평가연구센터(CDER)의 신규조성물 신약 및 신규 생물의약품 허가현황 자료에 따르면 지난 23일 최초의 척수성 근위축증 치료제로 허가를 취득한 바이오젠社의 ‘스핀라자’(Spinraza: 뉴시너센)까지 포함하더라도 전체 승인건수가 지난해의 45개에 미치지 못한 것으로 분석됐다.
참고로 지난해에는 희귀질환 치료제만도 전체 허가취득 신약의 절반에 육박하는 21개에 달하면서 47%를 점유한 것으로 집계됐었다. 그렇다면 전체 신약 허가건수가 지금까지 가장 많은 수의 새로운 희귀질환 치료제들이 FDA로부터 승인받은 해로 기록된 2015년의 21개와 앞‧뒷집 차이를 내보이는 데 그친 셈이다.
당초 애널리스트들은 올해 총 25개의 신규조성물 신약 및 생물의약품 신약들이 FDA의 허가를 취득할 수 있을 것으로 예상해 왔다.
하지만 이 수치는 12월 중으로 허가취득이 기대되었던 로슈社의 다발성 경화증 치료제 ‘오크레버스’(Ocrevus: 오크렐리주맙)과 셈프라社(Cempra)의 마크로라이드 계열 항균제 ‘솔리테라’(Solithera: 솔리스로마이신)까지 포함한 것이다.
‘오크레버스’는 지난 20일 FDA가 검토기간을 3개월 연장키로 했으며, ‘솔리테라’는 29일 FDA로부터 “불허한다”를 통보받았다.
이 중 ‘오크레버스’는 2016년 최대의 허가취득 사례가 될 수 있을 것이라는 전망까지 제기되면서 또 하나의 블록버스터 드럭 출현을 고대하케 했던 기대주이다.
또 다른 기대주였던 일라이 릴리社의 알쯔하이머 치료제 솔라네주맙(solanezumab)의 경우 지난달 개발이 실패로 귀결되면서 새삼 신약개발에 내재된 위험성을 환기시킨 바 있다.
이에 따라 설령 ‘오크레버스’와 ‘솔리테라’가 허가관문을 넘어섰더라도 2016년은 FDA의 허가를 취득한 신약들의 숫자가 크게 감소한 해로 기록되면서 최근 2년 동안 눈에 띄었던 연구‧개발 생산성 향상이 단지 일시적인 상황변화에 불과한 것이었을 수 있다는 관측에 무게가 실리게 할 것으로 보인다.
지난해의 경우 11월 말까지만 하더라도 총 40개의 신규조성물 신약들이 FDA로부터 발매를 승인받아 2014년 및 2013년의 기록을 조기에 훌쩍 뛰어넘은 바 있기 때문이다.
▉ 2016년 FDA 신약 허가현황

무단 전재·복사·배포 등을 금지합니다.



