온코닉테라퓨틱스(대표 김존)는 국산 37호 신약 위식도역류질환 치료제 ‘자큐보정(성분명 자스타프라잔)’ 임상 3상 결과가 SCIE급 의학 학술지인 American Journal of Gastroenterology에 게재되며 우수성과 안전성을 다시 입증했다고 21일 밝혔다.
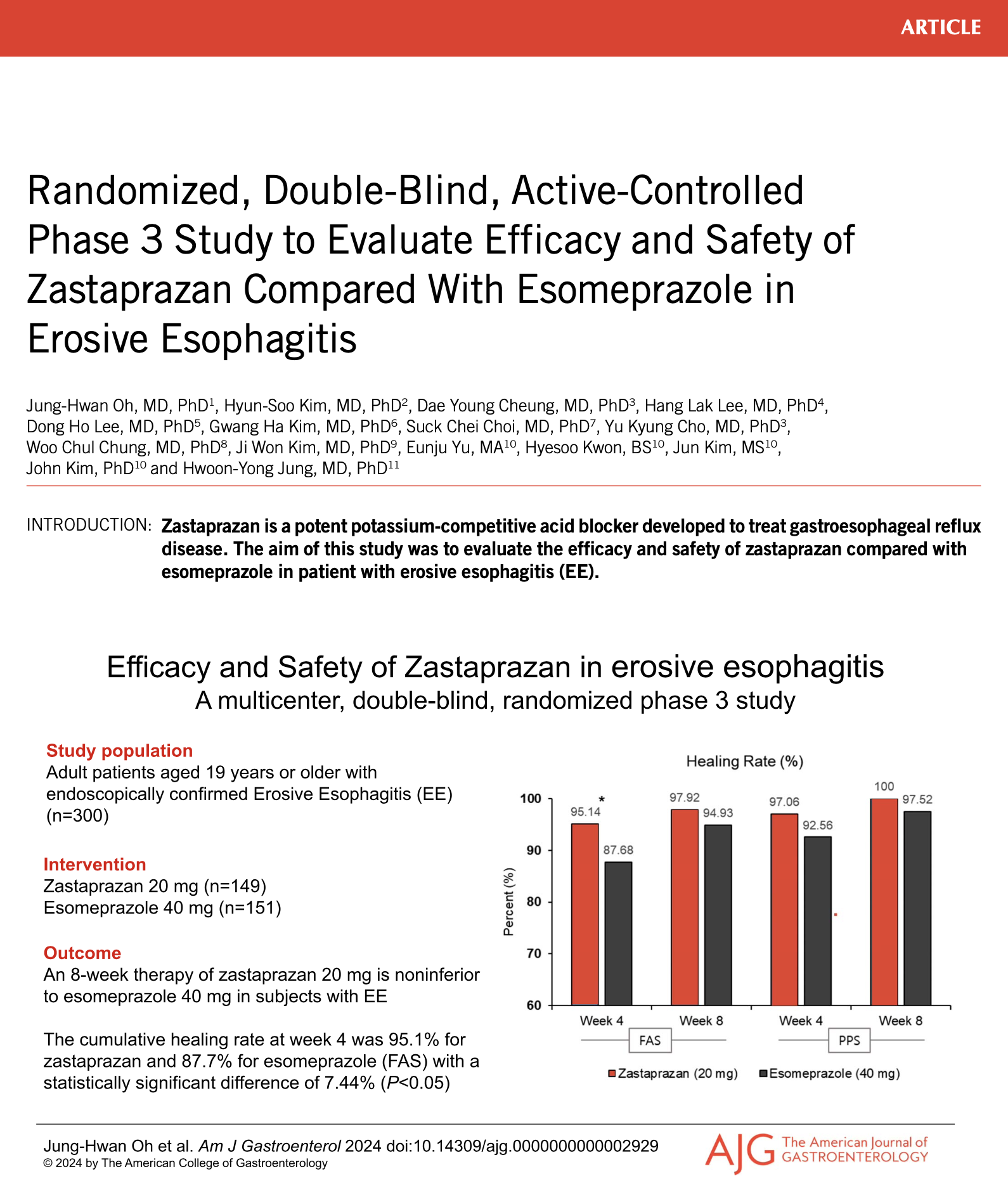
게재 논문명은 ‘Randomized, double-blind, active-controlled phase 3 study to evaluate efficacy and safety of zastaprazan compared with esomeprazole in erosive esophagitis’으로, P-CAB계열인 국내 37호 신약 자스타프라잔의 유효성 및 안전성에 관한 임상 3상시험을 미란성 위식도역류질환 환자를 대상으로 대조군인 PPI계열 약물 에스오메프라졸과의 비교 연구한 결과다.
이번 임상3상 시험은 서울아산병원 소화기내과 정훈용 교수 주도하에 국내 주요 병원에서 내시경상 미란성 위식도역류질환 환자 300명을 대상으로 이중눈가림, 무작위 배정을 통해 자스타프라잔 20 mg(149명), 대조군 에스오메프라졸 40 mg(151명)으로 나눠 최대 8주 동안 투여했다.
8주 투여 결과, 자스타프라잔은 97.9%의 높은 치료율로 대조군 94.9% 대비 우수한 효능을 확인했다. 특히, 4주 투여 시 자스타프라잔 치료율은 95.1%로 대조군 87.7% 보다 7.44%높은 치료율을 보이며 신속하게 효능이 발휘되는 것을 확인했다고 회사는 전했다.
부작용 분석결과 자스타프라잔과 대조군 간의 통계적 차이는 없었다. 따라서 안전성에 측면에서 오랫동안 표준치료제로 사용해 왔던 에스오메프라졸과 비슷해 특별한 부작용이 나타나지는 않을 것으로 회사는 기대하고 있다.
현재 자스타프라잔은 기허가 받은 미란성 위식도역류질환뿐만 아니라, 위궤양 및 NSAID 유도성 소화성 궤양 예방 적응증 등으로 확대하기 위한 임상시험을 진행하고 있다.
온코닉테라퓨틱스 김존 대표는 "세계적인 소화기 저널에 3상 시험 논문이 게재돼 전 세계 의료진에게 K-신약인 자스타프라잔의 임상 결과를 공유할 수 있어 기쁘다”며 "앞으로 한국 및 해외에서의 빠른 상용화를 위해 최선을 다할 것이며, 적응증 확대에도 역량을 집중할 것"이라고 강조했다.
온코닉테라퓨틱스는 중국 제약기업 리브존파마슈티컬그룹과 중화권에서의 자스타프라잔 개발 및 상업화에 1억2750만달러(한화 약1600억원) 규모의 기술수출 계약을 체결한 바 있다.
한편 이번 임상 결과가 등재된 American Journal of Gastroenterology는 SCIE급 소화기분야 세계 최고 의학 학술지(피인용지수 10.2) 중 하나다.
| 인기기사 | 더보기 + |
-
1 [약업분석] 알테오젠, 매출 2배·영업익 320% 급등 -
2 [기고] 김 변호사의 쉽게 읽는 바이오 ①리가켐바이오사이언스 -
3 상장 제약·바이오 2025년 누적 평균 매출총이익 코스피 3338억·코스닥 1020억 -
4 상장 제약·바이오사 2025년 평균 매출… 코스피 7487억원, 코스닥 1990억원 기록 -
5 상장 제약·바이오 2025년 누적 평균 영업이익 코스피 1084억·코스닥 229억 -
6 [스페셜리포트] 인벤테라, 혁신 MRI 조영제 넘어 글로벌 나노의약품 기업 도약 -
7 다이이찌산쿄, ADC 생체지표 발굴 AI 접목 제휴 -
8 [약업 분석] 바이오솔루션, 순이익 122억원 늘며 '흑자전환' -
9 [약업분석] 엘앤씨바이오, 총매출 855억에도 순익 대규모 적자 -
10 상장 제약·바이오 2025년 누적 평균 순이익 코스피 917억원·코스닥 175억원
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 이상훈 기자 jianhs@yakup.com
- 입력 2024.08.21 10:33

온코닉테라퓨틱스(대표 김존)는 국산 37호 신약 위식도역류질환 치료제 ‘자큐보정(성분명 자스타프라잔)’ 임상 3상 결과가 SCIE급 의학 학술지인 American Journal of Gastroenterology에 게재되며 우수성과 안전성을 다시 입증했다고 21일 밝혔다.
게재 논문명은 ‘Randomized, double-blind, active-controlled phase 3 study to evaluate efficacy and safety of zastaprazan compared with esomeprazole in erosive esophagitis’으로, P-CAB계열인 국내 37호 신약 자스타프라잔의 유효성 및 안전성에 관한 임상 3상시험을 미란성 위식도역류질환 환자를 대상으로 대조군인 PPI계열 약물 에스오메프라졸과의 비교 연구한 결과다.
이번 임상3상 시험은 서울아산병원 소화기내과 정훈용 교수 주도하에 국내 주요 병원에서 내시경상 미란성 위식도역류질환 환자 300명을 대상으로 이중눈가림, 무작위 배정을 통해 자스타프라잔 20 mg(149명), 대조군 에스오메프라졸 40 mg(151명)으로 나눠 최대 8주 동안 투여했다.
8주 투여 결과, 자스타프라잔은 97.9%의 높은 치료율로 대조군 94.9% 대비 우수한 효능을 확인했다. 특히, 4주 투여 시 자스타프라잔 치료율은 95.1%로 대조군 87.7% 보다 7.44%높은 치료율을 보이며 신속하게 효능이 발휘되는 것을 확인했다고 회사는 전했다.
부작용 분석결과 자스타프라잔과 대조군 간의 통계적 차이는 없었다. 따라서 안전성에 측면에서 오랫동안 표준치료제로 사용해 왔던 에스오메프라졸과 비슷해 특별한 부작용이 나타나지는 않을 것으로 회사는 기대하고 있다.
현재 자스타프라잔은 기허가 받은 미란성 위식도역류질환뿐만 아니라, 위궤양 및 NSAID 유도성 소화성 궤양 예방 적응증 등으로 확대하기 위한 임상시험을 진행하고 있다.
온코닉테라퓨틱스 김존 대표는 "세계적인 소화기 저널에 3상 시험 논문이 게재돼 전 세계 의료진에게 K-신약인 자스타프라잔의 임상 결과를 공유할 수 있어 기쁘다”며 "앞으로 한국 및 해외에서의 빠른 상용화를 위해 최선을 다할 것이며, 적응증 확대에도 역량을 집중할 것"이라고 강조했다.
온코닉테라퓨틱스는 중국 제약기업 리브존파마슈티컬그룹과 중화권에서의 자스타프라잔 개발 및 상업화에 1억2750만달러(한화 약1600억원) 규모의 기술수출 계약을 체결한 바 있다.
한편 이번 임상 결과가 등재된 American Journal of Gastroenterology는 SCIE급 소화기분야 세계 최고 의학 학술지(피인용지수 10.2) 중 하나다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
