 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
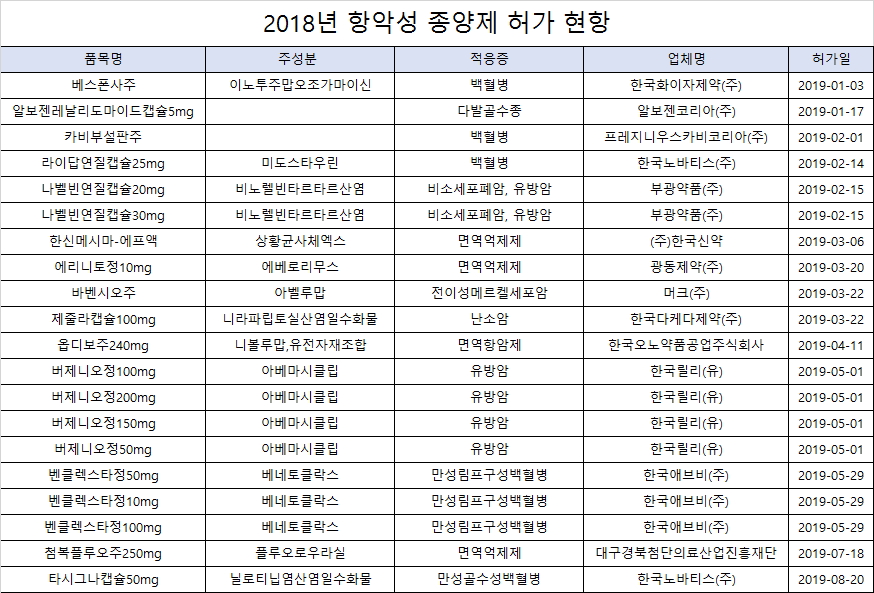
올해들어 전이성 메르켈세포암 치료제인 '바벤시오주' 등 14개성분 20개 품목의 항암제가 국내에서 허가를 받은 것으로 집계됐다.
식품의약품안전처에 따르면 지난 1월 한국화이자제약의 백혈병치료제 '베스폰사주'가 허가를 받은 이후 지난 8월 20일 한국노바티스의 '타시그나캡슐50mg' 까지 올해들어 총 20품목의 항악성 종양제가 허가를 받았다.
적응증으로는 백혈병치료제가 7품목으로 가장 많았고, 유방암치료제 6품목 등의 순이었다.
국내 제약업체는 알보젠코리아의 다발성골수종치료제 알보젠'레날리도마이드캡슐5mg', 부광약품의 비소세포폐암 유방암 치료제인 '나벨빈연질캡슐20mg'. 한국신약의 생약제제인 '한신메시마-에프액', 광동제약의 면역억제제'에리니토정10mg' 등이 허가를 받았다.
한국다케다제약은 '제줄라캡슐100mg'을 2차 이상의 백금기반 항암화학요법에 완전·부분 반응한 백금민감성 재발성 고도장액성 난소암(난관암 또는 일차 복막암 포함) 성인 환자의 단독 유지요법으로 허가받았다.
머크는 국내 유일의 전이성 메르켈세포암 치료제인 '바벤시오주'를 허가받았고, 한국릴리는 유방암치료제 신약인 '버제니오정100mg' 등 4개 품목을 허가받았다.
한국에브비는 국내 최초이자 유일한 경구용 B세포 림프종-2(BCL-2, B-cell lymphoma-2) 억제제인 '벤클렉스타정(VENCLEXTA, 성분명: 베네토클락스(venetoclax)) 50mg' 등 3품목을 만성 림프구성 백혈병(CLL, Chronic Lymphocytic Leukemia) 치료제로 5월 29일 허가받았다.
| 인기기사 | 더보기 + |
-
1 창고형 약국 공세…'가격으론 못 이긴다' 동네약국 생존법은 -
2 인벤티지랩,'장기지속 치매치료제' 호주 임상1상 미국신경학회 학술대회 발표 -
3 지엔티파마, 반려견 치매 신약 ‘제다큐어’ 원료물질 유럽 제조 특허 취득 -
4 로킷헬스케어 AI 당뇨발 재생 플랫폼, 이집트 국가보험 취득 -
5 유통협, 21일 대웅 앞 대규모 집회…'거점도매 철회' 총력 투쟁 -
6 "수십억 들인 DTx가 '단순 보조 앱'?… 낡은 잣대에 갇힌 K-의료 AI" -
7 큐로셀, 서울대병원·스탠퍼드와 AACR서 CAR-T 신기술 발표 -
8 비씨켐,폐암 면역항암제 'STING Agonist LNP' 기술이전 계약 체결 -
9 HK이노엔-넥스트젠바이오,특발성 폐섬유증 신약 공동 연구개발 추진 -
10 웨스트파마슈티컬서비스 “주사제 ‘용기·투여 시스템’까지 검증 필수”
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 김용주 기자 yjkim@yakup.com
- 입력 2019.09.16 06:00 수정 2019.09.16 07:09
올해들어 전이성 메르켈세포암 치료제인 '바벤시오주' 등 14개성분 20개 품목의 항암제가 국내에서 허가를 받은 것으로 집계됐다.
식품의약품안전처에 따르면 지난 1월 한국화이자제약의 백혈병치료제 '베스폰사주'가 허가를 받은 이후 지난 8월 20일 한국노바티스의 '타시그나캡슐50mg' 까지 올해들어 총 20품목의 항악성 종양제가 허가를 받았다.
적응증으로는 백혈병치료제가 7품목으로 가장 많았고, 유방암치료제 6품목 등의 순이었다.
국내 제약업체는 알보젠코리아의 다발성골수종치료제 알보젠'레날리도마이드캡슐5mg', 부광약품의 비소세포폐암 유방암 치료제인 '나벨빈연질캡슐20mg'. 한국신약의 생약제제인 '한신메시마-에프액', 광동제약의 면역억제제'에리니토정10mg' 등이 허가를 받았다.
한국다케다제약은 '제줄라캡슐100mg'을 2차 이상의 백금기반 항암화학요법에 완전·부분 반응한 백금민감성 재발성 고도장액성 난소암(난관암 또는 일차 복막암 포함) 성인 환자의 단독 유지요법으로 허가받았다.
머크는 국내 유일의 전이성 메르켈세포암 치료제인 '바벤시오주'를 허가받았고, 한국릴리는 유방암치료제 신약인 '버제니오정100mg' 등 4개 품목을 허가받았다.
한국에브비는 국내 최초이자 유일한 경구용 B세포 림프종-2(BCL-2, B-cell lymphoma-2) 억제제인 '벤클렉스타정(VENCLEXTA, 성분명: 베네토클락스(venetoclax)) 50mg' 등 3품목을 만성 림프구성 백혈병(CLL, Chronic Lymphocytic Leukemia) 치료제로 5월 29일 허가받았다.

무단 전재·복사·배포 등을 금지합니다.



