 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
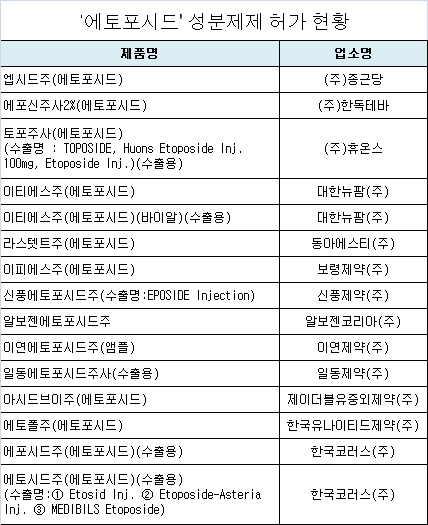
식품의약품안전처는 '에토포시드' 성분제제의 미국 식품의약품청(FDA) 안전성 정보와 관해 국내·외 허가 현황, 제출의견 등을 종합 검토한 결과에 따라 13개사 15품목에 대해 8월 19일자로 허가사항 변경지시를 내렸다고 밝혔다.
'에토포시드' 성분 제제의 대표 품목은 종근당의 '엡시드주'이다.
'엡시드주'는 소세포폐암, 악성림프종, 급성백혈병, 고환종양, 방광암, 융모성질환의 효능효과를 갖고 있다.
식약처는 '에토포시드' 성분제제의 허가사항중 이상반응항에 '급성신부전증 : 조혈모세포 이식을 위해 에토포시드 고용량(2220 mg/m2) 투여 및 전신조사(total body irradiation) 후 가역성 급성 신부전증 발병이 보고 되었다. 급성 신부전증은 덱스트란 40을 함유한 에토포시드 성분제제를 고용량으로 투여한 것과 관련되어 있다'는 내용을 신설하도록 했다.
| 인기기사 | 더보기 + |
-
1 디앤디파마텍 MASH 치료제 임상2상 48주 데이터베이스 락 완료 -
2 큐리옥스,'Pluto Code' 전사적 도입 포괄적 소프트웨어 라이선스 계약 체결 -
3 [AACR] 에이비엘바이오 승부수 이중항체 ADC ‘ABL209’ 첫 청신호 켜졌다 -
4 네이처셀,조인트스템 FDA 가속승인 본격화..브리핑 패키지 제출 -
5 상장 제약·바이오 2025년 평균 유보율 코스피 2142.15%·코스닥 2583.86% -
6 페니트리움바이오,표적항암제 내성 해결 'Dual-agnostic Basket Trial' 추진 -
7 AI 설계 신약 173개 임상…첫 허가 '초읽기', 개발 전주기 재편 -
8 [AACR] 삼성바이오에피스가 'Nectin-4' ADC 선택한 이유는 -
9 식약처 CHORUS 3년차…의약품 규제 ‘공동 설계’ 체계로 전환 -
10 대웅제약 "블록형 거점도매, 독점 아닌 '유통 혁신'… 특혜 사실무근"
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 김용주 기자 yjkim@yakup.com
- 입력 2019.08.02 12:00 수정 2019.08.02 12:02

식품의약품안전처는 '에토포시드' 성분제제의 미국 식품의약품청(FDA) 안전성 정보와 관해 국내·외 허가 현황, 제출의견 등을 종합 검토한 결과에 따라 13개사 15품목에 대해 8월 19일자로 허가사항 변경지시를 내렸다고 밝혔다.
'에토포시드' 성분 제제의 대표 품목은 종근당의 '엡시드주'이다.
'엡시드주'는 소세포폐암, 악성림프종, 급성백혈병, 고환종양, 방광암, 융모성질환의 효능효과를 갖고 있다.
식약처는 '에토포시드' 성분제제의 허가사항중 이상반응항에 '급성신부전증 : 조혈모세포 이식을 위해 에토포시드 고용량(2220 mg/m2) 투여 및 전신조사(total body irradiation) 후 가역성 급성 신부전증 발병이 보고 되었다. 급성 신부전증은 덱스트란 40을 함유한 에토포시드 성분제제를 고용량으로 투여한 것과 관련되어 있다'는 내용을 신설하도록 했다.
무단 전재·복사·배포 등을 금지합니다.



