지난해 전문약 1,002건 허가...전년 대비 소폭 감소
국내 신약 3품목, 세계 최초 바이오시밀러 등 허가
이혜선 기자
lhs@yakup.com  기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
입력 2013.02.25 09:34
수정 2013.02.25 11:21
지난해 허가된 전문의약품이 모두 1002건인 것으로 나타났다.
지난 2010년 재심사 기간 만료 또는 특허만료로 인해 1343건이 허가 이후 해마다 조금씩 감소하는 추세다. 일반의약품은 GMP의무화 이전인 2009년 대거 허가를 받은 이후 비슷한 수준을 유지하고 있는 중이다.
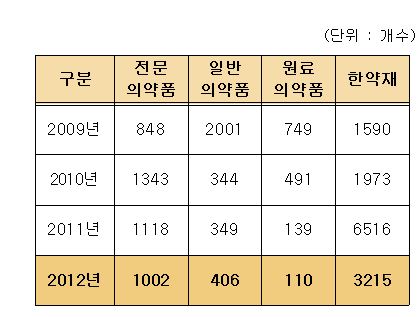
또한 허가신고된 품목수는 모두 4,733개로서 2011년(8,122개)에 비해 42% 정도 감소했다고 밝혔다.
허가신고 품목수가 대폭 감소한 이유는 한약재 허가가 2011년(6,516개)에 비해 지난해에는 3,215개로 크게 감소했기 때문이다.
지난 2011년 10월 부터 한약도매업소에서 한약재를 단순 가공 하는 등의 행위를 금지함에 따라 그해에 한약재 허가신고 품목수가 급증한 바 있다.
한약재를 제외한 의약품 허가(신고)품목수도 2012년 1,518개로 2011년(1,606개)에 비해 약 5% 감소했다.
식약청은 지난 2008년 품목별 사전 GMP 제도 실시 이후 국내 제약업계의 산업구조가 소품목 대량생산으로 재편되고 있어 신규 허가(신고) 신청이 증가하지 않는 것으로 분석했다.
◆지난해 국내 개발 신약 3품목 허가
지난해 허가된 국내 개발 신약으로 백혈병치료제 슈펙트캡슐 100mg 및 200mg과 당뇨병 치료제인 제미글로정 등 3개가 허가됐다.
개량신약은 ‘애피트롤이에스 내복 현탁액’ 등 6품목이 허가돼 2011년 2품목에 비해 늘어났다.
더불어 수입에 의존하던 희귀의약품도 지난해 국내에서 처음으로 ‘헌터라제(헌터증후군)’, ‘애브서틴(고셔병)’ 2품목이 허가됐다.
생물의약품은 바이오시밀러로 국내에서 개발된 ‘램시마’가 세계 최초로 허가됐으며, 세포치료제인 ‘카티스템(골관절염)’ 및 ‘큐피스템(크론병)’ 2품목이 허가됐다.
◆발기부전치료제 등 허가 대폭 증가
지난해 허가(신고) 품목 중 한약재, 원료의약품을 제외한 1,408개를 약효군 별로 분석한 결과 ▲‘해열·진통·소염제’ 등 신경계의약품(269개, 19%) ▲‘골다공증 치료제’ 등 대사성의약품(200개, 14%) ▲‘고혈압치료제’ 등 순환계의약품(162개, 11%)순이었다.
특히, 대사성의약품은 골다공증치료제 개발(53개)이 활기를 띄면서 2011년(10개)에 비해 상승폭이 가장 컸으며, 그 다음으로 발기부전치료제 등 비뇨생식기관용의약품이 2011년 20개에서 2012년 79개로 증가했다.
오늘의 헤드라인
전체댓글 0개
등록된 댓글이 없습니다.
| 인기기사 | 더보기 + |
-
1 [기고] 김 변호사의 쉽게 읽는 바이오 ②알테오젠 -
2 메지온 “ ADPKD 치료제 임상,진행 중 전임상 종료후 2상 시작 가능” -
3 유통협회, '이지메디컴' 정조준…병원도매 합류로 대웅 압박 전면전 -
4 복지부 "첨단재생의료 치료 1호, 희귀질환 극복의 실질적 이정표" -
5 로킷헬스케어, 사우디 만성신장질환 AI 플랫폼 계약 체결 -
6 상장 제약바이오 환율변동손익 ‘뚝’…코스피 55.3%↓·코스닥 손실 전환 -
7 에임드바이오,베링거 인겔하임서 'ODS025' 기술이전 연구개발비 수령 -
8 알파타우, 미국 췌장암 임상 범위 확대… FDA IDE 보충안 승인 획득 -
9 [2026 기대 신약 TOP 10] ⑦ 본태성 진전 치료제 ‘울릭사칼타마이드’ -
10 2027년도 수가협상 시작…의약단체 "보상 필요" 공단 "재정 부담"
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

지난해 전문약 1,002건 허가...전년 대비 소폭 감소
국내 신약 3품목, 세계 최초 바이오시밀러 등 허가
- 이혜선 기자 lhs@yakup.com
- 입력 2013.02.25 09:34 수정 2013.02.25 11:21
지난해 허가된 전문의약품이 모두 1002건인 것으로 나타났다.
지난 2010년 재심사 기간 만료 또는 특허만료로 인해 1343건이 허가 이후 해마다 조금씩 감소하는 추세다. 일반의약품은 GMP의무화 이전인 2009년 대거 허가를 받은 이후 비슷한 수준을 유지하고 있는 중이다.

또한 허가신고된 품목수는 모두 4,733개로서 2011년(8,122개)에 비해 42% 정도 감소했다고 밝혔다.
허가신고 품목수가 대폭 감소한 이유는 한약재 허가가 2011년(6,516개)에 비해 지난해에는 3,215개로 크게 감소했기 때문이다.
지난 2011년 10월 부터 한약도매업소에서 한약재를 단순 가공 하는 등의 행위를 금지함에 따라 그해에 한약재 허가신고 품목수가 급증한 바 있다.
한약재를 제외한 의약품 허가(신고)품목수도 2012년 1,518개로 2011년(1,606개)에 비해 약 5% 감소했다.
식약청은 지난 2008년 품목별 사전 GMP 제도 실시 이후 국내 제약업계의 산업구조가 소품목 대량생산으로 재편되고 있어 신규 허가(신고) 신청이 증가하지 않는 것으로 분석했다.
◆지난해 국내 개발 신약 3품목 허가
지난해 허가된 국내 개발 신약으로 백혈병치료제 슈펙트캡슐 100mg 및 200mg과 당뇨병 치료제인 제미글로정 등 3개가 허가됐다.
개량신약은 ‘애피트롤이에스 내복 현탁액’ 등 6품목이 허가돼 2011년 2품목에 비해 늘어났다.
더불어 수입에 의존하던 희귀의약품도 지난해 국내에서 처음으로 ‘헌터라제(헌터증후군)’, ‘애브서틴(고셔병)’ 2품목이 허가됐다.
생물의약품은 바이오시밀러로 국내에서 개발된 ‘램시마’가 세계 최초로 허가됐으며, 세포치료제인 ‘카티스템(골관절염)’ 및 ‘큐피스템(크론병)’ 2품목이 허가됐다.
◆발기부전치료제 등 허가 대폭 증가
지난해 허가(신고) 품목 중 한약재, 원료의약품을 제외한 1,408개를 약효군 별로 분석한 결과 ▲‘해열·진통·소염제’ 등 신경계의약품(269개, 19%) ▲‘골다공증 치료제’ 등 대사성의약품(200개, 14%) ▲‘고혈압치료제’ 등 순환계의약품(162개, 11%)순이었다.
특히, 대사성의약품은 골다공증치료제 개발(53개)이 활기를 띄면서 2011년(10개)에 비해 상승폭이 가장 컸으며, 그 다음으로 발기부전치료제 등 비뇨생식기관용의약품이 2011년 20개에서 2012년 79개로 증가했다.
Copyright © Yakup.com All rights reserved.
약업신문 의 모든 컨텐츠(기사)는 저작권법의 보호를 받습니다.
무단 전재·복사·배포 등을 금지합니다.
무단 전재·복사·배포 등을 금지합니다.



