 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
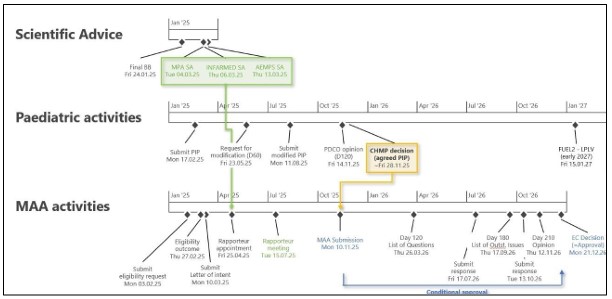
폰탄치료제 ‘jurvigo’ 미국 FDA 승인을 추진 중인 메지온이 유럽 신약 허가 승인 추진 일정을 공개했다.
20일 메지온 ‘유럽 NDA 추진 현황’에 따르면 먼저 심혈관 계통 혹은 소아과 신약 허가에 우호적인 EU국가를 선별(3개국 정도)하고 각 국가 Scientific Advice(SA)에Briefing Package를 준비해 제출, 내년 2-3월 선별된 각 국가 SA 개최를 예상하고 있다.
동시에 Pediatric Committee(PDCO)에 제출할 Pediatric Investigation Program(PIP)를 준비하며, 준비된 서류에 대한 PDCO 판단 여부는 내년 4분기 경을 예상하고 있다.
이러한 과정이 완료되면 EMA에 Marketing Authorization Application(MAA)를 진행하기 위해, 조사 위원(Rapporteur)지정과 미팅을 거치게 되며, 이후 준비된 서류를 기반으로 조건부 승인(Conditional Approval)을 신청하게 된다. 회사는 시기를 2025년 4분기로 예상하고 있다.
회사 관계자는 " 약 1년 정도 검토가 모두 완료된 후 조건부 승인을 득하게 되면 유럽에서 신약 판매가 가능하게 된다"며 “이후 미국 FDA의 FUEL-2에 대한 승인이 나면, 그 내용을 추가해 유럽에서 완전한 승인(Full Approval)을 받고자 한다”고 설명했다.

- 이권구 기자 kwon9@yakup.com
- 입력 2024.12.20 09:30 수정 2024.12.20 10:49

폰탄치료제 ‘jurvigo’ 미국 FDA 승인을 추진 중인 메지온이 유럽 신약 허가 승인 추진 일정을 공개했다.
20일 메지온 ‘유럽 NDA 추진 현황’에 따르면 먼저 심혈관 계통 혹은 소아과 신약 허가에 우호적인 EU국가를 선별(3개국 정도)하고 각 국가 Scientific Advice(SA)에Briefing Package를 준비해 제출, 내년 2-3월 선별된 각 국가 SA 개최를 예상하고 있다.
동시에 Pediatric Committee(PDCO)에 제출할 Pediatric Investigation Program(PIP)를 준비하며, 준비된 서류에 대한 PDCO 판단 여부는 내년 4분기 경을 예상하고 있다.
이러한 과정이 완료되면 EMA에 Marketing Authorization Application(MAA)를 진행하기 위해, 조사 위원(Rapporteur)지정과 미팅을 거치게 되며, 이후 준비된 서류를 기반으로 조건부 승인(Conditional Approval)을 신청하게 된다. 회사는 시기를 2025년 4분기로 예상하고 있다.
회사 관계자는 " 약 1년 정도 검토가 모두 완료된 후 조건부 승인을 득하게 되면 유럽에서 신약 판매가 가능하게 된다"며 “이후 미국 FDA의 FUEL-2에 대한 승인이 나면, 그 내용을 추가해 유럽에서 완전한 승인(Full Approval)을 받고자 한다”고 설명했다.
무단 전재·복사·배포 등을 금지합니다.



