앱클론이 AACR 2026에서 차세대 고형암 CAR-T와 이중항체 플랫폼을 동시에 공개하며 전임상 데이터 경쟁력을 제시했다. 핵심은 ‘초저용량에서도 완전 종양 억제’와 ‘종양미세환경(TME) 제어’다. 고형암 CAR-T의 구조적 한계를 겨냥한 플랫폼 설계가 실제 데이터로 연결됐다는 점에 의미가 있다.
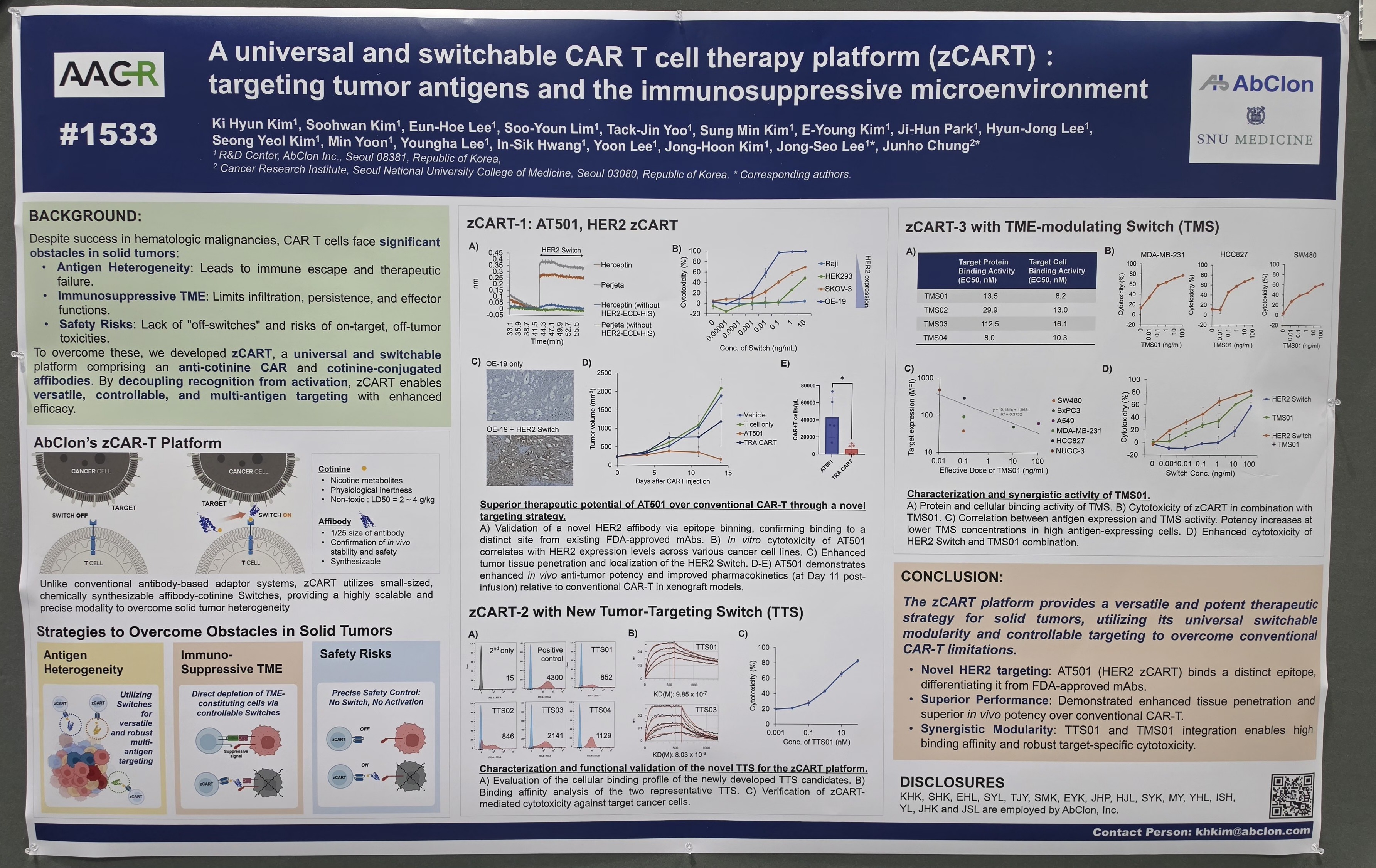
항체 신약개발 기업 앱클론은 미국 샌디에이고에서 열린 미국암연구학회(AACR) 2026에서 차세대 항암 플랫폼 ‘zCAR-T’와 전립선암 타깃 이중항체 ‘AM109’ 연구 결과를 포스터로 발표했다고 21일 밝혔다.
이번 발표에서 먼저 공개된 AM109는 자사 이중항체 플랫폼 ‘어피맵(AffiMab)’ 기반 후보물질이다. 전립선암 표적 PSMA와 T세포 공동자극 수용체 4-1BB(CD137)를 동시에 겨냥하는 구조다. 종양미세환경 내 PSMA 발현 세포가 존재할 때만 T세포를 활성화하는 타깃 의존적 기전이 핵심이다.
전임상 결과, AM109는 0.1~0.3 mg/kg(체중당 투여량) 수준의 저용량에서도 종양의 완전 관해(complete tumor regression)를 유도했다. 동일 계열 4-1BB 작용제인 우토밀루맙 대비 항암 효능에서 차별성이 확인됐다는 설명이다. 또한 12주 이상 구조적·기능적 안정성과 함께 약동학(PK) 및 내약성에서도 양호한 프로파일을 보였다.
앱클론은 해당 데이터가 전립선암 치료에서 4-1BB 기반 면역항암제의 독성 한계를 회피하면서 효능을 확보할 수 있는 설계 가능성을 시사한다고 설명했다.
이어 공개된 zCAR-T는 스위처블(Switchable) 구조를 적용한 차세대 CAR-T 플랫폼이다. 외부에서 투여하는 ‘스위치’ 물질을 통해 CAR-T 활성도를 조절하는 방식이다. 기존 CAR-T가 고형암에서 보인 사이토카인 방출증후군(CRS) 및 TME 장벽 문제를 구조적으로 보완하는 접근이다.
발표 데이터에 따르면, zCAR-T는 스위치 투여 조건에서 항암 효능을 유지하면서, 신규 표적 스위치를 통해 종양세포뿐 아니라 종양미세환경까지 조절할 수 있는 가능성을 확인했다. 단일 항원 인식 구조를 넘어 다중 표적 및 미세환경 개입까지 확장되는 설계다.
앱클론은 zCAR-T 파이프라인 중 ‘AT501’의 국내 임상시험 진입을 추진할 계획이다. 전임상 단계에서 확보한 효능과 제어 가능성을 임상으로 확장하겠다는 전략이다.
회사 측은 “이번 AACR 발표는 zCAR-T와 AM109의 차별적 기전을 데이터로 입증한 자리”라며 “현지에서 다수의 파트너링 미팅을 진행 중이며, 기술이전 및 공동개발로 이어질 수 있도록 사업개발 역량을 집중하고 있다”고 밝혔다.
| 인기기사 | 더보기 + |
-
1 에이비엘바이오 'ABL001' 쇼크?…“핵심은 그랩바디 플랫폼” -
2 메지온, FDA 공식 의견 제출...폰탄치료제 ‘JURVIGO’ 승인 가속 -
3 에이비엘바이오-컴퍼스, 담도암 2차 ‘토베시미그’ 2/3상 '무진행생존기간 개선' 확인 -
4 상장 제약·바이오 2025년 평균 자기자본이익률 코스피 0.30%·코스닥 -2.57% -
5 네이처셀,미국FDA 승인 알츠하이머병 임상 2b상 본격 개시 -
6 상장 제약·바이오 2025년 지배지분순이익 코스피 834억원·코스닥 72억원 -
7 “간의 벽 깨졌다” 올릭스 2.0, 비만·CNS siRNA 신약개발 드라이브 -
8 “조건부 허가 아니다” 큐로셀 CAR-T ‘림카토주’ 3상 없이 정식 허가된 이유 -
9 OLSS 서밋 2026, K-바이오 글로벌 도약의 산실로… 글로벌 창업 허브 향한 퀀텀 점프 -
10 경구 GLP-1 시장 개막…노보 ‘선점’, 릴리 ‘추격’
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 권혁진 기자 hjkwon@yakup.com
- 입력 2026.04.21 15:07

앱클론이 AACR 2026에서 차세대 고형암 CAR-T와 이중항체 플랫폼을 동시에 공개하며 전임상 데이터 경쟁력을 제시했다. 핵심은 ‘초저용량에서도 완전 종양 억제’와 ‘종양미세환경(TME) 제어’다. 고형암 CAR-T의 구조적 한계를 겨냥한 플랫폼 설계가 실제 데이터로 연결됐다는 점에 의미가 있다.
항체 신약개발 기업 앱클론은 미국 샌디에이고에서 열린 미국암연구학회(AACR) 2026에서 차세대 항암 플랫폼 ‘zCAR-T’와 전립선암 타깃 이중항체 ‘AM109’ 연구 결과를 포스터로 발표했다고 21일 밝혔다.
이번 발표에서 먼저 공개된 AM109는 자사 이중항체 플랫폼 ‘어피맵(AffiMab)’ 기반 후보물질이다. 전립선암 표적 PSMA와 T세포 공동자극 수용체 4-1BB(CD137)를 동시에 겨냥하는 구조다. 종양미세환경 내 PSMA 발현 세포가 존재할 때만 T세포를 활성화하는 타깃 의존적 기전이 핵심이다.
전임상 결과, AM109는 0.1~0.3 mg/kg(체중당 투여량) 수준의 저용량에서도 종양의 완전 관해(complete tumor regression)를 유도했다. 동일 계열 4-1BB 작용제인 우토밀루맙 대비 항암 효능에서 차별성이 확인됐다는 설명이다. 또한 12주 이상 구조적·기능적 안정성과 함께 약동학(PK) 및 내약성에서도 양호한 프로파일을 보였다.
앱클론은 해당 데이터가 전립선암 치료에서 4-1BB 기반 면역항암제의 독성 한계를 회피하면서 효능을 확보할 수 있는 설계 가능성을 시사한다고 설명했다.
이어 공개된 zCAR-T는 스위처블(Switchable) 구조를 적용한 차세대 CAR-T 플랫폼이다. 외부에서 투여하는 ‘스위치’ 물질을 통해 CAR-T 활성도를 조절하는 방식이다. 기존 CAR-T가 고형암에서 보인 사이토카인 방출증후군(CRS) 및 TME 장벽 문제를 구조적으로 보완하는 접근이다.
발표 데이터에 따르면, zCAR-T는 스위치 투여 조건에서 항암 효능을 유지하면서, 신규 표적 스위치를 통해 종양세포뿐 아니라 종양미세환경까지 조절할 수 있는 가능성을 확인했다. 단일 항원 인식 구조를 넘어 다중 표적 및 미세환경 개입까지 확장되는 설계다.
앱클론은 zCAR-T 파이프라인 중 ‘AT501’의 국내 임상시험 진입을 추진할 계획이다. 전임상 단계에서 확보한 효능과 제어 가능성을 임상으로 확장하겠다는 전략이다.
회사 측은 “이번 AACR 발표는 zCAR-T와 AM109의 차별적 기전을 데이터로 입증한 자리”라며 “현지에서 다수의 파트너링 미팅을 진행 중이며, 기술이전 및 공동개발로 이어질 수 있도록 사업개발 역량을 집중하고 있다”고 밝혔다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
