면역항암제 불응 종양 모델 90% 이상 종양 성장 억제.."설계부터 전임상 검증까지 자체 수행"
 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
AI 신약개발 기업 갤럭스(대표이사 석차옥)는 미국암연구학회(AACR 2026)에서 자사 AI 단백질 설계 기술을 적용한 이중항체 신약 후보물질 ‘PD-1/IL-18v’ 전임상 연구 결과를 포스터 발표 예정이라고 15일 밝혔다. 이번 연구는 기존 면역항암제의 한계를 개선할 가능성을 제시했다는 점에서 주목된다.
해당 연구는 강력한 항암 효과에도 불구하고 심각한 전신 면역활성 부작용으로 활용이 제한돼 온 사이토카인(Cytokine)과, 반응률이 낮은 기존 PD-1 기반 면역항암제 한계를 동시 겨냥했다. 갤럭스는 AI 기술을 활용해 이러한 한계를 개선할 수 있는 설계 전략과 전임상 검증 결과를 공개했다.
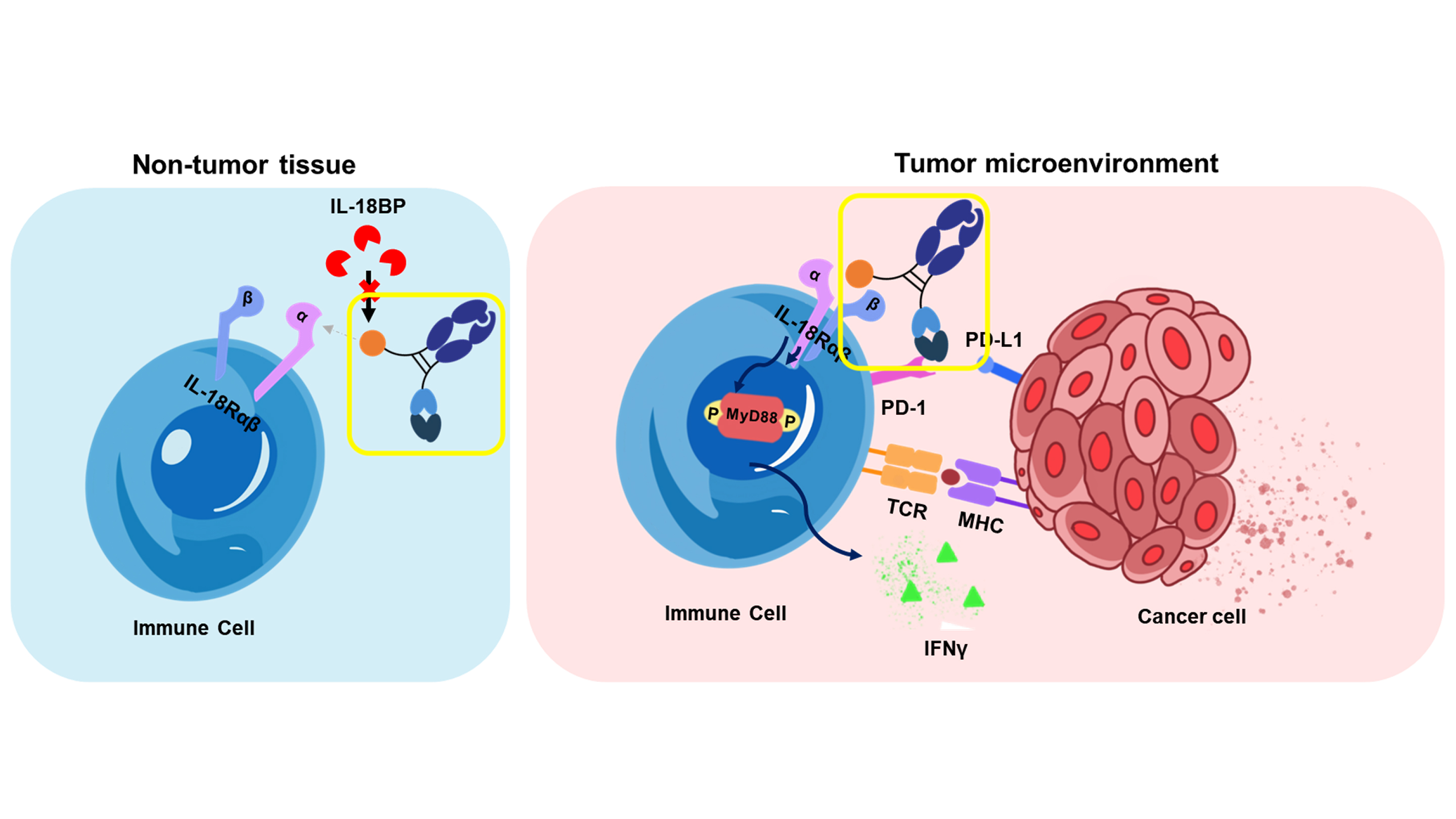
사이토카인은 면역세포 간 신호를 전달하는 단백질로, 이 가운데 인터루킨-18(IL-18)은 암을 공격하는 면역세포를 활성화할 수 있는 유망한 물질로 평가된다. 그러나 체내 투여 시 억제 단백질인 IL-18BP에 의해 쉽게 비활성화되고, 과량 투여 시 전신 염증 등 독성 유발 위험이 커 치료제로 활용은 한계가 있었다.
갤럭스는 자체 AI 단백질 설계 플랫폼 ‘갤럭스디자인(GaluxDesign)’을 활용해 IL-18 구조와 상호작용을 정밀 분석하고, 기존 단백질을 재설계한 IL-18 변이체 (IL-18v)를 개발했다. 이 변이체는 IL-18BP에 의한 억제를 회피하는 동시에 활성을 낮춰, 단독으로는 면역세포를 거의 활성화하지 않도록 설계됐다. 대신 PD-1 항체와 결합 시 종양 미세환경 내 PD-1 발현 면역세포에만 선택적으로 활성화되도록 했다.
해당 변이체를 PD-1 항체와 융합한 PD-1/IL-18v 이중항체는 PD-1 비발현 세포에서는 거의 신호 활성을 보이지 않았지만, PD-1 발현 세포에서는 1,000배 이상 높은 활성을 나타내며 종양 특이적인 면역 반응을 유도했다.
동물실험에서도 긍정적인 결과가 확인됐다. 기존 PD-1 면역항암제로 충분한 효과를 보이지 않던 불응 종양 모델에서 90% 이상 종양 감소가 관찰됐으며, 반복 투여에도 유의한 체중 변화가 나타나지 않아 전신 독성 우려가 낮은 것으로 확인됐다.
회사는 이번 연구는 AI를 활용해 기존 생체 분자의 복합적 한계를 개선한 치료제 후보를 구현할 수 있음을 보여줬다는 점에서 의미가 있다고 설명했다. 더 나아가 효능과 부작용 개선에 그치지 않고 생체 분자의 안정성과 발현성까지 높여, AI 기반 설계를 통해 후보물질의 개발 적합성까지 높일 수 있음을 제시했다고 밝혔다.
갤럭스 박태용 부사장은 “이번 연구는 단백질 설계 AI를 활용해 생체 분자 성질을 복합적으로 최적화함으로써 기존 면역항암 치료 한계를 개선할 수 있는 가능성을 보여준 결과”라며 “갤럭스는 AI개발 역량 뿐 아니라 이를 활용한 신약 후보물질 설계와 검증까지 자체 수행할 수 있는 역량을 갖추고 있다”고 밝혔다. 이어 “이를 기반으로 차별화된 파이프라인을 지속적으로 확대해 나갈 것”이라고 덧붙였다.

- 이권구 기자 kwon9@yakup.com
- 입력 2026.04.15 08:54 수정 2026.04.15 09:00
AI 신약개발 기업 갤럭스(대표이사 석차옥)는 미국암연구학회(AACR 2026)에서 자사 AI 단백질 설계 기술을 적용한 이중항체 신약 후보물질 ‘PD-1/IL-18v’ 전임상 연구 결과를 포스터 발표 예정이라고 15일 밝혔다. 이번 연구는 기존 면역항암제의 한계를 개선할 가능성을 제시했다는 점에서 주목된다.
해당 연구는 강력한 항암 효과에도 불구하고 심각한 전신 면역활성 부작용으로 활용이 제한돼 온 사이토카인(Cytokine)과, 반응률이 낮은 기존 PD-1 기반 면역항암제 한계를 동시 겨냥했다. 갤럭스는 AI 기술을 활용해 이러한 한계를 개선할 수 있는 설계 전략과 전임상 검증 결과를 공개했다.

사이토카인은 면역세포 간 신호를 전달하는 단백질로, 이 가운데 인터루킨-18(IL-18)은 암을 공격하는 면역세포를 활성화할 수 있는 유망한 물질로 평가된다. 그러나 체내 투여 시 억제 단백질인 IL-18BP에 의해 쉽게 비활성화되고, 과량 투여 시 전신 염증 등 독성 유발 위험이 커 치료제로 활용은 한계가 있었다.
갤럭스는 자체 AI 단백질 설계 플랫폼 ‘갤럭스디자인(GaluxDesign)’을 활용해 IL-18 구조와 상호작용을 정밀 분석하고, 기존 단백질을 재설계한 IL-18 변이체 (IL-18v)를 개발했다. 이 변이체는 IL-18BP에 의한 억제를 회피하는 동시에 활성을 낮춰, 단독으로는 면역세포를 거의 활성화하지 않도록 설계됐다. 대신 PD-1 항체와 결합 시 종양 미세환경 내 PD-1 발현 면역세포에만 선택적으로 활성화되도록 했다.
해당 변이체를 PD-1 항체와 융합한 PD-1/IL-18v 이중항체는 PD-1 비발현 세포에서는 거의 신호 활성을 보이지 않았지만, PD-1 발현 세포에서는 1,000배 이상 높은 활성을 나타내며 종양 특이적인 면역 반응을 유도했다.
동물실험에서도 긍정적인 결과가 확인됐다. 기존 PD-1 면역항암제로 충분한 효과를 보이지 않던 불응 종양 모델에서 90% 이상 종양 감소가 관찰됐으며, 반복 투여에도 유의한 체중 변화가 나타나지 않아 전신 독성 우려가 낮은 것으로 확인됐다.
회사는 이번 연구는 AI를 활용해 기존 생체 분자의 복합적 한계를 개선한 치료제 후보를 구현할 수 있음을 보여줬다는 점에서 의미가 있다고 설명했다. 더 나아가 효능과 부작용 개선에 그치지 않고 생체 분자의 안정성과 발현성까지 높여, AI 기반 설계를 통해 후보물질의 개발 적합성까지 높일 수 있음을 제시했다고 밝혔다.
갤럭스 박태용 부사장은 “이번 연구는 단백질 설계 AI를 활용해 생체 분자 성질을 복합적으로 최적화함으로써 기존 면역항암 치료 한계를 개선할 수 있는 가능성을 보여준 결과”라며 “갤럭스는 AI개발 역량 뿐 아니라 이를 활용한 신약 후보물질 설계와 검증까지 자체 수행할 수 있는 역량을 갖추고 있다”고 밝혔다. 이어 “이를 기반으로 차별화된 파이프라인을 지속적으로 확대해 나갈 것”이라고 덧붙였다.
무단 전재·복사·배포 등을 금지합니다.



