
세계 최초 MASH(대사이상 관련 지방간염) 치료제 탄생이 눈앞으로 다가왔다. 마드리갈 파마슈티컬스(Madrigal Pharmaceuticals)의 MASH 신약후보 '레스메티롬(Resmetirom)'이 그 주인공이다. FDA는 늦어도 오는 3월 14일까지 레스메티롬의 승인 여부를 결정해야 한다. 신약으로 확정되면 최대 30조원의 새로운 MASH 시장이 열린다.
MASH는 기존에는 'NASH(비알콜성 지방간염)'라는 명칭으로 사용됐다. 지난해 11월 글로벌 주요 간 학회에서 공동 입장문을 통해 43년 만에 명칭 변경을 알렸다. MSAH는 기존 NASH와 동일하게 술로 인해 발병되는 지방간과 달리, 비만과 당뇨병과 같이 대사과정의 이상으로 발병하는 지방간염을 가리킨다. MASH는 간 관련 사망의 주요 원인으로 간경변과 간암 발병률을 크게 증가시키는 중대한 질환이다. 그러나 현재 치료제는 전무한 실정이다.
시장조사 기관 글로벌데이터에 따르면 글로벌 MASH 치료 시장은 2026년 253억 달러(33조7375억원) 규모에 이를 전망이다. 특히 MASH 환자는 지속해서 증가하는 추세다. 건강보험심사평가원은 2021년 기준 국내에만 40만5950명의 MASH 환자가 집계돼 5년 사이 40% 이상 증가했다고 밝혔다. 현재 전 세계 MASH 환자 수는 약 4억4000만명 이상으로 추산되고 있다.
업계 관계자는 16일 “최근 ADC, AI 열풍에 MASH 치료제 탄생의 중요성이 상대적으로 가려져 있다”면서 “MASH 치료제는 고혈압, 제2형 당뇨병 치료제와 같이 엄청난 시장성을 가진 치료제”라고 강조했다.
마드리갈 파마슈티컬스는 MASH 신약후보 레스메티롬의 임상시험 3상을 마치고, 현재 FDA 사용 승인을 기다리고 있다. 레스메티롬은 지난해 9월 13일(현지시간) FDA 신속심사 대상으로 지정됐다. 신속심사 대상으로 지정되면 전문의약품 이용자부담금법(PDUFA, Prescription Drug User Fee Act)에 따라 FDA는 6개월 안에 심사를 마쳐야 한다.
업계에선 레스메티롬의 승인 가능성을 높게 보고 있다. 레스메티롬이 임상시험에서 보인 우수한 안전성 및 유효성 데이터와 이를 FDA에서도 인정해 신속심사 대상으로 지정했다는 이유에서다.
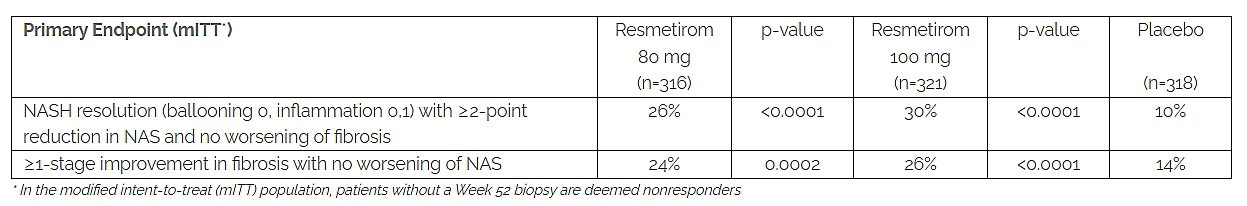
실제 마드리갈 파마슈티컬스는 1000여명에 달하는 인원이 참여하는 대규모 임상 3상인 'MAESTRO-NASH Trial'를 성공했다. 해당 임상은 조직학적 △주요결과변수(Primary Outcome Measures) NASH 해소(NASH Resolution)와 △보조결과변수(Secondary Outcome Measures) 간 섬유화 지표 개선 사항을 모두 충족, △1차평가변수(Primary Endpoint)에서 통계적 유의성을 달성했다. 이 외에도 마드리갈 파카슈티컬스는 임상 3상 3건을 진행했고, 여기에서도 안전성과 유효성이 긍정적으로 확인됐다.
업계 관계자는 “레스메티롬이 최종적으로 FDA 승인을 획득할지는 장담할 수 없으나, 미충족 의료 수요가 큰 질환을 해결할 치료제가 탄생하기를 기대하고 있다"고 말했다. 이어 그는 "MASH가 비만과 같은 대사증후군과 연관성이 크다 보니, 비만치료제에서도 MASH 치료 효과가 입증되고 있다”면서 “향후 GLP-1 계열 비만치료제가 적응증을 MASH 치료로 확장할 가능성도 크다”고 전했다.
한편 국내 기업 중에선 한미약품이 임상 2b상 단계에 MASH 신약 파이프라인(HM12525A, HM15211)을 개발 중으로 가장 앞서 있다. 이 밖에도 동아에스티(DA-1241, 임상 2상), 유한양행(YH25724, 임상 1상), 올릭스(OLX7501, 임상 1상)가 MASH 치료제를 개발 중이다.
| 인기기사 | 더보기 + |
-
1 “조건부 허가 아니다” 큐로셀 CAR-T ‘림카토주’ 3상 없이 정식 허가된 이유 -
2 100만 바이오 빅데이터 문 열린다… '의료 AI·신약' 대도약 시대 개막 -
3 유통업계, 대웅 압박 국회로…5월 국회 릴레이 1인 시위 돌입 -
4 “2029년, 매출 10억 달러” SK바이오팜, 엑스코프리 성공과 미래 전략 제시 -
5 FDA, 암젠 희귀질환 치료제 허가 취소 압박…‘데이터 조작’ 직접 언급 -
6 중국 제약사 세계 최초 재조합 보툴리눔 독소 개발 -
7 "비만, GLP-1 이후를 본다” 한국투자파트너스, 스웨덴 바이오텍에 베팅한 이유 -
8 임상 규제 허문다… 복지부, 시범사업 넘어 '분산형 임상' 전격 제도화 -
9 화이자, ‘빈다맥스’ 제네릭 2031년까지 봉쇄…ATTR-CM 시장 주도권 경쟁 격화 -
10 EU 포장규제 8월 시행…K-뷰티도 준비해야
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 권혁진 기자 hjkwon@yakup.com
- 입력 2024.01.17 06:00 수정 2024.01.17 06:01

세계 최초 MASH(대사이상 관련 지방간염) 치료제 탄생이 눈앞으로 다가왔다. 마드리갈 파마슈티컬스(Madrigal Pharmaceuticals)의 MASH 신약후보 '레스메티롬(Resmetirom)'이 그 주인공이다. FDA는 늦어도 오는 3월 14일까지 레스메티롬의 승인 여부를 결정해야 한다. 신약으로 확정되면 최대 30조원의 새로운 MASH 시장이 열린다.
MASH는 기존에는 'NASH(비알콜성 지방간염)'라는 명칭으로 사용됐다. 지난해 11월 글로벌 주요 간 학회에서 공동 입장문을 통해 43년 만에 명칭 변경을 알렸다. MSAH는 기존 NASH와 동일하게 술로 인해 발병되는 지방간과 달리, 비만과 당뇨병과 같이 대사과정의 이상으로 발병하는 지방간염을 가리킨다. MASH는 간 관련 사망의 주요 원인으로 간경변과 간암 발병률을 크게 증가시키는 중대한 질환이다. 그러나 현재 치료제는 전무한 실정이다.
시장조사 기관 글로벌데이터에 따르면 글로벌 MASH 치료 시장은 2026년 253억 달러(33조7375억원) 규모에 이를 전망이다. 특히 MASH 환자는 지속해서 증가하는 추세다. 건강보험심사평가원은 2021년 기준 국내에만 40만5950명의 MASH 환자가 집계돼 5년 사이 40% 이상 증가했다고 밝혔다. 현재 전 세계 MASH 환자 수는 약 4억4000만명 이상으로 추산되고 있다.
업계 관계자는 16일 “최근 ADC, AI 열풍에 MASH 치료제 탄생의 중요성이 상대적으로 가려져 있다”면서 “MASH 치료제는 고혈압, 제2형 당뇨병 치료제와 같이 엄청난 시장성을 가진 치료제”라고 강조했다.
마드리갈 파마슈티컬스는 MASH 신약후보 레스메티롬의 임상시험 3상을 마치고, 현재 FDA 사용 승인을 기다리고 있다. 레스메티롬은 지난해 9월 13일(현지시간) FDA 신속심사 대상으로 지정됐다. 신속심사 대상으로 지정되면 전문의약품 이용자부담금법(PDUFA, Prescription Drug User Fee Act)에 따라 FDA는 6개월 안에 심사를 마쳐야 한다.
업계에선 레스메티롬의 승인 가능성을 높게 보고 있다. 레스메티롬이 임상시험에서 보인 우수한 안전성 및 유효성 데이터와 이를 FDA에서도 인정해 신속심사 대상으로 지정했다는 이유에서다.

실제 마드리갈 파마슈티컬스는 1000여명에 달하는 인원이 참여하는 대규모 임상 3상인 'MAESTRO-NASH Trial'를 성공했다. 해당 임상은 조직학적 △주요결과변수(Primary Outcome Measures) NASH 해소(NASH Resolution)와 △보조결과변수(Secondary Outcome Measures) 간 섬유화 지표 개선 사항을 모두 충족, △1차평가변수(Primary Endpoint)에서 통계적 유의성을 달성했다. 이 외에도 마드리갈 파카슈티컬스는 임상 3상 3건을 진행했고, 여기에서도 안전성과 유효성이 긍정적으로 확인됐다.
업계 관계자는 “레스메티롬이 최종적으로 FDA 승인을 획득할지는 장담할 수 없으나, 미충족 의료 수요가 큰 질환을 해결할 치료제가 탄생하기를 기대하고 있다"고 말했다. 이어 그는 "MASH가 비만과 같은 대사증후군과 연관성이 크다 보니, 비만치료제에서도 MASH 치료 효과가 입증되고 있다”면서 “향후 GLP-1 계열 비만치료제가 적응증을 MASH 치료로 확장할 가능성도 크다”고 전했다.
한편 국내 기업 중에선 한미약품이 임상 2b상 단계에 MASH 신약 파이프라인(HM12525A, HM15211)을 개발 중으로 가장 앞서 있다. 이 밖에도 동아에스티(DA-1241, 임상 2상), 유한양행(YH25724, 임상 1상), 올릭스(OLX7501, 임상 1상)가 MASH 치료제를 개발 중이다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
