간세포암 대상 면역항암제 병용 치료 가능성 평가
 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기

압타머사이언스(대표이사 정집훈)는 자사 항암 후보물질 AST-201과 MSD(미국 Merck & Co., Inc.)의 항-PD-1 치료제 키트루다(KEYTRUDA®, 성분명: 펨브롤리주맙) 병용요법을 평가하기 위해 MSD와 임상시험 협력 및 의약품 공급 계약(Clinical Trial Collaboration and Supply Agreement, CTCSA)을 체결했다고 15일 밝혔다.
이 계약 조건에 따라 압타머사이언스는 AST-201과 키트루다의 병용 투여 가능성을 평가하기 위한 임상 2상 시험을 진행하고, MSD는 임상시험에 사용될 키트루다를 공급하며 임상시험 수행 과정에서 과학적으로 협력한다.
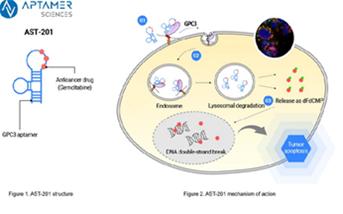
AST-201은 GPC3 (Glypican-3)를 표적으로 하는 압타머-약물접합체(ApDC®) 기반 항암 신약 후보물질로, 간세포암을 포함한 GPC3 발현 고형암을 주요 적응증으로 개발 중이다. GPC3는 간세포암 환자 다수에서 발현되는 종양 특이 항원으로 알려져 있어, 표적 치료 전략 측면에서 임상적 의미가 있는 바이오마커로 평가된다.
현재 압타머사이언스는 AST-201 단독요법에 대한 임상 1상을 진행 중이며(NCT06687941), 계획된 용량 증량 코호트에 따라 안전성 및 약동학(PK)을 중심으로 임상 데이터를 축적하고 있다. 현재까지 임상 진행 과정에서 중대한 안전성 이슈는 관찰되지 않았으며, 임상적으로 관리 가능한 수준의 이상반응이 확인되고 있다.
회사는 임상 1상 진행 현황을 토대로, 이번 MSD와 협력을 통해 면역항암제 병용 전략에 대한 임상적 확장 가능성을 단계적으로 평가할 계획이다. 종양세포 표적 치료에 따른 종양미세환경 변화가 면역항암제 반응성을 향상시킬 수 있다는 과학적 근거에 기반해, AST-201과 키트루다 병용요법 임상적 유효성과 안전성을 탐색한다는 전략이다.
압타머사이언스는 이번 CTCSA 체결을 AST-201 임상 개발 과정에서 의미 있는 마일스톤으로 평가하고 있다. 단독요법 중심 초기 임상 단계에서 한 단계 나아가, 글로벌 표준 면역항암제와 병용 임상 개발 단계로 진입했다는 점에서 개발 전략상 중요한 전환점이라는 설명이다.
특히 해당 계약은 압타머사이언스가 스폰서로서 병용 임상시험을 수행하면서 키트루다 같은 글로벌 표준 면역항암제를 활용할 수 있는 협력 기반을 확보했다는 점에서 의미가 있다고 회사 측은 설명했다. 이는 AST-201의 기전적 타당성과 초기 임상 진행 현황을 바탕으로 병용 임상 개발이 추진된 결과로, 회사는 이이를 통해 AST-201의 치료적 잠재력을 보다 폭넓은 임상 환경에서 검증할 수 있을 것으로 기대하고 있다.
회사 관계자는 “ 향후 이 병용 임상시험을 통해 축적되는 데이터를 기반으로, AST-201의 임상적 포지셔닝과 중장기 개발 방향을 단계적으로 검토해 나갈 계획”이라고 전했다.
| 인기기사 | 더보기 + |
-
1 한미약품,GLP-1 비만신약 '에페' 우여곡절 끝 연내 상용화 착수 -
2 코로나19 신변이 'BA.3.2(매미)' 확산…유전체 분석 기업 셀레믹스 재조명 -
3 첫 국가바이오혁신위원회 회의서 나온 ‘말말말’ -
4 셀루메드, 이상인 경영지배인 선임 -
5 릴리, '파운다요' 안전성 논란 반격…임상 통한 안전성 입증 나서 -
6 국내 신약 파이프라인 2162개 '역대 최대'…'글로벌 갭' 줄일 넥스트 모달리티 관건 -
7 다이이산쿄, OTC 사업 매각…항암 중심 전환 -
8 [DIA 2026] “AI는 선택 아닌 필수”…식약처 규제과학 혁신 전략 공개 -
9 큐로셀, 727억원 규모 대규모 자금 조달 -
10 생존율 떨어진 인디 뷰티…해답은 'IR'과 '더마핏'
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 이권구 기자 kwon9@yakup.com
- 입력 2026.04.15 08:32 수정 2026.04.15 08:37

압타머사이언스(대표이사 정집훈)는 자사 항암 후보물질 AST-201과 MSD(미국 Merck & Co., Inc.)의 항-PD-1 치료제 키트루다(KEYTRUDA®, 성분명: 펨브롤리주맙) 병용요법을 평가하기 위해 MSD와 임상시험 협력 및 의약품 공급 계약(Clinical Trial Collaboration and Supply Agreement, CTCSA)을 체결했다고 15일 밝혔다.
이 계약 조건에 따라 압타머사이언스는 AST-201과 키트루다의 병용 투여 가능성을 평가하기 위한 임상 2상 시험을 진행하고, MSD는 임상시험에 사용될 키트루다를 공급하며 임상시험 수행 과정에서 과학적으로 협력한다.
AST-201은 GPC3 (Glypican-3)를 표적으로 하는 압타머-약물접합체(ApDC®) 기반 항암 신약 후보물질로, 간세포암을 포함한 GPC3 발현 고형암을 주요 적응증으로 개발 중이다. GPC3는 간세포암 환자 다수에서 발현되는 종양 특이 항원으로 알려져 있어, 표적 치료 전략 측면에서 임상적 의미가 있는 바이오마커로 평가된다.
현재 압타머사이언스는 AST-201 단독요법에 대한 임상 1상을 진행 중이며(NCT06687941), 계획된 용량 증량 코호트에 따라 안전성 및 약동학(PK)을 중심으로 임상 데이터를 축적하고 있다. 현재까지 임상 진행 과정에서 중대한 안전성 이슈는 관찰되지 않았으며, 임상적으로 관리 가능한 수준의 이상반응이 확인되고 있다.
회사는 임상 1상 진행 현황을 토대로, 이번 MSD와 협력을 통해 면역항암제 병용 전략에 대한 임상적 확장 가능성을 단계적으로 평가할 계획이다. 종양세포 표적 치료에 따른 종양미세환경 변화가 면역항암제 반응성을 향상시킬 수 있다는 과학적 근거에 기반해, AST-201과 키트루다 병용요법 임상적 유효성과 안전성을 탐색한다는 전략이다.
압타머사이언스는 이번 CTCSA 체결을 AST-201 임상 개발 과정에서 의미 있는 마일스톤으로 평가하고 있다. 단독요법 중심 초기 임상 단계에서 한 단계 나아가, 글로벌 표준 면역항암제와 병용 임상 개발 단계로 진입했다는 점에서 개발 전략상 중요한 전환점이라는 설명이다.
특히 해당 계약은 압타머사이언스가 스폰서로서 병용 임상시험을 수행하면서 키트루다 같은 글로벌 표준 면역항암제를 활용할 수 있는 협력 기반을 확보했다는 점에서 의미가 있다고 회사 측은 설명했다. 이는 AST-201의 기전적 타당성과 초기 임상 진행 현황을 바탕으로 병용 임상 개발이 추진된 결과로, 회사는 이이를 통해 AST-201의 치료적 잠재력을 보다 폭넓은 임상 환경에서 검증할 수 있을 것으로 기대하고 있다.
회사 관계자는 “ 향후 이 병용 임상시험을 통해 축적되는 데이터를 기반으로, AST-201의 임상적 포지셔닝과 중장기 개발 방향을 단계적으로 검토해 나갈 계획”이라고 전했다.

무단 전재·복사·배포 등을 금지합니다.



