지난해 마지막까지 더 우수한 의약품을 개발하기 위한 도전이 이어졌다. 식품의약품안전처가 2023년 12월 승인한 IND(임상시험계획승인신청서) 중 국내 기업 네 곳이 포함돼 있다. 이들은 새로운 모달리티 기반의 항암제와 탈모치료제, 더불어 인플루엔자 백신 개발에 나섰다.
약업닷컴(약업신문)이 3일 한국바이오의약품협회 산업동향정보와 식약처 의약품통합정보시스템 자료를 분석한 결과, 지난해 12월 한 달간(1일~31일) 바이오의약품 IND는 총 12건 승인됐다. 전체 승인된 IND 중 임상 3상이 7건으로 가장 많았고, 1상 4건(1/2a상 포함)과 2상 1건 순으로 집계됐다.
임상 3상 승인을 받은 기업 중 국내 기업으로는 일양약품이 유일하다. 영유아 대상 인플루엔자 분할백신(Split vaccine) 개발을 위한 3상 승인을 받았다. 이 외 다국적 기업 △한국엠에스디 △아이콘클리니컬리서치코리아(CRO, 임상시험수탁기관) △한국아이큐비아(CRO) △알렉시온파마 △사노피-아벤티스 코리아가 3상을 승인받았다. 이 밖에 국내 기업은 △에피바이오텍(1/2a상) △지씨셀(1상) △알지노믹스(1/2a상)가 임상 단계에 진입했다.
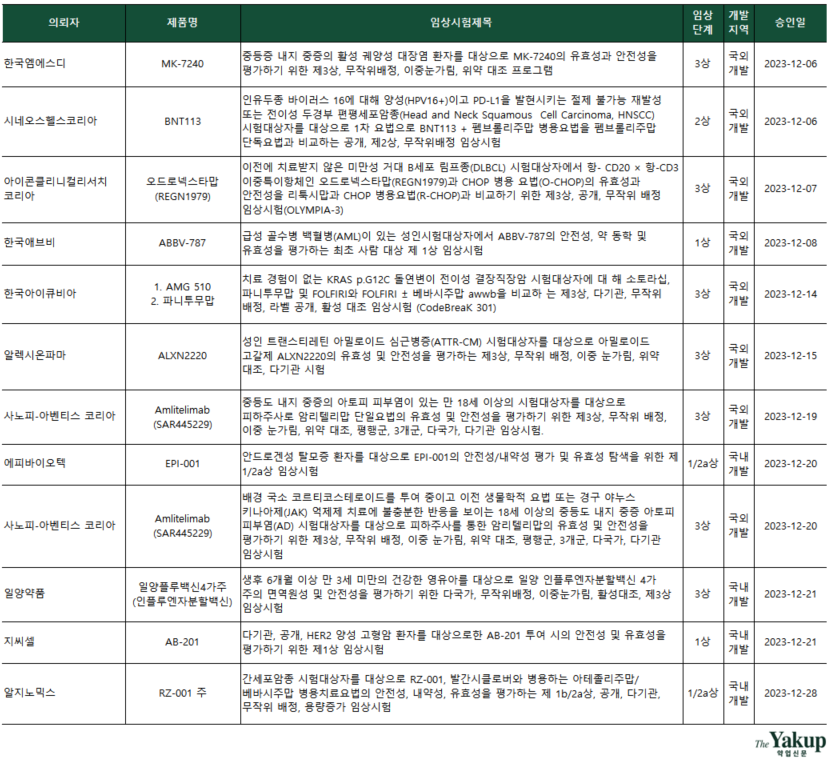
이달엔 항종양 관련 임상시험이 6건 승인됐으며, 국내기업 지씨셀과 알지노믹스가 고형암을 타깃하는 임상시험을 승인받았다.
지씨셀은 고형암의 대표적인 표적 인자 HER2(인간상피세포 증식인자 수용체 2형)를 타깃하는 CAR-NK 세포치료제 ‘AB-201’ 임상 1상을 승인받았다. 특히 AB-201은 국내 최초의 동종(Allogenic)유래 CAR-NK 세포치료제로 개발 중이다. 지씨셀은 국내와 호주에서 HER2 과발현 유방암, 위암 및 위식도접합부암 환자를 대상으로 임상을 진행할 계획이다. 이 임상에선 안전성과 함께 유효성 일부를 평가할 예정이다.
동종유래 치료제는 자신의 조직을 기반으로 제작된 자가유래(Autologous) 치료제 대비 활용성이 큰 것이 강점이다. 일반적인 의약품과 같이 미리 제조된 의약품을 필요할 때 바로 사용할 수 있고, 대량생산과 수출도 가능해 경제성이 높다. CAR-T 치료제로 대표적인 킴리아도 자가유래, 개인 맞춤형 치료제 한계로 건강보험 급여 적용 대상 이전 가격이 1회당 4억6000만원에 달했다.
알지노믹스는 고형암 중 간암치료제로 개발 중인 ‘RZ-001’의 임상 1/2a상을 승인받았다. RZ-001는 아데노바이러스(Adenovirus) 벡터로 리보핵산 치환효소(RNA trans-splicing ribozyme)를 전달, 암세포에 특이적으로 발현하는 텔로머레이스(hTERT) RNA를 표적하면서, 동시에 항암 작용을 유도하는 유전자를 발현시켜 암세포를 사멸하는 효과를 보인다.
알지노믹스는 이번 임상에서 간암의 1차 표준치료제인 티센트릭(아테졸리주맙)과 아바스틴(베바시주맙) 병용요법에 RZ-001을 추가로 병용투여하는 방식으로 진행할 예정이다. 또한 RZ-001은 지난해 5월 FDA로부터 악성교모세포종(뇌암)치료제 임상 1/2a상도 승인받았다. 특히 같은 해 11월 FDA로부터 패스트트랙(Fast Track)에 지정됐다. 이에 따라 RZ-001은 FDA로부터 더 신속한 허가과정을 지원받게 됐다.
또한 국내 기업 중 에피바이오텍이 안드로겐성 탈모증 치료제로 개발 중인 'EPI-001'의 1/2a상을 승인받았고, 이밖에 △궤양성 대장염 △아토피 피부염 △인플루엔자 백신 등을 적응증으로 하는 임상시험이 승인됐다.
이외에 아스트라제네카가 2021년 7월 인수한 알렉시온파마가 국내에서 희귀유전질환 신약개발에 나섰다. 알렉시온파마는 희귀유전질환 신약개발 전문 기업으로, 트랜스티레틴 아밀로이드 심근병증(ATTR-CM) 치료제 ‘ALXN2220’의 임상 3상을 승인받았다. 트랜스티레틴 아밀로이드 심근병증은 발병 시에 생존기간이 3년도 채 안 되는 중대 질환이다.

- 권혁진 기자 hjkwon@yakup.com
- 입력 2024.01.04 06:00 수정 2024.01.04 06:01

지난해 마지막까지 더 우수한 의약품을 개발하기 위한 도전이 이어졌다. 식품의약품안전처가 2023년 12월 승인한 IND(임상시험계획승인신청서) 중 국내 기업 네 곳이 포함돼 있다. 이들은 새로운 모달리티 기반의 항암제와 탈모치료제, 더불어 인플루엔자 백신 개발에 나섰다.
약업닷컴(약업신문)이 3일 한국바이오의약품협회 산업동향정보와 식약처 의약품통합정보시스템 자료를 분석한 결과, 지난해 12월 한 달간(1일~31일) 바이오의약품 IND는 총 12건 승인됐다. 전체 승인된 IND 중 임상 3상이 7건으로 가장 많았고, 1상 4건(1/2a상 포함)과 2상 1건 순으로 집계됐다.
임상 3상 승인을 받은 기업 중 국내 기업으로는 일양약품이 유일하다. 영유아 대상 인플루엔자 분할백신(Split vaccine) 개발을 위한 3상 승인을 받았다. 이 외 다국적 기업 △한국엠에스디 △아이콘클리니컬리서치코리아(CRO, 임상시험수탁기관) △한국아이큐비아(CRO) △알렉시온파마 △사노피-아벤티스 코리아가 3상을 승인받았다. 이 밖에 국내 기업은 △에피바이오텍(1/2a상) △지씨셀(1상) △알지노믹스(1/2a상)가 임상 단계에 진입했다.

이달엔 항종양 관련 임상시험이 6건 승인됐으며, 국내기업 지씨셀과 알지노믹스가 고형암을 타깃하는 임상시험을 승인받았다.
지씨셀은 고형암의 대표적인 표적 인자 HER2(인간상피세포 증식인자 수용체 2형)를 타깃하는 CAR-NK 세포치료제 ‘AB-201’ 임상 1상을 승인받았다. 특히 AB-201은 국내 최초의 동종(Allogenic)유래 CAR-NK 세포치료제로 개발 중이다. 지씨셀은 국내와 호주에서 HER2 과발현 유방암, 위암 및 위식도접합부암 환자를 대상으로 임상을 진행할 계획이다. 이 임상에선 안전성과 함께 유효성 일부를 평가할 예정이다.
동종유래 치료제는 자신의 조직을 기반으로 제작된 자가유래(Autologous) 치료제 대비 활용성이 큰 것이 강점이다. 일반적인 의약품과 같이 미리 제조된 의약품을 필요할 때 바로 사용할 수 있고, 대량생산과 수출도 가능해 경제성이 높다. CAR-T 치료제로 대표적인 킴리아도 자가유래, 개인 맞춤형 치료제 한계로 건강보험 급여 적용 대상 이전 가격이 1회당 4억6000만원에 달했다.
알지노믹스는 고형암 중 간암치료제로 개발 중인 ‘RZ-001’의 임상 1/2a상을 승인받았다. RZ-001는 아데노바이러스(Adenovirus) 벡터로 리보핵산 치환효소(RNA trans-splicing ribozyme)를 전달, 암세포에 특이적으로 발현하는 텔로머레이스(hTERT) RNA를 표적하면서, 동시에 항암 작용을 유도하는 유전자를 발현시켜 암세포를 사멸하는 효과를 보인다.
알지노믹스는 이번 임상에서 간암의 1차 표준치료제인 티센트릭(아테졸리주맙)과 아바스틴(베바시주맙) 병용요법에 RZ-001을 추가로 병용투여하는 방식으로 진행할 예정이다. 또한 RZ-001은 지난해 5월 FDA로부터 악성교모세포종(뇌암)치료제 임상 1/2a상도 승인받았다. 특히 같은 해 11월 FDA로부터 패스트트랙(Fast Track)에 지정됐다. 이에 따라 RZ-001은 FDA로부터 더 신속한 허가과정을 지원받게 됐다.
또한 국내 기업 중 에피바이오텍이 안드로겐성 탈모증 치료제로 개발 중인 'EPI-001'의 1/2a상을 승인받았고, 이밖에 △궤양성 대장염 △아토피 피부염 △인플루엔자 백신 등을 적응증으로 하는 임상시험이 승인됐다.
이외에 아스트라제네카가 2021년 7월 인수한 알렉시온파마가 국내에서 희귀유전질환 신약개발에 나섰다. 알렉시온파마는 희귀유전질환 신약개발 전문 기업으로, 트랜스티레틴 아밀로이드 심근병증(ATTR-CM) 치료제 ‘ALXN2220’의 임상 3상을 승인받았다. 트랜스티레틴 아밀로이드 심근병증은 발병 시에 생존기간이 3년도 채 안 되는 중대 질환이다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
