ALK7 표적 비만 치료, ‘지방 선택적 감량·근육 보존’ 체성분 개선 데이터 확보
CNS까지 확장…2026년 생체 내 개념 입증(in vivo PoC) 확보 목표


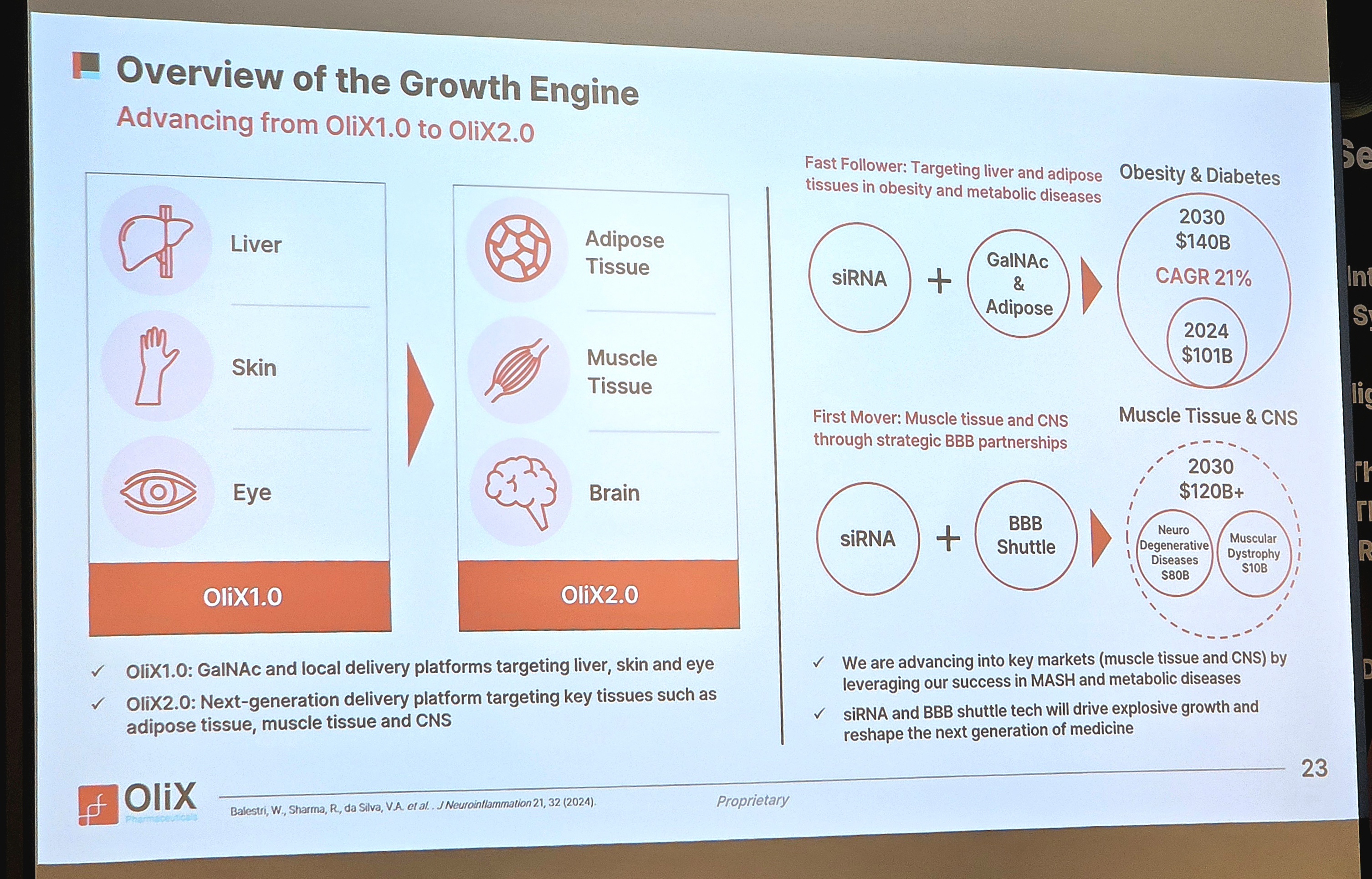
올릭스가 간 중심 RNA 간섭(RNAi) 치료제 개발에서 벗어나 비만 치료와 중추신경계(CNS)까지 확장하는 ‘올릭스 2.0’ 전략을 제시했다. 핵심은 간 외 조직으로 전달 범위를 넓히는 siRNA 플랫폼 ‘OASIS(OliX Advanced Small Interfering RNA System)’다. 기존 ‘GalNAc’ 기반 간 타깃 siRNA 전달 전략에서 한 단계 나아가, 지방·CNS 등 추가 조직으로 적용 영역을 확장하겠다는 전략이다.
올릭스 이동기 대표는 29일 서울 코엑스에서 열린 ‘바이오코리아 2026’ 컨퍼런스 세션 ‘올리고뉴클레오타이드 치료제’에 연사로 참석해 이 같은 전략을 발표했다.
이 대표는 “현재 상업화된 다수 siRNA 치료제가 GalNAc 기반 전달 기술을 활용해 간에 선택적으로 전달되는 구조에 머물러 있다”며 “OASIS는 siRNA에 지질 결합체(lipid conjugate)와 다양한 타깃 결합 구조를 적용해 지방조직이나 중추신경계와 같은 간 외 조직으로의 전달을 가능하게 하는 플랫폼”이라고 설명했다.
이어 그는 “단순히 전달되는 수준을 넘어, 특정 조직에서 의미 있는 수준의 유전자 발현 억제와 지속성을 동시에 확보한 것이 핵심”이라며 “이를 기반으로 siRNA 치료제를 간 질환 중심에서 대사질환, 신경퇴행성 질환 등으로 확장할 수 있는 개발 기반을 마련했다”고 강조했다. GalNAc은 간세포 표적 siRNA 전달에 쓰이는 리간드로, 미국 바이오텍 앨나일램 파마슈티컬스(Alnylam Pharmaceuticals)가 이를 기반으로 한 전달 기술을 상용화했다.
OASIS 플랫폼, 지방조직 전달 데이터로 ‘간 외 조직 확장’ 제시
OASIS는 올릭스의 기존 asiRNA 및 cp-asiRNA(자가전달 비대칭 siRNA) 기술을 기반으로 지질 결합체, GalNAc, 항체 등 다양한 전달 요소를 통합한 RNAi 플랫폼이다. siRNA 자체 설계 기술에 조직 특이적 전달 요소를 결합해, 기존 간 중심에서 지방·근육·중추신경계(CNS) 등 간 외 조직으로 적용 범위를 확장한 것이 특징이다.
상업화된 siRNA 치료제의 상당수가 GalNAc 기반 전달 기술을 통해 간에 선택적으로 축적되는 구조였다면, OASIS는 특정 조직을 표적으로 하는 전달 전략을 적용해 간 외 조직으로의 분포를 설계하는 플랫폼이다.
실제 비임상 연구에서 해당 플랫폼의 전달 성능이 확인됐다. 발표에 따르면, OASIS 플랫폼 기반 지방조직 표적 siRNA를 마우스에 피하 투여한 결과, 단회 3mg/kg 투여로 지방조직 내 표적 유전자 발현이 약 80% 감소했고, 해당 효과는 2개월 이상 유지됐다. 조직 분포 분석에서도 간 대비 지방조직에서 선택적인 mRNA 감소가 확인됐다.
이는 siRNA 치료제에서 핵심 과제로 꼽히던 조직 선택성과 지속성 측면에서 의미 있는 개선 가능성을 보여주는 데이터로 해석할 수 있다.
이 대표는 “지방조직에서 의미 있는 수준의 유전자 발현 억제와 지속성이 동시에 확인된 점이 중요하다”며 “해당 데이터는 siRNA 치료제의 적용 범위를 실제로 간 외 조직으로 확장할 수 있음을 보여준다”고 설명했다.
ALK7 표적 비만 신약개발 전략…“지방 선택적 감량”
올릭스는 OASIS 플랫폼을 기반으로 지방조직 표적 siRNA 전달 전략을 적용해 비만 치료제 ‘OLX501A’ 개발에 본격 착수했다.
핵심 타깃은 Activin receptor-like kinase 7(ALK7)이다. ALK7은 지방세포에서 지질 분해를 억제하고 에너지 저장을 조절하는 수용체로, 유전자 기능 저해 시 지방 축적이 감소하는 것으로 알려진 유전학적으로 검증된 타깃이다. 올릭스는 siRNA를 통해 ALK7 발현을 억제함으로써 지방조직 내 지질 분해를 촉진하는 접근을 적용하고 있다.
이 대표는 “ALK7 억제를 통해 지방세포의 대사를 저장 중심에서 소비 중심으로 전환하는 것이 핵심”이라며 “지방은 줄이면서 근육은 유지하는 방향의 치료 전략을 목표로 하고 있다”고 설명했다. 이어 “비만 치료제의 평가 기준이 단순 체중 감소에서 체성분 개선으로 이동할 가능성이 있다”고 덧붙였다.
실제 비임상 DIO(diet-induced obesity) 마우스 모델에서 ALK7 siRNA 후보물질은 체중 약 13% 감소를 유도했다. 동시에 지방량은 22.7~30.3% 감소한 반면, 제지방량은 유지되는 경향을 보였다. 단순 체중 감소가 아니라 지방량 감소 중심의 체성분 개선 효과가 확인된 것이다.
전임상 단계에서의 전환 가능성은 영장류 데이터에서도 확인됐다. ALK7 siRNA 후보물질 OLX501A는 비인간 영장류(NHP)에서 SC 3 mg/kg 단회 투여 시 최대 84% 수준의 ALK7 mRNA 감소를 나타냈다.
설치류를 넘어 영장류에서도 강력한 유전자 발현 억제 효과가 재현되면서, RNAi 기반 치료제 개발에서 주요 리스크로 꼽히는 종간 차이에 대한 부담을 일정 부분 낮출 수 있는 근거로 평가된다.
이 대표는 “siRNA 치료제에서 가장 중요한 것은 사람으로 얼마나 잘 이어질 수 있느냐”라며 “영장류 데이터는 그 가능성을 보여주는 핵심 지표로, 효능뿐 아니라 지속성과 용량 측면에서도 경쟁력을 확인하고 있다”고 강조했다.
CNS 확장 전략…“세포 내 타깃 공략” RNAi 강점 부각
올릭스 2.0 전략의 또 다른 방향은 중추신경계다. 회사는 siRNA 기반 치료제가 세포 내(intracellular) 타깃을 직접 억제할 수 있다는 점을 핵심 경쟁력으로 제시했다.
알츠하이머병, 파킨슨병 등 신경퇴행성 질환의 주요 병리 단백질인 타우, 알파-시누클레인은 세포 내 단백질이다. 항체 기반 치료제가 주로 세포 외(extracellular) 타깃에 제한되는 것과 달리, RNAi는 질병 기전에 직접 개입할 수 있는 접근이다.
올릭스는 전달 전략을 단계적으로 설계했다. 초기에는 척수강내(intrathecal) 투여를 통해 CNS 내 siRNA 전달 가능성을 검증하고, 이후 혈뇌장벽(BBB) 투과를 위해 트랜스페린 수용체(TfR1), IGF1R 등을 타깃으로 한 셔틀 기반 전달 기술을 적용하는 구조다. 현재 BBB 셔틀 기술은 외부 플랫폼 기업과의 협업을 통해 개발이 진행되고 있다.
비임상 단계에서는 설치류 모델에서 뇌 영역별 유전자 발현 억제 지속성이 확인됐다. 또한 파킨슨병 PFF(pre-formed fibril) 모델에서는 운동 기능 개선이 관찰되며, siRNA 기반 CNS 치료제의 초기 효능 가능성이 제시됐다.
이 대표는 “CNS 영역은 전달 자체가 가장 큰 장벽이지만, siRNA는 세포 내 타깃을 직접 조절할 수 있다는 점에서 기존 치료제와 차별화된다”며 “2026년 하반기 CNS 영역에서 생체 내 개념 입증(in vivo PoC)을 확보하는 것이 목표”라고 밝혔다.
현재 올릭스는 일라이 릴리와 MASH·비만 후보물질 ‘OLX702A’ 공동개발 및 기술이전 계약을 체결했으며, 한소제약과는 중화권에서 심혈관·대사 등 주요 적응증을 겨냥한 siRNA 치료제 개발·상업화 협력을 진행하고 있다. 로레알과는 RNAi 기술을 활용한 피부·모발 건강, 재생·장수 관련 공동연구도 진행 중이다. 올릭스는 향후 비만 치료제와 CNS 영역에서도 유사한 사업 모델을 추진할 계획이다.

| 인기기사 | 더보기 + |
-
1 에이비엘바이오 'ABL001' 쇼크?…“핵심은 그랩바디 플랫폼” -
2 메지온, FDA 공식 의견 제출...폰탄치료제 ‘JURVIGO’ 승인 가속 -
3 “간의 벽 깨졌다” 올릭스 2.0, 비만·CNS siRNA 신약개발 드라이브 -
4 ‘바이오코리아 2026’ 개막... 혁신과 협력의 장, K-바이오 글로벌 대도약 청사진 제시 -
5 리가켐바이오,김용주 회장-박세진 사장 체제 돌입 -
6 [포토] "혁신과 돌파, 더 나은 미래로" 바이오코리아 2026 개막 -
7 첨단바이오 제품화 병목 풀릴까…식약처, ‘Bio Rise-Up’ 본격 가동 -
8 지아이이노베이션,차세대 폐동맥고혈압 치료제 ‘GI-214’ 특허 출원 -
9 한미,“비만 넘어 항암으로 혁신”..미국암연구학회서 차세대 신약 대거 공개 -
10 "과다 의료이용, 진료 단계서 막는다"…심평원, 실시간 관리 도입
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 권혁진 기자 hjkwon@yakup.com
- 입력 2026.04.29 06:00 수정 2026.04.29 06:18


올릭스가 간 중심 RNA 간섭(RNAi) 치료제 개발에서 벗어나 비만 치료와 중추신경계(CNS)까지 확장하는 ‘올릭스 2.0’ 전략을 제시했다. 핵심은 간 외 조직으로 전달 범위를 넓히는 siRNA 플랫폼 ‘OASIS(OliX Advanced Small Interfering RNA System)’다. 기존 ‘GalNAc’ 기반 간 타깃 siRNA 전달 전략에서 한 단계 나아가, 지방·CNS 등 추가 조직으로 적용 영역을 확장하겠다는 전략이다.
올릭스 이동기 대표는 29일 서울 코엑스에서 열린 ‘바이오코리아 2026’ 컨퍼런스 세션 ‘올리고뉴클레오타이드 치료제’에 연사로 참석해 이 같은 전략을 발표했다.
이 대표는 “현재 상업화된 다수 siRNA 치료제가 GalNAc 기반 전달 기술을 활용해 간에 선택적으로 전달되는 구조에 머물러 있다”며 “OASIS는 siRNA에 지질 결합체(lipid conjugate)와 다양한 타깃 결합 구조를 적용해 지방조직이나 중추신경계와 같은 간 외 조직으로의 전달을 가능하게 하는 플랫폼”이라고 설명했다.
이어 그는 “단순히 전달되는 수준을 넘어, 특정 조직에서 의미 있는 수준의 유전자 발현 억제와 지속성을 동시에 확보한 것이 핵심”이라며 “이를 기반으로 siRNA 치료제를 간 질환 중심에서 대사질환, 신경퇴행성 질환 등으로 확장할 수 있는 개발 기반을 마련했다”고 강조했다. GalNAc은 간세포 표적 siRNA 전달에 쓰이는 리간드로, 미국 바이오텍 앨나일램 파마슈티컬스(Alnylam Pharmaceuticals)가 이를 기반으로 한 전달 기술을 상용화했다.
OASIS 플랫폼, 지방조직 전달 데이터로 ‘간 외 조직 확장’ 제시
OASIS는 올릭스의 기존 asiRNA 및 cp-asiRNA(자가전달 비대칭 siRNA) 기술을 기반으로 지질 결합체, GalNAc, 항체 등 다양한 전달 요소를 통합한 RNAi 플랫폼이다. siRNA 자체 설계 기술에 조직 특이적 전달 요소를 결합해, 기존 간 중심에서 지방·근육·중추신경계(CNS) 등 간 외 조직으로 적용 범위를 확장한 것이 특징이다.
상업화된 siRNA 치료제의 상당수가 GalNAc 기반 전달 기술을 통해 간에 선택적으로 축적되는 구조였다면, OASIS는 특정 조직을 표적으로 하는 전달 전략을 적용해 간 외 조직으로의 분포를 설계하는 플랫폼이다.
실제 비임상 연구에서 해당 플랫폼의 전달 성능이 확인됐다. 발표에 따르면, OASIS 플랫폼 기반 지방조직 표적 siRNA를 마우스에 피하 투여한 결과, 단회 3mg/kg 투여로 지방조직 내 표적 유전자 발현이 약 80% 감소했고, 해당 효과는 2개월 이상 유지됐다. 조직 분포 분석에서도 간 대비 지방조직에서 선택적인 mRNA 감소가 확인됐다.
이는 siRNA 치료제에서 핵심 과제로 꼽히던 조직 선택성과 지속성 측면에서 의미 있는 개선 가능성을 보여주는 데이터로 해석할 수 있다.
이 대표는 “지방조직에서 의미 있는 수준의 유전자 발현 억제와 지속성이 동시에 확인된 점이 중요하다”며 “해당 데이터는 siRNA 치료제의 적용 범위를 실제로 간 외 조직으로 확장할 수 있음을 보여준다”고 설명했다.
ALK7 표적 비만 신약개발 전략…“지방 선택적 감량”
올릭스는 OASIS 플랫폼을 기반으로 지방조직 표적 siRNA 전달 전략을 적용해 비만 치료제 ‘OLX501A’ 개발에 본격 착수했다.
핵심 타깃은 Activin receptor-like kinase 7(ALK7)이다. ALK7은 지방세포에서 지질 분해를 억제하고 에너지 저장을 조절하는 수용체로, 유전자 기능 저해 시 지방 축적이 감소하는 것으로 알려진 유전학적으로 검증된 타깃이다. 올릭스는 siRNA를 통해 ALK7 발현을 억제함으로써 지방조직 내 지질 분해를 촉진하는 접근을 적용하고 있다.
이 대표는 “ALK7 억제를 통해 지방세포의 대사를 저장 중심에서 소비 중심으로 전환하는 것이 핵심”이라며 “지방은 줄이면서 근육은 유지하는 방향의 치료 전략을 목표로 하고 있다”고 설명했다. 이어 “비만 치료제의 평가 기준이 단순 체중 감소에서 체성분 개선으로 이동할 가능성이 있다”고 덧붙였다.
실제 비임상 DIO(diet-induced obesity) 마우스 모델에서 ALK7 siRNA 후보물질은 체중 약 13% 감소를 유도했다. 동시에 지방량은 22.7~30.3% 감소한 반면, 제지방량은 유지되는 경향을 보였다. 단순 체중 감소가 아니라 지방량 감소 중심의 체성분 개선 효과가 확인된 것이다.
전임상 단계에서의 전환 가능성은 영장류 데이터에서도 확인됐다. ALK7 siRNA 후보물질 OLX501A는 비인간 영장류(NHP)에서 SC 3 mg/kg 단회 투여 시 최대 84% 수준의 ALK7 mRNA 감소를 나타냈다.
설치류를 넘어 영장류에서도 강력한 유전자 발현 억제 효과가 재현되면서, RNAi 기반 치료제 개발에서 주요 리스크로 꼽히는 종간 차이에 대한 부담을 일정 부분 낮출 수 있는 근거로 평가된다.
이 대표는 “siRNA 치료제에서 가장 중요한 것은 사람으로 얼마나 잘 이어질 수 있느냐”라며 “영장류 데이터는 그 가능성을 보여주는 핵심 지표로, 효능뿐 아니라 지속성과 용량 측면에서도 경쟁력을 확인하고 있다”고 강조했다.
CNS 확장 전략…“세포 내 타깃 공략” RNAi 강점 부각
올릭스 2.0 전략의 또 다른 방향은 중추신경계다. 회사는 siRNA 기반 치료제가 세포 내(intracellular) 타깃을 직접 억제할 수 있다는 점을 핵심 경쟁력으로 제시했다.
알츠하이머병, 파킨슨병 등 신경퇴행성 질환의 주요 병리 단백질인 타우, 알파-시누클레인은 세포 내 단백질이다. 항체 기반 치료제가 주로 세포 외(extracellular) 타깃에 제한되는 것과 달리, RNAi는 질병 기전에 직접 개입할 수 있는 접근이다.
올릭스는 전달 전략을 단계적으로 설계했다. 초기에는 척수강내(intrathecal) 투여를 통해 CNS 내 siRNA 전달 가능성을 검증하고, 이후 혈뇌장벽(BBB) 투과를 위해 트랜스페린 수용체(TfR1), IGF1R 등을 타깃으로 한 셔틀 기반 전달 기술을 적용하는 구조다. 현재 BBB 셔틀 기술은 외부 플랫폼 기업과의 협업을 통해 개발이 진행되고 있다.
비임상 단계에서는 설치류 모델에서 뇌 영역별 유전자 발현 억제 지속성이 확인됐다. 또한 파킨슨병 PFF(pre-formed fibril) 모델에서는 운동 기능 개선이 관찰되며, siRNA 기반 CNS 치료제의 초기 효능 가능성이 제시됐다.
이 대표는 “CNS 영역은 전달 자체가 가장 큰 장벽이지만, siRNA는 세포 내 타깃을 직접 조절할 수 있다는 점에서 기존 치료제와 차별화된다”며 “2026년 하반기 CNS 영역에서 생체 내 개념 입증(in vivo PoC)을 확보하는 것이 목표”라고 밝혔다.
현재 올릭스는 일라이 릴리와 MASH·비만 후보물질 ‘OLX702A’ 공동개발 및 기술이전 계약을 체결했으며, 한소제약과는 중화권에서 심혈관·대사 등 주요 적응증을 겨냥한 siRNA 치료제 개발·상업화 협력을 진행하고 있다. 로레알과는 RNAi 기술을 활용한 피부·모발 건강, 재생·장수 관련 공동연구도 진행 중이다. 올릭스는 향후 비만 치료제와 CNS 영역에서도 유사한 사업 모델을 추진할 계획이다.


무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
