세계 최초 경구용 마이크로바이옴 치료제가 최근 FDA의 승인을 받으면서 관심이 집중되고 있다. 그러나 현재 수준의 마이크로바이옴 치료제는 블록버스터로 성장하기엔 무리가 있다는 전문가 제언이 나왔다.
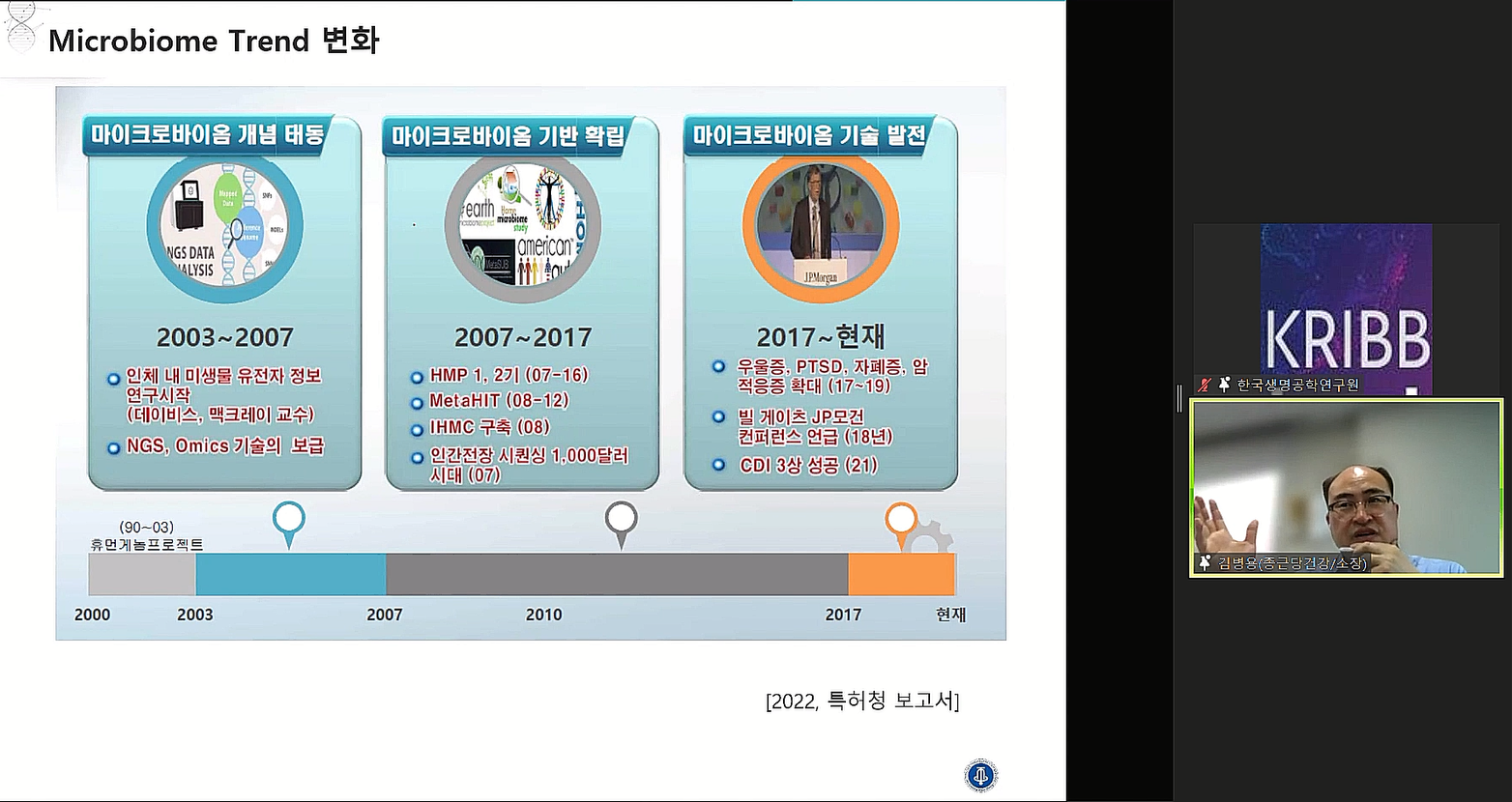
종근당건강 김병용 연구소장은 한국생명공학연구원과 서강대학교가 9일 온라인으로 개최한 ‘제10회 KRIBB 바이오 인더스트리 4.0’에 참석, ‘마이크로바이옴 기술과 산업 동향’을 제목으로 마이크로바이옴(Microbiome) 치료제의 미래 방향을 제시했다.
마이크로바이옴은 미생물과 생태계의 합성어다. 인체 내 공생하는 모든 미생물 군집 또는 군집의 유전정보 전체를 가리킨다. 특히 장내 마이크로바이옴의 무게는 1.5~2kg로 알려졌다. 뇌 1.3kg, 간 1.5kg과 비슷 수준으로 일각에선 제2의 장기라고까지 평가한다.
김 소장은 “현재 마이크로바이옴 치료제는 수십 종의 미생물이 혼합(Cocktail)된 형태로 작용기전(MoA)이 명확하지 않은 한계가 있다”면서 “명확한 작용기전이 입증된 미생물군 또는 단일 종 형태의 표준화되고 정제된 마이크로바이옴 치료제 개발이 필요하다”고 지적했다.
마이크로바이옴 치료제는 최근에만 해도 ‘미래 신약’이란 가능성으로만 존재했다. 지난달 26일 세레스 테라퓨틱스(Seres Therapeutics)의 경구용 마이크로바이옴 치료제 ‘SER-109’가 미국 FDA에 승인을 받으면서 ‘이 시대 신약’으로 현실화됐다.
세레스테라퓨틱스는 수십 종의 미생물을 포자형태로 만들어 표준화했고, 이를 통해 FDA로부터 클로스트리듐 디피실리균(Clostridium difficile) 감염증이 재발(rCDI) 적응증으로 사용 승인을 받았다. 보우스트(Vowst, SER-109)가 임상 3상에서 유효성을 확보했지만, 명확한 작용기전은 추정할 수밖에 없다는 것이 김 소장의 지적이다. 따라서 지금의 상태로는 마이크로바이옴 치료제가 블록버스터로 성장하기엔 한계가 있다는 것이다.
이러한 마이크로바이옴 치료제의 특성과 한계에 따라 주목받던 임상시험도 줄줄이 중단됐다.
에벨로 바이오사이언스(Evelo Biosciences)는 아토피를 적응증으로 ‘EDP2926’의 임상 2b상을 진행했지만, 유효성을 확보하지 못했다. 또 삼중음성 유방암을 적응증으로 한 ‘EDP1503’의 키트루다 병용 임상1/2상에서도 유효성 확보에 실패했다.
세레스테라퓨틱스도 궤양성대장염 적응증 파이프라인 ‘SER-287’은 임상 2b상에서 효능 부족을 확인, 임상시험을 중단했다.
이외에도 신로직 테라퓨틱스(Synlogic Therapeutics), 리터 파마슈티컬스(Ritter pharmaceuticals), 핀지 테라퓨틱스(finch Therapeutics) 등은 개발 중인 마이크로바이옴 파이프라인 중 일부 파이프라인의 임상시험을 중단, 더 이상 진행하지 않겠다고 밝혔다.
김 소장은 지속되는 임상 실패로 인한 마이크로바이옴 위기론에도 불구하고 마이크로바이옴은 미래 신약개발 분야의 성장동력이라는 것을 분명히 했다.
김 소장은 “마이크로바이옴 치료제가 비약적인 발전을 이루기 위해선 ‘표준화와 명확화(CMC)’가 이뤄져야 한다”면서 "염기서열분석(NGS)과 오믹스(Omics) 기술도 지속해서 발전하고 있어 마이크로바이옴 치료제 전망은 밝다”고 내다봤다.
한편 시장조사업체 그랜드뷰리서치(Grand View Research)는 마이크로바이옴 치료제 시장이 현재 1억 1400달러(약 1500억원)에서 2030년에는 10억 6000만 달러(1조 4300억원)를 넘어설 것으로 예상했다. 식품의약품안전처와 국제 규제기관에서 명확한 마이크로바이옴 치료제 개발을 위한 가이드라인을 제·개정 중이다.
| 인기기사 | 더보기 + |
-
1 네이처셀, 미국 순회 사업설명회 개최…"조인트스템 허가·상업화·나스닥 전략 공개" -
2 상장 제약·바이오사 1Q 평균 영업이익 코스피 299억, 코스닥 64억 달성 -
3 강스템바이오텍, ‘오스카’ 2a상 7월 톱라인 예고 "후속 임상·FDA 개발 전략 병행" -
4 차기 건보공단 수장 선임 앞두고…정기석 이사장 돌연 사의 -
5 KASBP 봄 심포지엄, 차세대 연구자 펠로우십 가동…“K-바이오 미래 주역 키운다” -
6 '스타틴 먹지 마라'는 말의 대가…심뇌혈관질환 위험 키운다 -
7 큐리언트, ADC 경쟁력 새 화두 제시…"전달 넘어 페이로드 혁신" -
8 idsTrust, 대웅그룹 SAP 클라우드 전환… 제약·바이오 PCE 선도 도입 -
9 ‘피네레논’, 비당뇨병성 콩팥병 임상 3상 성공…NEJM·JAMA 동시 등판 -
10 동아쏘시오홀딩스, AI 기반 '서비스데스크 AI봇' 도입… 디지털 전환 가속
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 권혁진 기자 hjkwon@yakup.com
- 입력 2023.05.10 06:00 수정 2023.05.14 15:14

세계 최초 경구용 마이크로바이옴 치료제가 최근 FDA의 승인을 받으면서 관심이 집중되고 있다. 그러나 현재 수준의 마이크로바이옴 치료제는 블록버스터로 성장하기엔 무리가 있다는 전문가 제언이 나왔다.
종근당건강 김병용 연구소장은 한국생명공학연구원과 서강대학교가 9일 온라인으로 개최한 ‘제10회 KRIBB 바이오 인더스트리 4.0’에 참석, ‘마이크로바이옴 기술과 산업 동향’을 제목으로 마이크로바이옴(Microbiome) 치료제의 미래 방향을 제시했다.
마이크로바이옴은 미생물과 생태계의 합성어다. 인체 내 공생하는 모든 미생물 군집 또는 군집의 유전정보 전체를 가리킨다. 특히 장내 마이크로바이옴의 무게는 1.5~2kg로 알려졌다. 뇌 1.3kg, 간 1.5kg과 비슷 수준으로 일각에선 제2의 장기라고까지 평가한다.
김 소장은 “현재 마이크로바이옴 치료제는 수십 종의 미생물이 혼합(Cocktail)된 형태로 작용기전(MoA)이 명확하지 않은 한계가 있다”면서 “명확한 작용기전이 입증된 미생물군 또는 단일 종 형태의 표준화되고 정제된 마이크로바이옴 치료제 개발이 필요하다”고 지적했다.

마이크로바이옴 치료제는 최근에만 해도 ‘미래 신약’이란 가능성으로만 존재했다. 지난달 26일 세레스 테라퓨틱스(Seres Therapeutics)의 경구용 마이크로바이옴 치료제 ‘SER-109’가 미국 FDA에 승인을 받으면서 ‘이 시대 신약’으로 현실화됐다.
세레스테라퓨틱스는 수십 종의 미생물을 포자형태로 만들어 표준화했고, 이를 통해 FDA로부터 클로스트리듐 디피실리균(Clostridium difficile) 감염증이 재발(rCDI) 적응증으로 사용 승인을 받았다. 보우스트(Vowst, SER-109)가 임상 3상에서 유효성을 확보했지만, 명확한 작용기전은 추정할 수밖에 없다는 것이 김 소장의 지적이다. 따라서 지금의 상태로는 마이크로바이옴 치료제가 블록버스터로 성장하기엔 한계가 있다는 것이다.
이러한 마이크로바이옴 치료제의 특성과 한계에 따라 주목받던 임상시험도 줄줄이 중단됐다.
에벨로 바이오사이언스(Evelo Biosciences)는 아토피를 적응증으로 ‘EDP2926’의 임상 2b상을 진행했지만, 유효성을 확보하지 못했다. 또 삼중음성 유방암을 적응증으로 한 ‘EDP1503’의 키트루다 병용 임상1/2상에서도 유효성 확보에 실패했다.
세레스테라퓨틱스도 궤양성대장염 적응증 파이프라인 ‘SER-287’은 임상 2b상에서 효능 부족을 확인, 임상시험을 중단했다.
이외에도 신로직 테라퓨틱스(Synlogic Therapeutics), 리터 파마슈티컬스(Ritter pharmaceuticals), 핀지 테라퓨틱스(finch Therapeutics) 등은 개발 중인 마이크로바이옴 파이프라인 중 일부 파이프라인의 임상시험을 중단, 더 이상 진행하지 않겠다고 밝혔다.
김 소장은 지속되는 임상 실패로 인한 마이크로바이옴 위기론에도 불구하고 마이크로바이옴은 미래 신약개발 분야의 성장동력이라는 것을 분명히 했다.
김 소장은 “마이크로바이옴 치료제가 비약적인 발전을 이루기 위해선 ‘표준화와 명확화(CMC)’가 이뤄져야 한다”면서 "염기서열분석(NGS)과 오믹스(Omics) 기술도 지속해서 발전하고 있어 마이크로바이옴 치료제 전망은 밝다”고 내다봤다.
한편 시장조사업체 그랜드뷰리서치(Grand View Research)는 마이크로바이옴 치료제 시장이 현재 1억 1400달러(약 1500억원)에서 2030년에는 10억 6000만 달러(1조 4300억원)를 넘어설 것으로 예상했다. 식품의약품안전처와 국제 규제기관에서 명확한 마이크로바이옴 치료제 개발을 위한 가이드라인을 제·개정 중이다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
