대웅제약 나보타주, 이상반응 '사지 경직' 추가
재심사 결과 발현율 8.31% 확인…3월 반영 예정
입력 2021.01.04 06:00
수정 2021.01.04 09:11
대웅제약의 나보타주 재심사 결과에 따라 사지 경직 등의 새로운 이상사례가 추가됐다.
식품의약품안전처는 지난 12월 29일 대웅제약 나보타주(성분명 클로스트리디움보툴리눔독소A형) 등 5품목에 대해 의약품 재심사 결과에 따른 허가사항 변경을 명령했다.
이는 대웅제약이 지난해 3월 10일 식약처에 제출한 의약품 수입품목 나보타주 등 5품목의 재심사 결과로, 약사법 제32조, 제87조제1항 단서조항 및 '의약품 등의 안전에 관한 규칙' 제8조제3항, 제23조제3항 규정에 의거해 결정됐다.
이번 변경사항으로 이상반응에 '상지 경직'이 추가된다.
국내에서 재심사를 위해 4년 동안 뇌졸중 후 상지국소 근육경직 환자 710명을 대상으로 실시한 시판 후 조사 결과, 이상사례의 발현율은 인과관계와 상관없이 8.31%(59/710명, 총 81건)로 보고됐다.
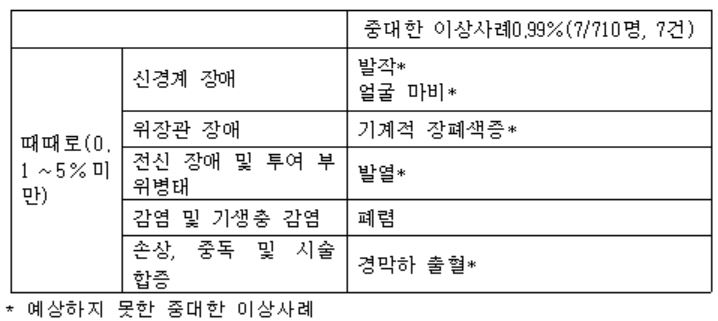
이 중 중대한 약물이상반응 보고는 없었으며, 중대한 이상사례는 발작, 얼굴 마비, 기계적 장폐색증, 발열, 폐렴, 경막하 출혈 순이며 발현율은 0.99%로 710명중 7명에게서 나타났다.
또한 예상하지 못한 이상사례는 두통, 진전, 변비, 발열, 감염, 관절통, 두드러기, 혈뇨 등 72건(6.06%)이 나타났으며, 예상치 못한 이상반응으로 주사 부위 출혈, 두드리기가 2건 확인됐다.
이번 허가사항 변경은 2021년 3월 15일 반영될 예정이다.
식약처는 관련 단체에서는 해당 내용을 주지하는 한편 협회 회원 및 비회원 등에 행정명령을 통보해 허가사항 관리에 착오가 없도록 하고 의약품을 취급하는 병‧의원 및 약국에서 의약품 사용에 적정을 기하도록 협조를 당부했다.
오늘의 헤드라인
전체댓글 0개
등록된 댓글이 없습니다.
| 인기기사 | 더보기 + |
-
1 마이크로니들 신약, FDA 승인 실패 원인은 ‘비임상 설계’ -
2 바이오시밀러 판 바뀐다…임상 간소화 '글로벌 표준' 부상 -
3 제약·바이오 미래 먹거리 발굴, "혁신 모달리티 선점과 입체적 리스크 관리가 성패 가른다" -
4 릴리 경구 비만치료제 미국 FDA 허가..각 국 시장·정책에 미칠 영향은? -
5 아리바이오, 성수현 공동대표 선임.. "경구 치매치료제 AR1001 상용화 박차" -
6 난임 지원 '전액 보장' 전환 신호…치료 패러다임 바뀌나 -
7 국가임상시험지원재단, KIC 2026 프로그램위원장에 이병건 특별고문 위촉 -
8 유한양행, 3월 제약업계 소비자 관심도 1위…한미약품·동국제약 순 -
9 김석진 대한혈액학회 이사장 “혈액암 신약 시대, 면역글로불린 선제적 급여 확대 필수” -
10 바이오젠, 56억달러 승부수…아펠리스 인수로 ‘단기 성장동력’ 확보
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

대웅제약 나보타주, 이상반응 '사지 경직' 추가
재심사 결과 발현율 8.31% 확인…3월 반영 예정
- 박선혜 기자 loveloveslee@yakup.com
- 입력 2021.01.04 06:00 수정 2021.01.04 09:11
대웅제약의 나보타주 재심사 결과에 따라 사지 경직 등의 새로운 이상사례가 추가됐다.
식품의약품안전처는 지난 12월 29일 대웅제약 나보타주(성분명 클로스트리디움보툴리눔독소A형) 등 5품목에 대해 의약품 재심사 결과에 따른 허가사항 변경을 명령했다.
이는 대웅제약이 지난해 3월 10일 식약처에 제출한 의약품 수입품목 나보타주 등 5품목의 재심사 결과로, 약사법 제32조, 제87조제1항 단서조항 및 '의약품 등의 안전에 관한 규칙' 제8조제3항, 제23조제3항 규정에 의거해 결정됐다.
이번 변경사항으로 이상반응에 '상지 경직'이 추가된다.
국내에서 재심사를 위해 4년 동안 뇌졸중 후 상지국소 근육경직 환자 710명을 대상으로 실시한 시판 후 조사 결과, 이상사례의 발현율은 인과관계와 상관없이 8.31%(59/710명, 총 81건)로 보고됐다.

이 중 중대한 약물이상반응 보고는 없었으며, 중대한 이상사례는 발작, 얼굴 마비, 기계적 장폐색증, 발열, 폐렴, 경막하 출혈 순이며 발현율은 0.99%로 710명중 7명에게서 나타났다.
또한 예상하지 못한 이상사례는 두통, 진전, 변비, 발열, 감염, 관절통, 두드러기, 혈뇨 등 72건(6.06%)이 나타났으며, 예상치 못한 이상반응으로 주사 부위 출혈, 두드리기가 2건 확인됐다.
이번 허가사항 변경은 2021년 3월 15일 반영될 예정이다.
식약처는 관련 단체에서는 해당 내용을 주지하는 한편 협회 회원 및 비회원 등에 행정명령을 통보해 허가사항 관리에 착오가 없도록 하고 의약품을 취급하는 병‧의원 및 약국에서 의약품 사용에 적정을 기하도록 협조를 당부했다.
Copyright © Yakup.com All rights reserved.
약업신문 의 모든 컨텐츠(기사)는 저작권법의 보호를 받습니다.
무단 전재·복사·배포 등을 금지합니다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
