한미FTA발효 후, 다국적사 특허만료 '줄줄'
발효 후 3년간 시판방지조치는 시행되지 않아
이혜선 기자
lhs@yakup.com  기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
입력 2011.11.24 06:30
수정 2011.11.24 17:50
한미FTA로 제약산업이 가장 타격을 받는 요인은 허가특허연계제도이다.
이 제도가 시행되면 제네릭사 허가를 받기 위해서는 식약청만이 아니라 원특허권자에게 제네릭을 개발하겠다는 통보를 해야 하며 원특허권자가 이의를 제기하면 제네릭의 출시는 지연된다.
그렇다면 가까운 시일내에 특허가 만료되는 미국계 오리지널 신약은 무엇이 있을까.
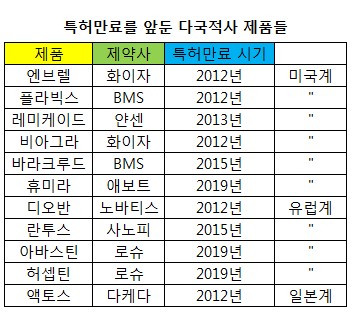 우선 화이자와 얀센, BMS, 애보트가 오는 2019년까지 블록버스터급 신약 특허의 만료를 앞두고 있다.
우선 화이자와 얀센, BMS, 애보트가 오는 2019년까지 블록버스터급 신약 특허의 만료를 앞두고 있다.
화이자는 2012년에 류마티즘 관절염 치료제인 엔브렐과 발기부전치료제인 비아그라 등의 특허만료(물질특허)를 앞두고 있다. 비아그라의 용도특허는 2014년에 만료된다.
얀센이 최근 판권을 회수한 류마티즘관절염 치료제 레미케이드의 특허만료는 2013년이며 B형간염치료제 1위인 BMS의 바라크루드가 2015년, 항혈전제 1위인 BMS/사노피의 플라빅스가 2012년 특허만료를 앞두고 있다. 또한 애보트의 류마티즘관절염치료제 휴미라는 2019년에 특허만료가 예정돼 있다.
그 외에 다국적 제약사 중에는 노바티스의 디오반, 다케다의 액토스가 2012년 특허만료를 앞두고 있고 베링거인겔하임의 미카르디스가 2013년, 로슈의 허셉틴, 아바스틴이 2019년에 특허가 만료된다.
물론 이번 한미FTA 비준안 통과로 허가특허연계제도가 곧바로 시행되는 것은 아니며 지난해 추가협상결과로 '시판방지조치'는 3년간 유예된다.
한미FTA 비준 이후 절차가 남아 있는데 비준안이 통과되면 국회는 15일 이내에 통과된 비준안을 정부에 넘겨야 한다.
그 이후에 미국과 한국은 FTA 절차를 마무리했다는 내용의 문서를 교환하게 된다.
이때, 문서 교환을 위해서는 한미FTA관련 법안의 제정 및 개정이 필요한데, 국회 본회의에서 한미FTA 비준안을 통과시키면서 14개 법안도 직권으로 일괄상정한 상태다.
이와 같은 법적 절차가 완료되면 미국과 한국이 확인서한을 교환하고 60일 후면 두 나라가 합의한 날짜를 기점으로 FTA는 발효되게 된다. 정부는 그 시점을 내년 1월 1일로 예상하고 있다.
물론, 비준안이 예정대로 발효되고 허가특허연계제도가 시행된다고 해도 제네릭판매가 완전 중단되는 것은 아니다.
그러나 허가특허연계제도로 인해 최대 1년 정도 제네릭 발매가 지연되기 때문에 국내제약사의 피해는 불가피할 전망이다.
이 제도가 시행되면 제네릭사 허가를 받기 위해서는 식약청만이 아니라 원특허권자에게 제네릭을 개발하겠다는 통보를 해야 하며 원특허권자가 이의를 제기하면 제네릭의 출시는 지연된다.
그렇다면 가까운 시일내에 특허가 만료되는 미국계 오리지널 신약은 무엇이 있을까.

화이자는 2012년에 류마티즘 관절염 치료제인 엔브렐과 발기부전치료제인 비아그라 등의 특허만료(물질특허)를 앞두고 있다. 비아그라의 용도특허는 2014년에 만료된다.
얀센이 최근 판권을 회수한 류마티즘관절염 치료제 레미케이드의 특허만료는 2013년이며 B형간염치료제 1위인 BMS의 바라크루드가 2015년, 항혈전제 1위인 BMS/사노피의 플라빅스가 2012년 특허만료를 앞두고 있다. 또한 애보트의 류마티즘관절염치료제 휴미라는 2019년에 특허만료가 예정돼 있다.
그 외에 다국적 제약사 중에는 노바티스의 디오반, 다케다의 액토스가 2012년 특허만료를 앞두고 있고 베링거인겔하임의 미카르디스가 2013년, 로슈의 허셉틴, 아바스틴이 2019년에 특허가 만료된다.
물론 이번 한미FTA 비준안 통과로 허가특허연계제도가 곧바로 시행되는 것은 아니며 지난해 추가협상결과로 '시판방지조치'는 3년간 유예된다.
한미FTA 비준 이후 절차가 남아 있는데 비준안이 통과되면 국회는 15일 이내에 통과된 비준안을 정부에 넘겨야 한다.
그 이후에 미국과 한국은 FTA 절차를 마무리했다는 내용의 문서를 교환하게 된다.
이때, 문서 교환을 위해서는 한미FTA관련 법안의 제정 및 개정이 필요한데, 국회 본회의에서 한미FTA 비준안을 통과시키면서 14개 법안도 직권으로 일괄상정한 상태다.
이와 같은 법적 절차가 완료되면 미국과 한국이 확인서한을 교환하고 60일 후면 두 나라가 합의한 날짜를 기점으로 FTA는 발효되게 된다. 정부는 그 시점을 내년 1월 1일로 예상하고 있다.
물론, 비준안이 예정대로 발효되고 허가특허연계제도가 시행된다고 해도 제네릭판매가 완전 중단되는 것은 아니다.
그러나 허가특허연계제도로 인해 최대 1년 정도 제네릭 발매가 지연되기 때문에 국내제약사의 피해는 불가피할 전망이다.
오늘의 헤드라인
전체댓글 0개
등록된 댓글이 없습니다.

한미FTA발효 후, 다국적사 특허만료 '줄줄'
발효 후 3년간 시판방지조치는 시행되지 않아
- 이혜선 기자 lhs@yakup.com
- 입력 2011.11.24 06:30 수정 2011.11.24 17:50
한미FTA로 제약산업이 가장 타격을 받는 요인은 허가특허연계제도이다.
이 제도가 시행되면 제네릭사 허가를 받기 위해서는 식약청만이 아니라 원특허권자에게 제네릭을 개발하겠다는 통보를 해야 하며 원특허권자가 이의를 제기하면 제네릭의 출시는 지연된다.
그렇다면 가까운 시일내에 특허가 만료되는 미국계 오리지널 신약은 무엇이 있을까.
 우선 화이자와 얀센, BMS, 애보트가 오는 2019년까지 블록버스터급 신약 특허의 만료를 앞두고 있다.
우선 화이자와 얀센, BMS, 애보트가 오는 2019년까지 블록버스터급 신약 특허의 만료를 앞두고 있다.
화이자는 2012년에 류마티즘 관절염 치료제인 엔브렐과 발기부전치료제인 비아그라 등의 특허만료(물질특허)를 앞두고 있다. 비아그라의 용도특허는 2014년에 만료된다.
얀센이 최근 판권을 회수한 류마티즘관절염 치료제 레미케이드의 특허만료는 2013년이며 B형간염치료제 1위인 BMS의 바라크루드가 2015년, 항혈전제 1위인 BMS/사노피의 플라빅스가 2012년 특허만료를 앞두고 있다. 또한 애보트의 류마티즘관절염치료제 휴미라는 2019년에 특허만료가 예정돼 있다.
그 외에 다국적 제약사 중에는 노바티스의 디오반, 다케다의 액토스가 2012년 특허만료를 앞두고 있고 베링거인겔하임의 미카르디스가 2013년, 로슈의 허셉틴, 아바스틴이 2019년에 특허가 만료된다.
물론 이번 한미FTA 비준안 통과로 허가특허연계제도가 곧바로 시행되는 것은 아니며 지난해 추가협상결과로 '시판방지조치'는 3년간 유예된다.
한미FTA 비준 이후 절차가 남아 있는데 비준안이 통과되면 국회는 15일 이내에 통과된 비준안을 정부에 넘겨야 한다.
그 이후에 미국과 한국은 FTA 절차를 마무리했다는 내용의 문서를 교환하게 된다.
이때, 문서 교환을 위해서는 한미FTA관련 법안의 제정 및 개정이 필요한데, 국회 본회의에서 한미FTA 비준안을 통과시키면서 14개 법안도 직권으로 일괄상정한 상태다.
이와 같은 법적 절차가 완료되면 미국과 한국이 확인서한을 교환하고 60일 후면 두 나라가 합의한 날짜를 기점으로 FTA는 발효되게 된다. 정부는 그 시점을 내년 1월 1일로 예상하고 있다.
물론, 비준안이 예정대로 발효되고 허가특허연계제도가 시행된다고 해도 제네릭판매가 완전 중단되는 것은 아니다.
그러나 허가특허연계제도로 인해 최대 1년 정도 제네릭 발매가 지연되기 때문에 국내제약사의 피해는 불가피할 전망이다.
이 제도가 시행되면 제네릭사 허가를 받기 위해서는 식약청만이 아니라 원특허권자에게 제네릭을 개발하겠다는 통보를 해야 하며 원특허권자가 이의를 제기하면 제네릭의 출시는 지연된다.
그렇다면 가까운 시일내에 특허가 만료되는 미국계 오리지널 신약은 무엇이 있을까.

화이자는 2012년에 류마티즘 관절염 치료제인 엔브렐과 발기부전치료제인 비아그라 등의 특허만료(물질특허)를 앞두고 있다. 비아그라의 용도특허는 2014년에 만료된다.
얀센이 최근 판권을 회수한 류마티즘관절염 치료제 레미케이드의 특허만료는 2013년이며 B형간염치료제 1위인 BMS의 바라크루드가 2015년, 항혈전제 1위인 BMS/사노피의 플라빅스가 2012년 특허만료를 앞두고 있다. 또한 애보트의 류마티즘관절염치료제 휴미라는 2019년에 특허만료가 예정돼 있다.
그 외에 다국적 제약사 중에는 노바티스의 디오반, 다케다의 액토스가 2012년 특허만료를 앞두고 있고 베링거인겔하임의 미카르디스가 2013년, 로슈의 허셉틴, 아바스틴이 2019년에 특허가 만료된다.
물론 이번 한미FTA 비준안 통과로 허가특허연계제도가 곧바로 시행되는 것은 아니며 지난해 추가협상결과로 '시판방지조치'는 3년간 유예된다.
한미FTA 비준 이후 절차가 남아 있는데 비준안이 통과되면 국회는 15일 이내에 통과된 비준안을 정부에 넘겨야 한다.
그 이후에 미국과 한국은 FTA 절차를 마무리했다는 내용의 문서를 교환하게 된다.
이때, 문서 교환을 위해서는 한미FTA관련 법안의 제정 및 개정이 필요한데, 국회 본회의에서 한미FTA 비준안을 통과시키면서 14개 법안도 직권으로 일괄상정한 상태다.
이와 같은 법적 절차가 완료되면 미국과 한국이 확인서한을 교환하고 60일 후면 두 나라가 합의한 날짜를 기점으로 FTA는 발효되게 된다. 정부는 그 시점을 내년 1월 1일로 예상하고 있다.
물론, 비준안이 예정대로 발효되고 허가특허연계제도가 시행된다고 해도 제네릭판매가 완전 중단되는 것은 아니다.
그러나 허가특허연계제도로 인해 최대 1년 정도 제네릭 발매가 지연되기 때문에 국내제약사의 피해는 불가피할 전망이다.
Copyright © Yakup.com All rights reserved.
약업신문 의 모든 컨텐츠(기사)는 저작권법의 보호를 받습니다.
무단 전재·복사·배포 등을 금지합니다.
무단 전재·복사·배포 등을 금지합니다.



