제일약품, 제조 3개 품목 허가 취소
잔류용매 시험 자료를 거짓 작성·제출해 품목 허가 획득
입력 2021.10.27 12:30

제일약품의 제품 3가지가 품목허가 취소 절차에 들어간다.
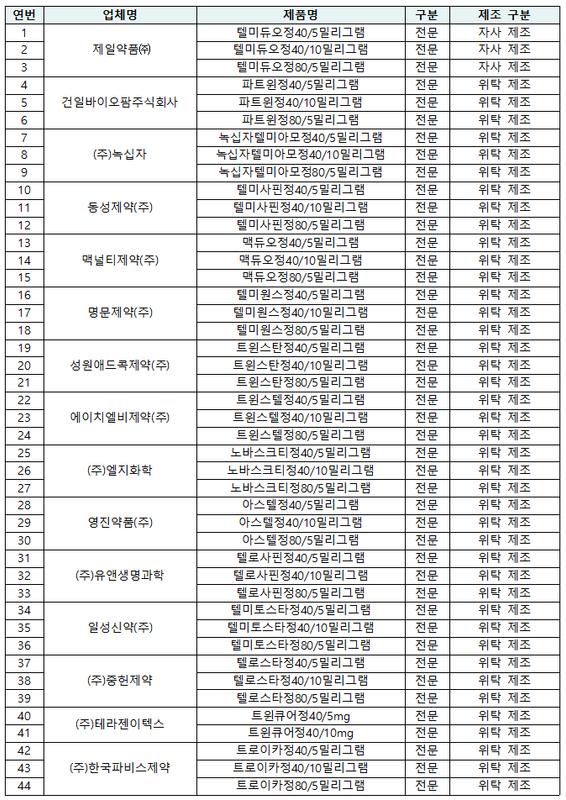
식품의약품안전처(처장 김강립)는 제일약품㈜이 제조한 `텔미듀오정40/5밀리그램’ 등 3개 품목에 대하여 잠정 제조·판매 중지와 회수 조치하고 품목허가 취소 절차에 착수했다고 밝혔다.
제일약품에서 `텔미듀오정40/5밀리그램’ 등 3개 품목과 동일하게 위탁 제조하는 품목 중 동일한 허가 신청자료를 제출해 허가받은 14개사 41개 품목도 잠정 제조·판매 중지와 회수 조치하고 품목허가 취소 절차를 진행한다.
식약처에 따르면 `의약품 GMP 특별 기획점검단`이 제일약품에 대해 점검(9.27.~10.8.)한 결과, 제일약품이 `텔미듀오정40/5밀리그램’ 등 3개 품목의 허가를 위해 제출한 자료 중 잔류용매 시험 자료가 허위로 작성됐음을 확인했다.
업체가 거짓·부정한 방법으로 품목허가를 받은 경우('약사법' 제76조제1항제2호의3 위반) 해당 품목은 품목허가 취소 처분 절차가 진행된다.
식약처는 해당 44개 품목을 대체 의약품으로 전환하고 제품 회수가 적절히 수행되도록 의‧약사 등 전문가의 협조를 요청하는 안전성 속보를 의‧약사, 소비자 단체에 배포한 상태다.
또한 보건복지부와 건강보험심사평가원에 병·의원에서 해당 품목이 처방되지 않도록 조치해 줄 것을 요청했다.
오늘의 헤드라인
전체댓글 0개
등록된 댓글이 없습니다.
| 인기기사 | 더보기 + |
-
1 [창간 72주년] 디앤디파마텍 이슬기 대표 “비만치료제, 전달 전략 바꿔야 주사제 넘는다” -
2 제네릭 약가 45% 대폭 인하 '초강수'… 약가제도 전면 개편안 건정심 통과 -
3 [창간 72주년] 인벤티지랩 김주희 대표 "투여 주기 혁신‥빅파마 제형 기술 파트너 자리매김" -
4 “일본 줄기세포 치료 5592명·8030건 10년 데이터 공개…치료 옵션 증명” -
5 [약업분석] 파미셀, 바이오케미컬 고성장 지속…영업익 6배 급증 -
6 운명의 26일, 약가제도 수술대 오른다… '제네릭 인하' 폭풍 전야 제약업계 -
7 비보존제약, 매출 감소 속 적자 지속…수익성 악화 -
8 [창간 72주년] 저주파 진동이 만든 뇌 속 소용돌이…아리바이오,치매 치료 새 길 연다 -
9 세마글루타이드 복제약 쏟아진다…시장 ‘혼전’ 예상 -
10 [창간 72주년] "차세대 위고비는 나의 것" 유한·한미·대웅·일동·동아 비만치료제 총력전
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

제일약품, 제조 3개 품목 허가 취소
잔류용매 시험 자료를 거짓 작성·제출해 품목 허가 획득
- 최윤수 기자 jjysc0229@yakup.com
- 입력 2021.10.27 12:30

제일약품의 제품 3가지가 품목허가 취소 절차에 들어간다.
식품의약품안전처(처장 김강립)는 제일약품㈜이 제조한 `텔미듀오정40/5밀리그램’ 등 3개 품목에 대하여 잠정 제조·판매 중지와 회수 조치하고 품목허가 취소 절차에 착수했다고 밝혔다.
제일약품에서 `텔미듀오정40/5밀리그램’ 등 3개 품목과 동일하게 위탁 제조하는 품목 중 동일한 허가 신청자료를 제출해 허가받은 14개사 41개 품목도 잠정 제조·판매 중지와 회수 조치하고 품목허가 취소 절차를 진행한다.
식약처에 따르면 `의약품 GMP 특별 기획점검단`이 제일약품에 대해 점검(9.27.~10.8.)한 결과, 제일약품이 `텔미듀오정40/5밀리그램’ 등 3개 품목의 허가를 위해 제출한 자료 중 잔류용매 시험 자료가 허위로 작성됐음을 확인했다.
업체가 거짓·부정한 방법으로 품목허가를 받은 경우('약사법' 제76조제1항제2호의3 위반) 해당 품목은 품목허가 취소 처분 절차가 진행된다.
식약처는 해당 44개 품목을 대체 의약품으로 전환하고 제품 회수가 적절히 수행되도록 의‧약사 등 전문가의 협조를 요청하는 안전성 속보를 의‧약사, 소비자 단체에 배포한 상태다.
또한 보건복지부와 건강보험심사평가원에 병·의원에서 해당 품목이 처방되지 않도록 조치해 줄 것을 요청했다.

Copyright © Yakup.com All rights reserved.
약업신문 의 모든 컨텐츠(기사)는 저작권법의 보호를 받습니다.
무단 전재·복사·배포 등을 금지합니다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
