승인건수는 1개 품목을 여러 제약사가 공동으로 진행하는 생동성시험이 가능해진 2011년 이후 감소 추세를 보였으나, 2015년에는 전년도에 비해 재심사 또는 특허 만료 예정 의약품이 늘어나면서 승인 건수가 증가했다.
지난해 승인된 생동성시험의 주요 특징은 △치료영역별 정신신경계의약품 개발 최다 △재심사 또는 특허 만료예정인 의약품 개발 집중 등이다.
◇정신신경계의약품 4년째 개발 최다
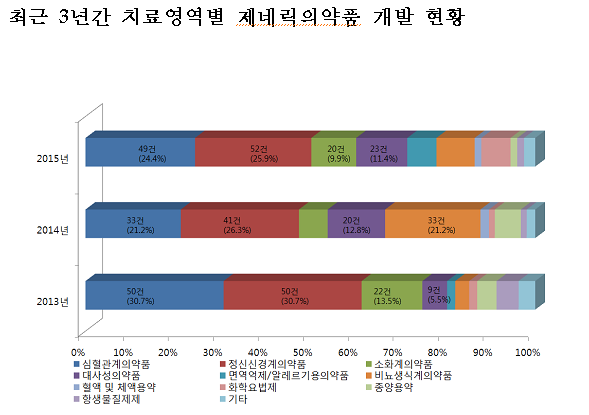
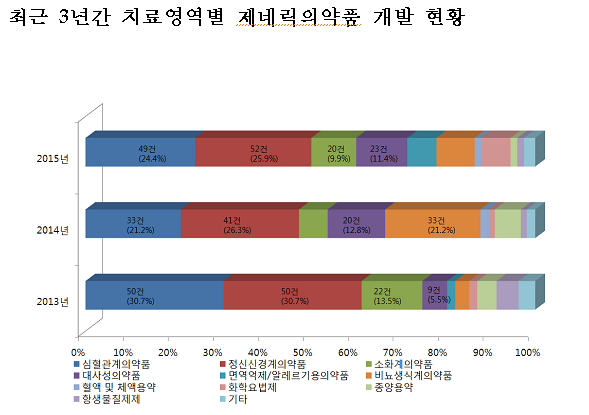
치료영역별 승인건수는 정신신경계의약품 52건(25.9%), 심혈관계의약품 49건(24.4%), 대사성의약품 23건(11.4%), 소화계의약품 20건(9.9%), 비뇨‧생식기계의약품 17건(8.4%), 화학요법제 13건(6.5%) 등의 순이었다.
스트레스 증가와 고령화 등의 영향으로 불안 우울장애, 치매 등을 치료하는 정신신경계의약품이 2011년 이후 4년 연속으로 가장 많이 승인되었으며, 심혈관계의약품이 뒤를 이어 매년 개발이 꾸준히 이루어지고 있다.
이들 심혈관계의약품 및 정신신경계의약품은 2015년 전체 승인건수의 절반을 넘는 것으로 나타났다.
화학요법제는 2014년에 승인건수가 2건에서 지난해 13건으로 급격히 증가하였으며, 이는 특허만료에 따라 화학요법제에 대한 개발이 많았기 때문인 것으로 분석된다.
반면, 비뇨·생식기계의약품의 경우 타다라필 등의 특허만료로 2014년에는 33건으로 증가하였으나, 2015년에는 개발이 주춤하여 17건으로 급감했다.
◇재심사 또는 특허 만료예정 의약품 개발 집중
지난해 재심사 또는 특허만료 예정인 제네릭의약품 개발을 위한 생동성시험 승인건수는 148건으로 전체(201건)의 73.6%에 달했다.
올해 6월 재심사가 만료되는 텔미사르탄, 암로디핀 복합제가 11건으로 가장 많았고 뇌기질성 정신증후군에 사용되는 콜린알포세레이트와 치매치료제 도네페질이 각각 그 뒤를 이었다.
지난해 승인을 처음받은 성분인 테노포비르와 티카글렐러는 2017년 재심사 만료예정인 품목이다.
식약처는 스트레스 증가 및 고령화 등의 영향으로 심혈관계의약품, 정신신경계의약품의 개발이 증가 추세에 있으며, 재심사 또는 특허만료예정 의약품에 대한 개발도 지속적으로 증가할 것으로 전망된다고 설명하였다.
생동성 승인 현황은 온라인의약도서관(http://drug.mfds.go.kr) 생동성주간승인정보]에서 주단위로 확인할 수 있으며, 제약업계는 물론 누구나 제네릭의약품 개발동향을 신속히 확인할 수 있도록 생동성시험 승인현황을 지속적으로 제공할 예정이다.
| 인기기사 | 더보기 + |
-
1 메지온 '유데나필', 폰탄환자 복용 관련 미국특허 등록 -
2 오름테라퓨틱, AACR서 CD123 표적 DAC ‘ORM-1153’ 전임상 데이터 발표 예정 -
3 “항암제 대세 여전히, 당분간 'ADC'…다음 주자 '이중특이항체' 전망” -
4 “구원투수, 드디어 등판” 네오이뮨텍 임상전문가 '김태경 CEO' 체제 출범 -
5 제네릭 40% 인하·신속등재 추진…약가개편 두고 '이견' -
6 리센스메디컬, 수요예측 흥행…공모가 1만1000원 확정 -
7 [약업분석]SK바이오사이언스, 유럽 매출 1000억→4000억 폭풍성장 -
8 경보제약, 아산공장 미국 FDA 현장 실사 통과 -
9 [직장 문화 탐방] DKSH코리아, "채용·성장·문화 하나로 연결…결국 '사람'이 중심" -
10 미·이란 장기전 돌입? 제약·바이오 '삼중고' 직면… "생존 골든타임 놓치지 말아야"
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 신은진 기자 ejshin@yakup.com
- 입력 2016.02.23 09:45 수정 2016.02.23 09:54


승인건수는 1개 품목을 여러 제약사가 공동으로 진행하는 생동성시험이 가능해진 2011년 이후 감소 추세를 보였으나, 2015년에는 전년도에 비해 재심사 또는 특허 만료 예정 의약품이 늘어나면서 승인 건수가 증가했다.
지난해 승인된 생동성시험의 주요 특징은 △치료영역별 정신신경계의약품 개발 최다 △재심사 또는 특허 만료예정인 의약품 개발 집중 등이다.
◇정신신경계의약품 4년째 개발 최다
치료영역별 승인건수는 정신신경계의약품 52건(25.9%), 심혈관계의약품 49건(24.4%), 대사성의약품 23건(11.4%), 소화계의약품 20건(9.9%), 비뇨‧생식기계의약품 17건(8.4%), 화학요법제 13건(6.5%) 등의 순이었다.
스트레스 증가와 고령화 등의 영향으로 불안 우울장애, 치매 등을 치료하는 정신신경계의약품이 2011년 이후 4년 연속으로 가장 많이 승인되었으며, 심혈관계의약품이 뒤를 이어 매년 개발이 꾸준히 이루어지고 있다.
이들 심혈관계의약품 및 정신신경계의약품은 2015년 전체 승인건수의 절반을 넘는 것으로 나타났다.
화학요법제는 2014년에 승인건수가 2건에서 지난해 13건으로 급격히 증가하였으며, 이는 특허만료에 따라 화학요법제에 대한 개발이 많았기 때문인 것으로 분석된다.
반면, 비뇨·생식기계의약품의 경우 타다라필 등의 특허만료로 2014년에는 33건으로 증가하였으나, 2015년에는 개발이 주춤하여 17건으로 급감했다.
◇재심사 또는 특허 만료예정 의약품 개발 집중
지난해 재심사 또는 특허만료 예정인 제네릭의약품 개발을 위한 생동성시험 승인건수는 148건으로 전체(201건)의 73.6%에 달했다.
올해 6월 재심사가 만료되는 텔미사르탄, 암로디핀 복합제가 11건으로 가장 많았고 뇌기질성 정신증후군에 사용되는 콜린알포세레이트와 치매치료제 도네페질이 각각 그 뒤를 이었다.
지난해 승인을 처음받은 성분인 테노포비르와 티카글렐러는 2017년 재심사 만료예정인 품목이다.
식약처는 스트레스 증가 및 고령화 등의 영향으로 심혈관계의약품, 정신신경계의약품의 개발이 증가 추세에 있으며, 재심사 또는 특허만료예정 의약품에 대한 개발도 지속적으로 증가할 것으로 전망된다고 설명하였다.
생동성 승인 현황은 온라인의약도서관(http://drug.mfds.go.kr) 생동성주간승인정보]에서 주단위로 확인할 수 있으며, 제약업계는 물론 누구나 제네릭의약품 개발동향을 신속히 확인할 수 있도록 생동성시험 승인현황을 지속적으로 제공할 예정이다.
무단 전재·복사·배포 등을 금지합니다.



 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
