AI 영상처리 기능 갖춘 소프트웨어 FDA 개별 허가
 기자가 쓴 기사 더보기
기자가 쓴 기사 더보기
의료 및 산업용 영상 솔루션 전문기업 뷰웍스(대표 김후식)는 자사의 디지털 의료영상 획득 및 처리 소프트웨어 ‘브이엑스뷰’(VXvue) 제품이 미국 FDA로부터 시판 전 허가(510K) 승인을 획득했다고 12일 밝혔다. 이로써 뷰웍스는 북미 시장에 엑스레이 디텍터 및 전용 소프트웨어가 결합된 시스템 일체를 공급할 수 있게 돼, 시장 경쟁력을 더욱 확보하게 됐다.
뷰웍스는 창사 이래 처음으로 FDA로부터 AI 기반 영상처리 알고리즘을 포함한 소프트웨어로 승인을 획득했다. 특히 기존보다 강화된 당국 심사 기준에 맞춰 시판 의료기기와 동등성, 품질관리 절차와 사후관리 체계를 입증하는 등 기술 역량과 신뢰성을 확보했다.
뷰웍스에 따르면 자체 개발한 브이엑스뷰는 엑스레이 디텍터를 통해 획득한 임상 이미지의 송출과 처리를 수행하는 사용자 중심 소프트웨어로, 임상 이미지의 선명도를 높이는 ‘퓨어임팩트’(PureImpact™) 알고리즘을 탑재해 인체 연조직과 골격 세부 묘사에 뛰어나다. 이와 함께 인체용, 수의용, 차량내 검진 등 진료 대상과 방식에 따라 세분화된 프리셋을 제공하는 등 편의성을 높였다.
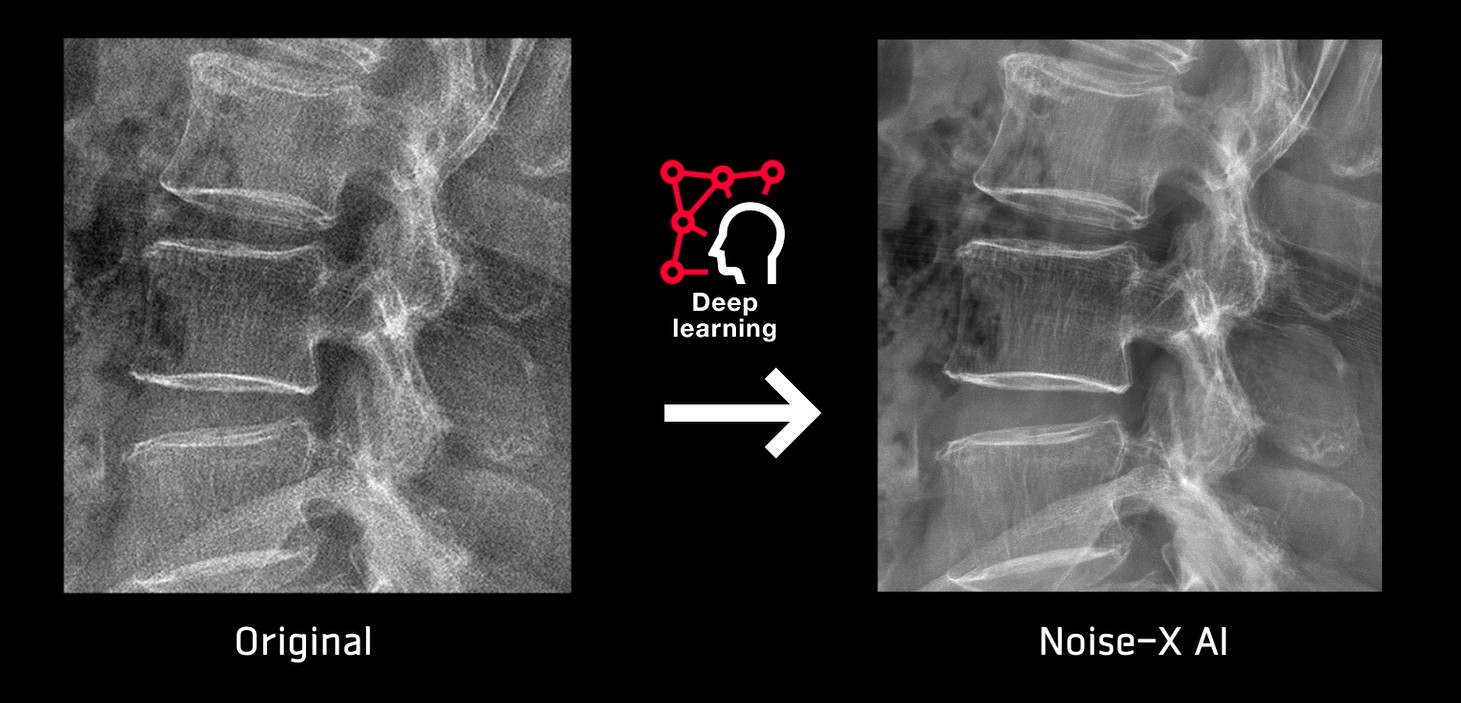
최근 다수 AI 기반 영상처리 솔루션을 내부 기능으로 통합하며 편의성과 사용성을 대폭 강화했다. 흉부 엑스레이 이미지에서 연조직 가시성을 높이는 ‘본엑스’(Bone-X AI), 딥러닝 기반 알고리즘으로 영상 노이즈를 저감하는 ‘노이즈엑스’(Noise-X AI) 등 분야별로 특화된 기능을 갖췄다.
뷰웍스는 FDA 승인과 유럽 CE 인증 등을 빠르게 늘리며 기술력을 인정받고 있다. 지난해 11월 장형 디텍터 ‘VIVIX-S 1751S’, 올해 1월 유방촬영술(맘모그래피)용 엑스레이 디텍터 ‘VIVIX-M 1824S’ 및 ‘VIVIX-M 2430S’에 대해 FDA 승인을 취득했다. 이어 지난 5월 슬라이드 스캐너 신제품 'VISQUE DPS(Digital Pathology System) LH510'에 대해 유럽 체외진단의료기기 인증인 'CE IVDR'을 획득했다.
이를 통해 뷰웍스는 인증 제품들을 주력으로 영업망 확대 및 마케팅에 적극 나선다는 전략이다. 이달 말 북미 최대 영상의학 전시회 RSNA 2025에서 신소재 엑스레이 디텍터와 신규 영상처리 솔루션이 탑재된 브이엑스뷰 등 FDA 승인 솔루션을 대거 선보일 계획이다.
뷰웍스 관계자는 “이번 FDA 승인으로 뷰웍스는 하드웨어 뿐만 아니라 소프트웨어 분야에서도 글로벌 기술 우위를 갖춘 기업임을 증명했다”며, “저선량 방사선 촬영, 병원 내 데이터 관리, 협진 용이성 등 최근 헬스케어 트렌드에 부합하는 고부가가치 제품을 꾸준히 선보이는 한편, 관련 규제 변화에 적극 대응해 나가겠다”고 말했다.
| 인기기사 | 더보기 + |
-
1 삼천당제약, 아일리아 바이오시밀러 독점공급-판매계약 7개국에 프랑스 추가 -
2 [첨생법 날개달다] 차바이오텍 “준비는 끝났다…이제 세계 무대서 승부할 것” -
3 디앤디파마텍 MASH 치료제 임상2상 AASLD ‘Late-Breaking Abstract’ 발표 -
4 네이처셀, 라정찬-정상목 사내이사 선임 -
5 '제약 · 바이오· 헬스케어' 최신 기술 한 자리에...AI 신약개발 고도화 가속 -
6 식약처, ‘사전상담 핫라인’ 본격 준비… “혁신제품 규제 장벽 낮춘다” -
7 현대약품,저용량 고혈압치료제 ‘현대미녹시딜정 2.5mg’ 품목허가 승인 -
8 강스템바이오텍,'퓨어스템-에이디주' 반복투여 임상1/2a상 IND 변경 승인 -
9 디앤디파마텍, MASH 치료제 'DD01' 이스라엘 특허 등록 결정 -
10 소비자와 '대화'하는 시대…뷰티 마케팅 공식 바뀌었다
| 인터뷰 | 더보기 + |
| PEOPLE | 더보기 + |
| 컬쳐/클래시그널 | 더보기 + |

- 이권구 기자 kwon9@yakup.com
- 입력 2025.11.12 08:50 수정 2025.11.12 08:58

의료 및 산업용 영상 솔루션 전문기업 뷰웍스(대표 김후식)는 자사의 디지털 의료영상 획득 및 처리 소프트웨어 ‘브이엑스뷰’(VXvue) 제품이 미국 FDA로부터 시판 전 허가(510K) 승인을 획득했다고 12일 밝혔다. 이로써 뷰웍스는 북미 시장에 엑스레이 디텍터 및 전용 소프트웨어가 결합된 시스템 일체를 공급할 수 있게 돼, 시장 경쟁력을 더욱 확보하게 됐다.
뷰웍스는 창사 이래 처음으로 FDA로부터 AI 기반 영상처리 알고리즘을 포함한 소프트웨어로 승인을 획득했다. 특히 기존보다 강화된 당국 심사 기준에 맞춰 시판 의료기기와 동등성, 품질관리 절차와 사후관리 체계를 입증하는 등 기술 역량과 신뢰성을 확보했다.
뷰웍스에 따르면 자체 개발한 브이엑스뷰는 엑스레이 디텍터를 통해 획득한 임상 이미지의 송출과 처리를 수행하는 사용자 중심 소프트웨어로, 임상 이미지의 선명도를 높이는 ‘퓨어임팩트’(PureImpact™) 알고리즘을 탑재해 인체 연조직과 골격 세부 묘사에 뛰어나다. 이와 함께 인체용, 수의용, 차량내 검진 등 진료 대상과 방식에 따라 세분화된 프리셋을 제공하는 등 편의성을 높였다.
최근 다수 AI 기반 영상처리 솔루션을 내부 기능으로 통합하며 편의성과 사용성을 대폭 강화했다. 흉부 엑스레이 이미지에서 연조직 가시성을 높이는 ‘본엑스’(Bone-X AI), 딥러닝 기반 알고리즘으로 영상 노이즈를 저감하는 ‘노이즈엑스’(Noise-X AI) 등 분야별로 특화된 기능을 갖췄다.
뷰웍스는 FDA 승인과 유럽 CE 인증 등을 빠르게 늘리며 기술력을 인정받고 있다. 지난해 11월 장형 디텍터 ‘VIVIX-S 1751S’, 올해 1월 유방촬영술(맘모그래피)용 엑스레이 디텍터 ‘VIVIX-M 1824S’ 및 ‘VIVIX-M 2430S’에 대해 FDA 승인을 취득했다. 이어 지난 5월 슬라이드 스캐너 신제품 'VISQUE DPS(Digital Pathology System) LH510'에 대해 유럽 체외진단의료기기 인증인 'CE IVDR'을 획득했다.
이를 통해 뷰웍스는 인증 제품들을 주력으로 영업망 확대 및 마케팅에 적극 나선다는 전략이다. 이달 말 북미 최대 영상의학 전시회 RSNA 2025에서 신소재 엑스레이 디텍터와 신규 영상처리 솔루션이 탑재된 브이엑스뷰 등 FDA 승인 솔루션을 대거 선보일 계획이다.
뷰웍스 관계자는 “이번 FDA 승인으로 뷰웍스는 하드웨어 뿐만 아니라 소프트웨어 분야에서도 글로벌 기술 우위를 갖춘 기업임을 증명했다”며, “저선량 방사선 촬영, 병원 내 데이터 관리, 협진 용이성 등 최근 헬스케어 트렌드에 부합하는 고부가가치 제품을 꾸준히 선보이는 한편, 관련 규제 변화에 적극 대응해 나가겠다”고 말했다.
무단 전재·복사·배포 등을 금지합니다.



